Luftfreie Technik - Air-free technique
Luftfreie Techniken beziehen sich auf eine Reihe von Manipulationen im Chemielabor für die Handhabung von Verbindungen , die luftempfindlich . Diese Techniken verhindern, dass die Verbindungen mit Luftbestandteilen , üblicherweise Wasser und Sauerstoff , reagieren . seltener Kohlendioxid und Stickstoff . Ein gemeinsames Thema unter diesen Techniken ist die Verwendung eines feinen (10 0 –10 –3 Torr) oder hohen (10 –3 –10 –6 Torr) Vakuums zum Entfernen von Luft und die Verwendung eines Inertgases : vorzugsweise Argon , aber oft Stickstoff .
Die beiden häufigsten Arten der luftfreien Technik umfassen die Verwendung eines Handschuhfachs und einer Schlenk-Leitung , obwohl einige strenge Anwendungen eine Hochvakuumleitung verwenden. Bei beiden Methoden werden Glaswaren (häufig Schlenk-Röhrchen ) vor der Verwendung in Öfen vorgetrocknet. Sie können flammgetrocknet werden, um adsorbiertes Wasser zu entfernen. Bevor sie in eine inerte Atmosphäre gelangen, werden die Gefäße durch Spülen und Nachfüllen weiter getrocknet. Das Gefäß wird einem Vakuum ausgesetzt, um Gase und Wasser zu entfernen, und dann mit Inertgas nachgefüllt. Dieser Zyklus wird normalerweise dreimal wiederholt oder das Vakuum wird über einen längeren Zeitraum angelegt. Einer der Unterschiede zwischen der Verwendung eines Handschuhfachs und einer Schlenk-Linie besteht darin, dass der Spül- und Nachfüllzyklus angewendet wird. Bei Verwendung eines Handschuhfachs wird das Spülen und Nachfüllen auf eine Luftschleuse angewendet, die am Handschuhfach angebracht ist und üblicherweise als "Port" oder "Vorkammer" bezeichnet wird. Im Gegensatz dazu wird bei Verwendung einer Schlenk-Leitung das Spülen und Nachfüllen über einen Schlauch oder eine gemahlene Glasverbindung, die mit dem Verteiler verbunden ist, direkt auf das Reaktionsgefäß aufgebracht.
Handschuhfach
Die einfachste Art der luftfreien Technik ist die Verwendung eines Handschuhfachs . Ein Handschuhbeutel verwendet dieselbe Idee, ist jedoch normalerweise ein schlechterer Ersatz, da er schwieriger zu reinigen und weniger gut versiegelt ist. Es gibt erfinderische Möglichkeiten, auf Gegenstände zuzugreifen, die außerhalb der Reichweite der Handschuhe liegen, beispielsweise die Verwendung von Zangen und Schnüren. Die Hauptnachteile bei der Verwendung eines Handschuhfachs sind die Kosten des Handschuhfachs und die eingeschränkte Geschicklichkeit beim Tragen der Handschuhe.
In der Handschuhbox können herkömmliche Laborgeräte häufig eingerichtet und manipuliert werden, obwohl das Gerät mit den Handschuhen gehandhabt werden muss. Durch die Bereitstellung einer abgedichteten, aber umlaufenden Atmosphäre des Inertgases erfordert das Handschuhfach nur wenige andere Vorsichtsmaßnahmen. Eine Kreuzkontamination von Proben aufgrund einer schlechten Technik ist ebenfalls problematisch, insbesondere wenn ein Handschuhfach zwischen Arbeitern geteilt wird, die unterschiedliche Reagenzien verwenden, insbesondere flüchtige .
Bei der Verwendung von Handschuhboxen für die synthetische Chemie haben sich zwei Stile entwickelt . In einem konservativeren Modus werden sie ausschließlich zum Speichern, Wiegen und Übertragen luftempfindlicher Reagenzien verwendet . Die Reaktionen werden danach unter Verwendung von Schlenk-Techniken durchgeführt. Die Handschuhboxen werden daher nur für die luftempfindlichsten Stufen eines Experiments verwendet. In ihrer liberaleren Verwendung werden Handschuhboxen für die gesamten Synthesevorgänge verwendet, einschließlich Reaktionen in Lösungsmitteln, Aufarbeitung und Vorbereitung von Proben für die Spektroskopie.
Nicht alle Reagenzien und Lösungsmittel sind für die Verwendung in der Handschuhbox akzeptabel, obwohl verschiedene Labors unterschiedliche Kulturen verwenden. Die "Kastenatmosphäre" wird üblicherweise kontinuierlich an einem Kupferkatalysator von Sauerstoff befreit. Bestimmte flüchtige Chemikalien wie halogenierte Verbindungen und besonders stark koordinierende Spezies wie Phosphine und Thiole können problematisch sein, da sie den Kupferkatalysator irreversibel vergiften. Aus diesem Grund entscheiden sich viele Experimentatoren dafür, solche Verbindungen mit Schlenk-Techniken zu handhaben. Bei der liberaleren Verwendung von Handschuhboxen wird angenommen, dass der Kupferkatalysator häufiger ausgetauscht werden muss, aber diese Kosten werden als akzeptabler Kompromiss für die Effizienz der Durchführung einer gesamten Synthese in einer geschützten Umgebung angesehen
Schlenk-Linie
Die andere Haupttechnik zur Herstellung und Handhabung luftempfindlicher Verbindungen ist mit der Verwendung einer Schlenk-Linie verbunden. Die Haupttechniken umfassen:
- Gegenstromzusätze, bei denen dem Reaktionsgefäß luftstabile Reagenzien gegen einen Inertgasstrom zugesetzt werden.
- die Verwendung von Spritzen und Gummisepta (Stopfen, die nach dem Einstechen wieder verschließen), um Flüssigkeiten und Lösungen zu übertragen
-
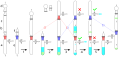
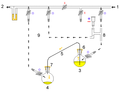
Kanülentransfer , bei dem Flüssigkeiten oder Lösungen luftempfindlicher Reagenzien zwischen verschiedenen mit Septen verschlossenen Gefäßen unter Verwendung eines langen, dünnen Röhrchens, das als Kanüle bezeichnet wird, übertragen werden. Der Flüssigkeitsstrom wird über Vakuum oder Inertgasdruck erreicht.
 Eine Kanüle wird verwendet, um THF vom Kolben rechts zum Kolben links zu übertragen.
Eine Kanüle wird verwendet, um THF vom Kolben rechts zum Kolben links zu übertragen.
Glaswaren werden normalerweise über fest sitzende und gefettete Glasschliffverbindungen verbunden . Runde Biegungen von Glasrohren mit gemahlenen Glasverbindungen können verwendet werden, um die Ausrichtung verschiedener Gefäße anzupassen. Die Filtration kann mit speziellen Geräten durchgeführt werden.
Zugehörige Vorbereitungen
Im Handel erhältliches gereinigtes Inertgas (Argon oder Stickstoff) ist für die meisten Zwecke ausreichend. Für bestimmte Anwendungen ist es jedoch erforderlich, Wasser und Sauerstoff weiter zu entfernen. Diese zusätzliche Reinigung kann erreicht werden, indem die Inertgasleitung durch eine beheizte Kupferkatalysatorsäule geleitet wird , die den Sauerstoff in Kupferoxid umwandelt. Wasser wird entfernt, indem das Gas durch eine Trockenmittelsäule wie Phosphorpentoxid oder Molekularsiebe geleitet wird.
Luft- und wasserfreie Lösungsmittel sind ebenfalls erforderlich. Wenn in mit Stickstoff gespülten Winchestern hochreine Lösungsmittel verfügbar sind , können diese direkt in das Handschuhfach gebracht werden. Zur Verwendung mit der Schlenk-Technik können sie schnell in mit Molekularsieben beladene Schlenkkolben gegossen und entgast werden . Typischerweise wird das Lösungsmittel direkt von einer Destillierkolonne oder einer Lösungsmittelreinigungssäule abgegeben.
Entgasung
Zwei Verfahren zur Entgasung sind üblich. Das erste ist als Gefrierpumpen-Auftauen bekannt - das Lösungsmittel wird unter flüssigem Stickstoff eingefroren und ein Vakuum angelegt. Danach wird der Absperrhahn geschlossen und das Lösungsmittel in warmem Wasser aufgetaut, so dass eingeschlossene Gasblasen entweichen können.
Das zweite Verfahren besteht darin, das Lösungsmittel einfach einem Vakuum auszusetzen. Rühren oder mechanisches Rühren unter Verwendung eines Ultraschallgeräts ist nützlich. Gelöste Gase entstehen zuerst; Sobald das Lösungsmittel zu verdampfen beginnt, was durch Kondensation außerhalb der Kolbenwände festgestellt wird, wird der Kolben wieder mit Inertgas gefüllt. Beide Verfahren werden dreimal wiederholt.
Trocknen
Lösungsmittel sind eine Hauptkontaminationsquelle bei chemischen Reaktionen. Obwohl traditionelle Trocknungstechniken die Destillation aus einem aggressiven Trockenmittel beinhalten , sind Molekularsiebe weit überlegen.
| Trockenmittel | Trocknungsdauer | Wassergehalt |
|---|---|---|
| unbehandelt | 0 h | 225 ppm |
| Natrium / Benzophenon | 48 h | 31 ppm |
| 3 Å Molekularsiebe | 24 h | 0,9 ppm |
Natrium als Trockenmittel (unter seinem Schmelzpunkt) ist nicht nur ineffizient, sondern reagiert auch langsam mit Spuren von Wasser. Wenn das Trockenmittel jedoch löslich ist, wird die Trocknungsgeschwindigkeit beschleunigt, obwohl sie Molekularsieben immer noch unterlegen ist. Benzophenon wird oft verwendet, um ein solches lösliches Trocknungsmittel zu erzeugen. Ein Vorteil dieser Anwendung ist die intensive blaue Farbe des Ketyl Radikalanion . Somit kann Natrium / Benzophenon als Indikator für luftfreie und feuchtigkeitsfreie Bedingungen bei der Reinigung von Lösungsmitteln durch Destillation verwendet werden.
Destillationsstills sind brandgefährlich und werden zunehmend durch alternative Lösungsmitteltrocknungssysteme ersetzt. Beliebt sind Systeme zur Filtration von sauerstofffreien Lösungsmitteln durch mit aktiviertem Aluminiumoxid gefüllte Säulen .
Das Trocknen von Feststoffen kann erreicht werden, indem der Feststoff über einem Trocknungsmittel wie Phosphorpentoxid ( P) gelagert wird
2 Ö
5 ) oder Kieselgel , Lagerung in einem Trocken- / Vakuumtrocknungsofen, Erhitzen unter Hochvakuum oder in einer Trockenpistole oder zum Entfernen von Spuren von Wasser, einfaches Lagern des Feststoffs in einem Handschuhfach mit trockener Atmosphäre.
Alternativen
Beide Techniken erfordern ziemlich teure Ausrüstung und können zeitaufwändig sein. Wenn die Anforderungen an die Luftfreiheit nicht streng sind, können andere Techniken verwendet werden. Beispielsweise kann die Verwendung eines Opferüberschusses eines Reagens verwendet werden, das mit Wasser / Sauerstoff reagiert. Der Opferüberschuss "trocknet" die Reaktion durch Reaktion mit dem Wasser (z. B. im Lösungsmittel). Dieses Verfahren ist jedoch nur geeignet, wenn die bei dieser Reaktion erzeugten Verunreinigungen das gewünschte Reaktionsprodukt nicht beeinträchtigen oder leicht entfernt werden können. Typischerweise sind Reaktionen unter Verwendung eines solchen Opferüberschusses nur dann wirksam, wenn Reaktionen in einem vernünftig großen Maßstab durchgeführt werden, so dass diese Nebenreaktion im Vergleich zu der gewünschten Produktreaktion vernachlässigbar ist. Beispielsweise wird bei der Herstellung von Grignard-Reagenzien häufig Magnesium (das billigste Reagenz) im Überschuss verwendet, das reagiert, um Spurenwasser zu entfernen, entweder durch direkte Reaktion mit Wasser zu Magnesiumhydroxid oder durch In-situ- Bildung des Grignard-Reagens, das wiederum reagiert mit Wasser (zB R-Mg-X + H 2 O → HO-Mg-X + RH). Zu der resultierenden „trockenen“ Umgebung aufrechtzuerhalten , ist es in der Regel ausreichend , um ein zu verbinden Schutzrohr gefüllt mit Calciumchlorid zu dem Rückflußkondensator zu langsam Feuchtigkeit Neueingabe der Reaktion im Laufe der Zeit, oder schließt eine Inertgasleitung .
Das Trocknen kann auch durch Verwendung von In-situ- Trockenmitteln wie Molekularsieben oder durch Verwendung azeotroper Destillationstechniken , z. B. mit einer Dean-Stark-Apparatur, erreicht werden .
Siehe auch
Verweise
- ^ Duward F. Shriver und MA Drezdzon "Die Manipulation luftempfindlicher Verbindungen" 1986, J. Wiley and Sons: New York. ISBN 0-471-86773-X .
- ^ Johansen, Martin B.; Kondrup, Jens C.; Scharnier, Mogene; Lindhardt, Anders T. (13. Juni 2018). "Verbesserte Sicherheit beim Transfer von pyrophorem tert-Butyllithium aus Kolben mit Schutzdichtungen". Forschung und Entwicklung organischer Prozesse . 22 (7): 903–905. doi : 10.1021 / acs.oprd.8b00151 .
- ^ Brown, HC "Organische Synthesen über Borane" John Wiley & Sons, Inc. New York: 1975. ISBN 0-471-11280-1 .
- ^ "Gefrierpumpen-Auftauen-Entgasung von Flüssigkeiten" (PDF) . Universität von Washington .
- ^ Williams, DBG, Lawton, M., "Trocknen von organischen Lösungsmitteln: Quantitative Bewertung der Effizienz mehrerer Trockenmittel", The Journal of Organic Chemistry 2010, vol. 75, 8351. doi : 10.1021 / jo101589h
- ^ Nathan L. Bauld (2001). "Einheit 6: Anionenradikale" . Universität von Texas .
- ^ WLF Armarego; C. Chai (2003). Reinigung von Laborchemikalien . Oxford: Butterworth-Heinemann. ISBN 0-7506-7571-3 .
- ^ Pangborn, AB; Giardello, MA; Grubbs, RH; Rosen, RK; Timmers, FJ (1996). "Sicheres und bequemes Verfahren zur Lösungsmittelreinigung". Metallorganika . 15 (5): 1518–20. doi : 10.1021 / om9503712 .
Externe Links
- Rob Toreki (24.05.2004). "Handschuhboxen" . Die Glaswarengalerie . Interaktive Lernparadigmen integriert.
- Rob Toreki (25.05.2004). "Schlenkleitungen und Vakuumleitungen" . Die Glaswarengalerie . Interaktive Lernparadigmen integriert.
- Jürgen Heck. "Der integrierte Synthesekurs: Schlenk-Technik" (PDF) . Universität Hamburg . Archiviert vom Original (Nachdruck an der norwegischen Universität für Wissenschaft und Technologie) am 09.03.2008.
- "AL-134: Handhabung und Lagerung luftempfindlicher Reagenzien" (PDF) . Technisches Bulletin . Sigma-Aldrich .
- R. John Errington (3. Juli 1997). Fortgeschrittene praktische anorganische und metallorganische Chemie . ISBN 9780751402254 .
- John Leonard; B. Lygo; Garry Procter (2. Juni 1994). Fortgeschrittene praktische organische Chemie . ISBN 9780748740710 .
Galerie
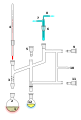
Perkin-Dreieck : Luftempfindliche Destillationen