Aluminiumhydrid - Aluminium hydride

|
|
| Namen | |
|---|---|
|
Bevorzugter IUPAC-Name
Aluminiumhydrid |
|
|
Systematischer IUPAC-Name
Alumane |
|
| Andere Namen
Alane
|
|
| Bezeichner | |
|
3D-Modell ( JSmol )
|
|
| ChEBI | |
| ChemSpider | |
| ECHA-Infokarte |
100.029.139 |
| 245 | |
|
PubChem- CID
|
|
| UNII | |
|
CompTox-Dashboard ( EPA )
|
|
|
|
|
|
| Eigenschaften | |
| AlH 3 | |
| Molmasse | 29,99 g/mol |
| Aussehen | weißer kristalliner Feststoff, nichtflüchtige, hochpolymerisierte, nadelförmige Kristalle |
| Dichte | 1,477 g/cm 3 , fest |
| Schmelzpunkt | 150 °C (302 °F; 423 K) beginnt sich bei 105 °C (221 °F) zu zersetzen |
| reagiert | |
| Löslichkeit | löslich in Ether reagiert in Ethanol |
| Thermochemie | |
|
Wärmekapazität ( C )
|
40,2 J/mol K |
|
Std molare
Entropie ( S |
30 J/mol K |
|
Std
Bildungsenthalpie (Δ f H ⦵ 298 ) |
-11,4 kJ/mol |
|
Gibbs freie Energie (Δ f G ˚)
|
46,4 kJ/mol |
| Verwandte Verbindungen | |
|
Verwandte Verbindungen
|
Lithiumaluminiumhydrid , Diboran |
|
Sofern nicht anders angegeben, beziehen sich die Daten auf Materialien im Standardzustand (bei 25 °C [77 °F], 100 kPa). |
|
|
|
|
| Infobox-Referenzen | |
Aluminiumhydrid (auch bekannt als Alan oder Aluman) ist eine anorganische Verbindung mit der Formel Al H 3 . Es stellt sich als weißer Feststoff dar und kann mit abnehmender Partikelgröße und Verunreinigungsgrad grau gefärbt sein. Je nach Synthesebedingungen kann die Oberfläche des Alans mit einer dünnen Schicht aus Aluminiumoxid und/oder -hydroxid passiviert werden. Alan und seine Derivate werden als Reduktionsmittel in der organischen Synthese verwendet .
Struktur
Alan ist ein Polymer. Daher wird seine Formel manchmal mit der Formel (AlH 3 ) n dargestellt . Alan bildet zahlreiche Polymorphe , die als α-Alan, α'-Alan, β-Alan, -Alan, δ-Alan, ε-Alan und ζ-Alan bezeichnet werden. α-Alan hat eine kubische oder rhomboedrische Morphologie, während α'-Alan nadelartige Kristalle bildet und γ-Alan ein Bündel verschmolzener Nadeln bildet. Alan ist in Tetrahydrofuran (THF) und Ether löslich. Die Fällungsrate von festem Alan aus Ether variiert mit dem Herstellungsverfahren.
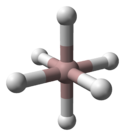
Die Kristallstruktur von α-Alan wurde bestimmt und weist Aluminiumatome auf, die von 6 Wasserstoffatomen umgeben sind, die zu 6 anderen Aluminiumatomen überbrücken. Die Al-H-Abstände sind alle gleich (172 pm) und der Al-H-Al-Winkel beträgt 141°.
 |
 |

|
| α-AlH 3 Einheitszelle | Al-Koordination | H-Koordination |
α-Alane ist das thermisch stabilste Polymorph. β-Alan und γ-Alan werden zusammen hergestellt und wandeln sich beim Erhitzen in α-Alan um. δ, und θ-Alan werden unter noch anderen Kristallisationsbedingungen hergestellt. Obwohl sie weniger thermisch stabil sind, wandeln sich δ-, ε- und θ-Polymorphe beim Erhitzen nicht in α-Alan um.
Molekülformen von Alan
Monomeres AlH 3 wurde bei niedriger Temperatur in einer festen Edelgasmatrix isoliert und erwies sich als planar. Das Dimer Al 2 H 6 wurde in festem Wasserstoff isoliert. Es ist isostrukturell mit Diboran (B 2 H 6 ) und Digallan (Ga 2 H 6 ).
Vorbereitung
Aluminiumhydride und verschiedene Komplexe davon sind seit langem bekannt. Seine erste Synthese wurde 1947 veröffentlicht und ein Patent für die Synthese wurde 1999 erteilt. Aluminiumhydrid wird hergestellt, indem Lithiumaluminiumhydrid mit Aluminiumtrichlorid behandelt wird . Das Verfahren ist kompliziert: Auf die Entfernung von Lithiumchlorid muss geachtet werden .
- 3 LiAlH 4 + AlCl 3 → 4 AlH 3 + 3 LiCl
Die Etherlösung von Alan erfordert eine sofortige Verwendung, da polymeres Material schnell als Feststoff ausfällt. Es ist bekannt, dass Aluminiumhydridlösungen nach 3 Tagen abgebaut werden. Aluminiumhydrid ist reaktiver als LiAlH 4 .
Es gibt mehrere andere Methoden zur Herstellung von Aluminiumhydrid:
- 2 LiAlH 4 + BeCl 2 → 2 AlH 3 + Li 2 BeH 2 Cl 2
- 2 LiAlH 4 + H 2 SO 4 → 2 AlH 3 + Li 2 SO 4 + 2 H 2
- 2 LiAlH 4 + ZnCl 2 → 2 AlH 3 + 2 LiCl + ZnH 2
- 2 LiAlH 4 + I 2 → 2 AlH 3 + 2 LiI + H 2
Elektrochemische Synthese
Mehrere Gruppen haben gezeigt, dass Alan elektrochemisch hergestellt werden kann . Verschiedene elektrochemische Alan-Herstellungsverfahren wurden patentiert. Die elektrochemische Erzeugung von Alan vermeidet Chloridverunreinigungen. Zwei mögliche Mechanismen werden für die Bildung von Alan in Clasens elektrochemischer Zelle diskutiert, die THF als Lösungsmittel, Natriumaluminiumhydrid als Elektrolyt, eine Aluminiumanode und einen in Quecksilber (Hg) getauchten Eisendraht (Hg) als Kathode enthält. Das Natrium bildet mit der Hg-Kathode ein Amalgam, wodurch Nebenreaktionen verhindert werden, und der in der ersten Reaktion erzeugte Wasserstoff könnte aufgefangen und mit dem Natrium-Quecksilber-Amalgam zurückreagiert werden, um Natriumhydrid zu erzeugen. Das System von Clasen führt zu keinem Verlust an Ausgangsmaterial. Bei unlöslichen Anoden findet Reaktion 1 statt, während bei löslichen Anoden eine anodische Auflösung gemäß Reaktion 2 erwartet wird:
- AlH 4 − - e − → AlH 3 · nTHF + 1 ⁄ 2 H 2
- 3AlH 4 − + Al - 3e − → 4AlH 3 · nTHF
In Reaktion 2 wird die Aluminiumanode verbraucht, was die Produktion von Aluminiumhydrid für eine gegebene elektrochemische Zelle begrenzt.
Die Kristallisation und Rückgewinnung von Aluminiumhydrid aus elektrochemisch erzeugtem Alan wurde demonstriert.
Hochdruckhydrierung von Aluminiummetall
α-AlH 3 kann durch Hydrierung von Aluminiummetall bei 10 GPa und 600 °C (1.112 °F) hergestellt werden. Die Reaktion zwischen dem verflüssigten Wasserstoff erzeugt &agr;-AlH 3 , das unter Umgebungsbedingungen gewonnen werden könnte.
Reaktionen
Bildung von Addukten mit Lewis-Basen
AlH 3 bildet leicht Addukte mit starken Lewis-Basen . Zum Beispiel bilden sich mit Trimethylamin sowohl 1:1- als auch 1:2-Komplexe . Der 1:1-Komplex ist in der Gasphase tetraedrisch, in der Festphase jedoch dimer mit verbrückenden Wasserstoffzentren (NMe 3 Al(μ-H)) 2 . Der 1:2-Komplex nimmt eine trigonal-bipyramidale Struktur an . Einige Addukte (zB Dimethylethylamin Alan, NMe 2 Et · AlH 3 ) zersetzen sich thermisch zu Aluminiummetall und können in MOCVD- Anwendungen Verwendung finden.
Sein Komplex mit Diethylether bildet sich nach folgender Stöchiometrie:
- AlH 3 + (C 2 H 5 ) 2 O → H 3 Al · O(C 2 H 5 ) 2
Die Reaktion mit Lithiumhydrid in Ether erzeugt Lithiumaluminiumhydrid :
- AlH 3 + LiH → LiAlH 4
Reduzierung der Funktionsgruppen
In der organischen Chemie wird Aluminiumhydrid hauptsächlich zur Reduktion funktioneller Gruppen verwendet. In vielerlei Hinsicht ähnelt die Reaktivität von Aluminiumhydrid der von Lithiumaluminiumhydrid . Aluminiumhydrid reduziert Aldehyde , Ketone , Carbonsäuren , Anhydride , Säurechloride , Ester und Lactone zu ihren entsprechenden Alkoholen . Amide , Nitrile und Oxime werden zu ihren entsprechenden Aminen reduziert .
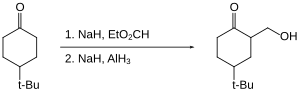
In Bezug auf die Selektivität für funktionelle Gruppen unterscheidet sich Alan von anderen Hydridreagentien. Beispielsweise ergibt bei der folgenden Cyclohexanon-Reduktion Lithiumaluminiumhydrid ein trans:cis-Verhältnis von 1,9:1, während Aluminiumhydrid ein trans:cis-Verhältnis von 7,3:1 ergibt.
Alan ermöglicht die Hydroxymethylierung bestimmter Ketone (d. h. den Ersatz von CH durch C-CH 2 OH an der Alpha-Position ). Das Keton selbst wird nicht reduziert, da es als Enolat "geschützt" ist.
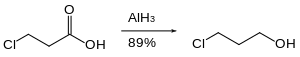
Organohalogenide werden durch Aluminiumhydrid langsam oder gar nicht reduziert. Daher können reaktive funktionelle Gruppen wie Carbonsäuren in Gegenwart von Halogeniden reduziert werden.
Nitrogruppen werden durch Aluminiumhydrid nicht reduziert. Ebenso kann Aluminiumhydrid die Reduktion eines Esters in Gegenwart von Nitrogruppen bewirken .
Aluminiumhydrid kann bei der Reduktion von Acetalen zu halbgeschützten Diolen verwendet werden.
Aluminiumhydrid kann auch in der Epoxidringöffnungsreaktion verwendet werden, wie unten gezeigt.
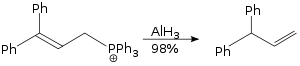
Die mit Aluminiumhydrid durchgeführte allylische Umlagerungsreaktion ist eine S N 2 -Reaktion und sterisch nicht anspruchsvoll.
Aluminiumhydrid reduziert beim Erhitzen sogar Kohlendioxid zu Methan :
- 4 AlH 3 + 3 CO 2 → 3 CH 4 + 2 Al 2 O 3
Hydroaluminierung
Es wurde gezeigt, dass Aluminiumhydrid an Propargylalkohole addiert . Zusammen mit Titantetrachlorid verwendet , kann Aluminiumhydrid an Doppelbindungen addieren . Die Hydroborierung ist eine ähnliche Reaktion.
Kraftstoff
In seiner passivierten Form ist Alane ein aktiver Kandidat für die Speicherung von Wasserstoff und kann für eine effiziente Stromerzeugung über Brennstoffzellenanwendungen, einschließlich Brennstoffzellen- und Elektrofahrzeuge und andere leichte Stromanwendungen, verwendet werden. AlH 3 enthält bis zu 10 Gew.-% Wasserstoff, entsprechend 148 g H 2 /L oder der doppelten Wasserstoffdichte von flüssigem H 2 . In seiner nicht passivierten Form ist Alan auch ein vielversprechendes Raketentreibstoffadditiv , das eine Impulseffizienzsteigerung von bis zu 10 % erreichen kann.
Vorsichtsmaßnahmen
Alan ist nicht selbstentzündlich. Es sollte ähnlich gehandhabt werden wie andere komplexe Metallhydrid-Reduktionsmittel wie Lithiumaluminiumhydrid. Alan zersetzt sich in Luft und Wasser, obwohl die Passivierung die Zersetzungsrate stark verringert. Passiviertes Alan wird generell der Gefahrenklasse 4,3 (Chemikalien, die in Berührung mit Wasser entzündbare Gase entwickeln) zugeordnet.
Verweise
Externe Links
- Aluminiumhydrid in der Chemical Database von EnvironmentalChemistry.com
- Wasserstoffspeicherung vom Brookhaven National Laboratory
- Aluminiumtrihydrid auf WebElements