Americium(III)-chlorid - Americium(III) chloride
|
|
| Namen | |
|---|---|
|
IUPAC-Name
Americium(III)-chlorid
|
|
|
Systematischer IUPAC-Name
Americium(3+)chlorid |
|
| Andere Namen
Americiumchlorid
Americiumtrichlorid |
|
| Bezeichner | |
|
3D-Modell ( JSmol )
|
|
| ChemSpider | |
|
PubChem- CID
|
|
|
|
|
|
| Eigenschaften | |
| Bin Cl 3 | |
| Molmasse | 349 g·mol -1 |
| Aussehen | Hellrote, opake Kristalle |
| Dichte | 5,87 gcm -3 |
| Schmelzpunkt | 715 °C (1.319 °F; 988 K) |
| Siedepunkt | 850 °C (1.560 °F; 1.120 K) |
| Struktur | |
| hexagonal ( UCl 3 Typ ), hP8 | |
| P6 3 /m, Nr. 176 | |
| Dreifach überkappt trigonal prismatisch (Neun-Koordinaten) |
|
| Verwandte Verbindungen | |
|
Andere Kationen
|
Europium(III)-chlorid |
|
Sofern nicht anders angegeben, beziehen sich die Daten auf Materialien im Standardzustand (bei 25 °C [77 °F], 100 kPa). |
|
|
|
|
| Infobox-Referenzen | |
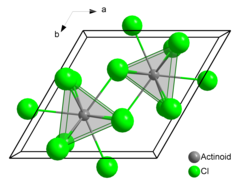
Americium(III)chlorid oder Americiumtrichlorid ist die chemische Verbindung aus Americium und Chlor mit der Formel AmCl 3 . Es bildet rosa sechseckige Kristalle. Im Festkörper hat jedes Americiumatom neun Chloratome als nahe Nachbarn in ungefähr gleichem Abstand in einer dreifachen trigonal-prismatischen Konfiguration.
Das Hexahydrat hat eine monokline Kristallstruktur mit: a = 970,2 pm, b = 656,7 pm und c = 800,9 pm; β = 93° 37'; Raumgruppe: P 2/ n .
Reaktionen
Es wurde ein Americium(III)-Chlorid- Elektroraffinationsverfahren untersucht, um Gemische von Actiniden zu trennen , da die freie Gibbs-Standard-Bildungsenergie von Americium(III)-Chlorid sich stark von den übrigen Actinidenchloriden unterscheidet. Dies kann verwendet werden, um Americium aus Plutonium zu entfernen, indem das Rohgemisch zusammen mit Salzen wie Natriumchlorid geschmolzen wird .
Verweise
