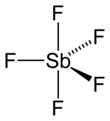
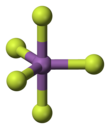
Antimonpentafluorid - Antimony pentafluoride
|
|
|||
| Namen | |||
|---|---|---|---|
|
IUPAC-Name
Antimon (V) fluorid
|
|||
| Andere Namen
Antimonpenta
pentafluoridoantimony |
|||
| Kennungen | |||
|
3D-Modell ( JSmol )
|
|||
| ChemSpider | |||
| ECHA InfoCard |
100.029.110 |
||
| EG-Nummer | |||
|
PubChem CID
|
|||
| RTECS-Nummer | |||
| UNII | |||
| UN-Nummer | 1732 | ||
|
CompTox Dashboard ( EPA )
|
|||
|
|||
|
|||
| Eigenschaften | |||
| SbF 5 | |||
| Molmasse | 216,74 g / mol | ||
| Aussehen | farblose ölige Flüssigkeit hygroskopisch |
||
| Geruch | scharf | ||
| Dichte | 2,99 g / cm 3 | ||
| Schmelzpunkt | 8,3 ° C (46,9 ° F; 281,4 K) | ||
| Siedepunkt | 149,5 ° C (301,1 ° F; 422,6 K) | ||
| Reagiert | |||
| Löslichkeit | löslich in KF , flüssiges SO 2 | ||
| Gefahren | |||
| Hauptgefahren | Gibt Flusssäure bei Kontakt mit Wasser oder biologischen Geweben frei | ||
| Sicherheitsdatenblatt | ICSC 0220 | ||
| GHS-Piktogramme |
  
|
||
| GHS Signalwort | Achtung | ||
| H302 , H314 , H332 , H411 , H412 | |||
| P260 , P261 , P264 , P270 , P271 , P273 , P280 , P301 + 312 , P301 + 330 + 331 , P303 + 361 + 353 , P304 + 312 , P304 + 340 , P305 + 351 + 338 , P310 , P312 , P321 , P330 , P363 , P391 , P405 , P501 | |||
| NFPA 704 (Feuerdiamant) | |||
| NIOSH (US-amerikanische Expositionsgrenzwerte): | |||
|
PEL (zulässig)
|
TWA 0,5 mg / m 3 (als Sb) | ||
|
REL (empfohlen)
|
TWA 0,5 mg / m 3 (als Sb) | ||
| Verwandte Verbindungen | |||
|
Andere Anionen
|
Antimonpentachlorid | ||
|
Andere Kationen
|
Phosphorpentafluorid Arsenpentafluorid Bismuth Penta |
||
|
Verwandte Verbindungen
|
Antimontrifluorid | ||
|
Sofern nicht anders angegeben, werden Daten für Materialien in ihrem Standardzustand (bei 25 ° C, 100 kPa) angegeben. |
|||
|
|
|||
| Infobox-Referenzen | |||
Antimonpentafluorid ist die anorganische Verbindung mit der Formel Sb F 5 . Diese farblose, viskose Flüssigkeit ist eine wertvolle Lewis-Säure und ein Bestandteil der Supersäure Fluorantimonsäure , die beim Mischen von flüssigem HF mit flüssigem SbF 5 im Verhältnis 2: 1 entsteht. Es zeichnet sich durch seine Lewis-Acidität und seine Fähigkeit aus, mit fast allen bekannten Verbindungen zu reagieren.
Vorbereitung
Antimonpentafluorid wird durch Reaktion von Antimonpentachlorid mit wasserfreiem Fluorwasserstoff hergestellt :
- SbCl 5 + 5 HF → SbF 5 + 5 HCl
Es kann auch aus Antimontrifluorid und Fluor hergestellt werden.
Struktur und chemische Reaktionen
In der Gasphase nimmt SbF 5 eine trigonale bipyramidale Struktur mit D 3h- Punktgruppensymmetrie an (siehe Bild). Das Material nimmt im flüssigen und festen Zustand eine kompliziertere Struktur an. Die Flüssigkeit enthält Polymere, wobei jedes Sb oktaedrisch ist, wobei die Struktur mit der Formel [SbF 4 (μ-F) 2 ] n beschrieben wird ((μ-F) bezeichnet die Tatsache, dass Fluoridzentren zwei Sb-Zentren überbrücken ). Das kristalline Material ist ein Tetramer, was bedeutet, dass es die Formel [SbF 4 (μ-F)] 4 hat . Die Sb-F-Bindungen betragen 2,02 Å innerhalb des achtgliedrigen Sb 4 F 4 -Rings; Die verbleibenden Fluoridliganden, die von den vier Sb-Zentren ausgehen, sind mit 1,82 Å kürzer. Die verwandten Spezies PF 5 und AsF 5 sind im festen und flüssigen Zustand monomer , wahrscheinlich aufgrund der kleineren Größe des Zentralatoms, was ihre Koordinationszahl begrenzt. BiF 5 ist ein Polymer.
Ebenso wie SbF 5 die Brønsted-Acidität von HF erhöht, erhöht es die Oxidationskraft von F 2 . Dieser Effekt wird durch die Oxidation von Sauerstoff veranschaulicht :
- 2 SbF 5 + F 2 + 2 O 2 → 2 [O 2 ] + [SbF 6 ] -
Antimonpentafluorid wurde auch in der ersten entdeckten chemischen Reaktion verwendet, bei der aus Fluoridverbindungen Fluorgas erzeugt wird:
- 4 SbF
5 + 2 K.
2 MnF
6 → 4 KSbF
6 + 2 MnF
3 + F.
2
Die treibende Kraft für diese Reaktion ist die hohe Affinität von SbF 5 zu F. - -
Dies ist dieselbe Eigenschaft, die die Verwendung von SbF 5 zur Erzeugung von Supersäuren empfiehlt .
Hexafluorantimonat
SbF 5 ist eine starke Lewis - Säure, so außergewöhnlich zu Quellen von F - der sehr stabilen Anion [SbF geben 6 ] - , Hexafluoroantimonat genannt. [SbF 6 ] - ist ein schwach koordinierendes Anion ähnlich PF 6 - . Obwohl es nur schwach basisch ist, reagiert [SbF 6 ] - mit zusätzlichem SbF 5 zu einem zentrosymmetrischen Addukt :
- SbF 5 + [SbF 6 ] - → [Sb 2 F 11 ] -
Sicherheit
SbF 5 reagiert heftig mit vielen Verbindungen und setzt häufig gefährlichen Fluorwasserstoff frei . Es ist ätzend für Haut und Augen.