Antimontrichlorid - Antimony trichloride

|
|||
|
|
|||
| Namen | |||
|---|---|---|---|
|
Bevorzugter IUPAC-Name
Antimontrichlorid |
|||
|
Systematischer IUPAC-Name
Trichlorstiban |
|||
| Andere Namen
Antimon(III)-chlorid, Antimonbutter, Antimonchlorid, Stibuschlorid, Trichlorstibin
|
|||
| Bezeichner | |||
|
3D-Modell ( JSmol )
|
|||
| ChEBI | |||
| ChemSpider | |||
| ECHA-InfoCard |
100.030.031 |
||
| EG-Nummer | |||
| KEGG | |||
| Gittergewebe | Antimon+Trichlorid | ||
|
PubChem- CID
|
|||
| RTECS-Nummer | |||
| UNII | |||
| UN-Nummer | 1733 | ||
|
CompTox-Dashboard ( EPA )
|
|||
|
|||
|
|||
| Eigenschaften | |||
| Cl 3 Sb | |||
| Molmasse | 228,11 g·mol -1 | ||
| Aussehen | Farbloser Feststoff, sehr hygroskopisch | ||
| Geruch | Scharf, scharf | ||
| Dichte | 3,14 g/cm 3 (25 °C) 2,51 g/cm 3 (150 °C) |
||
| Schmelzpunkt | 73,4 °C (164,1 °F; 346,5 K) | ||
| Siedepunkt | 223,5 °C (443,3 °F; 496,6 K) | ||
| 601,1 g/100 ml (0 °C) 985,1 g/100 ml (25 °C) 1,357 kg/100 ml (40 °C) |
|||
| Löslichkeit | Löslich in Aceton , Ethanol , CH 2 Cl 2 , Phenyls , Ether , Dioxan , CS 2 , CCl 4 , CHCl 3 , Cyclohexan , Selen(IV) oxychlorid Unlöslich in Pyridin , Chinolin , organische Basen |
||
| Löslichkeit in Essigsäure | 143,9 g/100 g (0 °C) 205,8 g/100 g (10 °C) 440,5 g/100 g (25 °C) 693,7 g/100 g (45 °C) |
||
| Löslichkeit in Aceton | 537,6 g/100 g (18 °C) | ||
| Löslichkeit in Benzoylchlorid | 139,2 g/100 g (15 °C) 169,5 g/100 g (25 °C) 2,76 kg/100 g (70 °C) |
||
| Löslichkeit in Salzsäure | 20 °C: 8,954 g/g (4,63% Gew./Gew. ) 8,576 g/g (14,4% Gew./Gew. ) 7,898 g/g (36,7% Gew./Gew.) |
||
| Löslichkeit in p-Cymen | 69,5 g/100 g (-3,5 °C) 85,5 g/100 g (10 °C) 150 g/100 g (30 °C) 2,17 kg/100 g (70 °C) |
||
| Dampfdruck | 13,33 Pa (18,1 °C) 0,15 kPa (50 °C) 2,6 kPa (100 °C) |
||
| -86,7·10 -6 cm 3 /mol | |||
|
Brechungsindex ( n D )
|
1.46 | ||
| Struktur | |||
| Orthorhombisch | |||
| 3,93 D (20 °C) | |||
| Thermochemie | |||
|
Wärmekapazität ( C )
|
183,3 J/mol·K | ||
|
Std molare
Entropie ( S |
110,5 J/mol·K | ||
|
Std
Bildungsenthalpie (Δ f H ⦵ 298 ) |
-381,2 kJ/mol | ||
|
Gibbs freie Energie (Δ f G ˚)
|
-322,5 kJ/mol | ||
| Gefahren | |||
| Sicherheitsdatenblatt | ICSC 1224 | ||
| GHS-Piktogramme |
 
|
||
| GHS-Signalwort | Achtung | ||
| H314 , H411 | |||
| P273 , P280 , P305+351+338 , P310 | |||
| NFPA 704 (Feuerdiamant) | |||
| Flammpunkt | Nicht brennbar | ||
| Letale Dosis oder Konzentration (LD, LC): | |||
|
LD 50 ( mediane Dosis )
|
525 mg/kg (oral, Ratte) | ||
| NIOSH (US-Grenzwerte für die Gesundheitsbelastung): | |||
|
PEL (zulässig)
|
TWA 0,5 mg/m 3 (als Sb) | ||
|
REL (empfohlen)
|
TWA 0,5 mg/m 3 (als Sb) | ||
| Verwandte Verbindungen | |||
|
Andere Anionen
|
Antimontrifluorid Antimontribromid Antimontriiodid |
||
|
Andere Kationen
|
Stickstofftrichlorid Phosphortrichlorid Arsentrichlorid Bismutchlorid |
||
|
Sofern nicht anders angegeben, beziehen sich die Daten auf Materialien im Standardzustand (bei 25 °C [77 °F], 100 kPa). |
|||
|
|
|||
| Infobox-Referenzen | |||
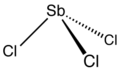
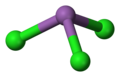
Antimontrichlorid ist die chemische Verbindung mit der Formel SbCl 3 . Es ist ein weicher, farbloser Feststoff mit einem stechenden Geruch und war den Alchemisten als Antimonbutter bekannt .
Vorbereitung
Antimontrichlorid wird durch Reaktion von Chlor mit Antimon , Antimontribromid , Antimontrioxid oder Antimontrisulfid hergestellt . Es kann auch durch Behandlung von Antimontrioxid mit konzentrierter Salzsäure hergestellt werden .
Reaktionen
SbCl 3 wird leicht hydrolysiert und Proben von SbCl 3 müssen vor Feuchtigkeit geschützt werden. Mit einer begrenzten Menge Wasser bildet es Antimonoxychlorid , das Chlorwasserstoff freisetzt :
- SbCl 3 + H 2 O → SbOCl + 2 HCl
Mit mehr Wasser bildet es Sb
4Ö
5Cl
2die sich beim Erhitzen auf 460° unter Argon in Sb . umwandelt
8Ö
11Cl
12.
SbCl 3 bildet leicht Komplexe mit Halogeniden, aber die Stöchiometrien sind keine gute Führung zu der Zusammensetzung, beispielsweise die (C
5H
5NH)SbCl
4enthält ein Kettenanion mit verzerrten Sb III -Oktaedern. Ebenso das Salz (C
4H
9NH
3)
2SbCl
5enthält ein polymeres Anion der Zusammensetzung [SbCl2−
5]
neinmit verzerrt oktaedrischem Sb III .
Mit Stickstoffdonorliganden, L, werden Komplexe mit einem stereochemisch aktiven freien Elektronenpaar gebildet, z. B. tri-trigonal-bipyramidales LSbCl 3 und octa -oktaedrisches L
2SbCl
3.
SbCl 3 ist nur eine schwache Lewis-Base, jedoch sind einige Komplexe bekannt, zum Beispiel die Carbonylkomplexe , Fe(CO)
3(SbCl
3)
2und Ni(CO)
3SbCl
3.
Struktur
In der Gasphase ist SbCl 3 pyramidal mit einem Cl-Sb-Cl-Winkel von 97,2° und einer Bindungslänge von 233 pm. In SbCl 3 hat jedes Sb drei Cl-Atome bei 234 pm, was die Persistenz der molekularen SbCl 3 -Einheit zeigt, jedoch gibt es weitere fünf benachbarte Cl-Atome, zwei bei 346 pm, eines bei 361 pm und zwei bei 374 pm. Diese acht Atome können als ein zweiseitiges trigonales Prisma betrachtet werden. Diese Abstände können mit BiCl 3 verglichen werden, das drei nahe Nachbarn bei 250 pm hat, mit zwei bei 324 pm und drei bei einem Mittelwert von 336 pm. Hier ist zu beachten, dass alle acht engen Nachbarn von Bi näher sind als die acht nächsten Nachbarn von Sb, was die Tendenz von Bi zeigt, höhere Koordinationszahlen anzunehmen.
Verwendet
SbCl 3 ist ein Reagenz zum Nachweis von Vitamin A und verwandten Carotinoiden im Carr-Price-Test . Das Antimontrichlorid reagiert mit dem Carotinoid zu einem blauen Komplex , der kolorimetrisch gemessen werden kann .
Antimontrichlorid wurde auch als Verfälschungsmittel verwendet , um die Louche-Wirkung in Absinth zu verstärken . Es wurde in der Vergangenheit verwendet, um Hornstummel von Kälbern aufzulösen und zu entfernen, ohne sie abschneiden zu müssen.
Es wird auch als Katalysator für Polymerisations-, Hydrocrack- und Chlorierungsreaktionen verwendet; als Beize ; und bei der Herstellung anderer Antimonsalze. Seine Lösung wird als analytisches Reagenz für Chloral, Aromaten und Vitamin A verwendet . Es hat eine sehr potenzielle Verwendung als Lewis-Säure-Katalysator in der synthetischen organischen Umwandlung.
Eine Lösung von Antimontrichlorid in flüssigem Schwefelwasserstoff ist ein guter Leiter, obwohl deren Anwendung durch die sehr niedrige Temperatur oder den hohen Druck begrenzt ist, die erforderlich sind, damit Schwefelwasserstoff flüssig ist.
Referenzen in der Populärkultur
In Episode 12 der dritten Staffel der beliebten britischen Sendung All Creatures Great and Small (adaptiert aus Kapitel sechs des Buches All Things Wise and Wonderful ) starben mehrere Kälber nach einer Episode von unspezifischer Gastroenteritis , deren Ursache später festgestellt wurde Einnahme von Antimontrichlorid sein, das in einer Lösung vorhanden ist, die zum Auflösen ihrer Hornstummel verwendet wird.