Arsensäure - Arsenous acid
|
|
|
|
| Namen | |
|---|---|
|
IUPAC-Name
brennende Säure
|
|
| Andere Namen
Arsenige Säure
Arsenoxid |
|
| Bezeichner | |
|
3D-Modell ( JSmol )
|
|
| ChEBI | |
| ChemSpider | |
| Arzneimittelbank | |
|
PubChem- CID
|
|
| UNII | |
|
CompTox-Dashboard ( EPA )
|
|
|
|
|
|
| Eigenschaften | |
| H 3 AsO 3 | |
| Molmasse | 125,94 g/mol |
| Aussehen | Nur in wässrigen Lösungen vorhanden |
| Base konjugieren | Arsenit |
| -51,2·10 -6 cm 3 /mol | |
| Gefahren | |
| Hauptgefahren | Giftig, ätzend |
| NIOSH (US-Grenzwerte für die Gesundheitsbelastung): | |
|
PEL (zulässig)
|
[1910.1018] TWA 0,010 mg/m 3 |
|
REL (empfohlen)
|
Ca C 0,002 mg/m 3 [15 Minuten] |
|
IDLH (unmittelbare Gefahr)
|
Ca [5 mg/m 3 (als As)] |
| Verwandte Verbindungen | |
|
Verwandte Verbindungen
|
Arsensäure |
|
Sofern nicht anders angegeben, beziehen sich die Daten auf Materialien im Standardzustand (bei 25 °C [77 °F], 100 kPa). |
|
|
|
|
| Infobox-Referenzen | |
Arsenige Säure (oder arsenige Säure ) ist die anorganische Verbindung mit der Formel H 3 AsO 3 . Es ist bekannt, dass es in wässrigen Lösungen vorkommt , aber es wurde nicht als reines Material isoliert, obwohl diese Tatsache die Bedeutung von As(OH) 3 nicht schmälert .
Eigenschaften
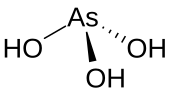
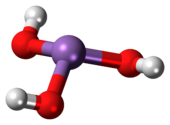
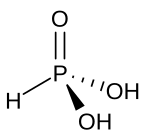
As(OH) 3 ist ein pyramidenförmiges Molekül, das aus drei an Arsen gebundenen Hydroxylgruppen besteht . Das 1 H- NMR- Spektrum von arsenigen Säurelösungen besteht aus einem einzigen Signal, das mit der hohen Symmetrie des Moleküls übereinstimmt. Im Gegensatz dazu nimmt die nominell verwandte phosphorige Säure H 3 PO 3 die Struktur HPO(OH) 2 an . Das strukturelle Analogon der arsenigen Säure (P(OH) 3 ) ist eine sehr untergeordnete Gleichgewichtskomponente solcher Lösungen. Das unterschiedliche Verhalten der As- und P-Verbindungen spiegelt einen Trend wider, dass hohe Oxidationsstufen für leichtere Mitglieder der Hauptgruppenelemente stabiler sind als ihre schwereren Artgenossen.
Ein Tautomer der arsenigen Säure ist HAsO(OH) 2 , die als Arsonsäure bezeichnet wird . Es wurde weder isoliert noch gut charakterisiert.
Synthese
Die Herstellung von As(OH) 3 beinhaltet eine langsame Hydrolyse von Arsentrioxid in Wasser. Durch Zugabe von Base wird arsenige Säure in die Arsenit-Ionen [AsO(OH) 2 ] − , [AsO 2 (OH)] 2− und [AsO 3 ] 3− umgewandelt .
Reaktionen
Mit einem ersten p K a von 9,2 ist As(OH) 3 eine schwache Säure. Reaktionen, die wässrigem Arsentrioxid zugeschrieben werden, sind auf arsenige Säure und ihre konjugierten Basen zurückzuführen.
Wie Arsentrioxid ist Arsensäure manchmal amphoter . Zum Beispiel reagiert es mit Salz-, Bromwasserstoff- und Iodwasserstoffsäure, um Arsentrichlorid, Tribromid und Triiodid herzustellen.
- As(OH) 3 + 3 HCl ⇌ AsCl 3 + 3 H 2 O
- As(OH) 3 + 3 HBr ⇌ AsBr 3 + 3 H 2 O
- As(OH) 3 + 3 HI ⇌ AsI 3 + 3 H 2 O
Reaktion von arsenige Säure mit Methyljodid ergibt Methylarson- . Diese historisch bedeutsame Umwandlung ist die Meyer-Reaktion :
- As(OH) 3 + CH 3 I + NaOH CH 3 AsO(OH) 2 + NaI + H 2 O
Bei Arsen findet eine Alkylierung statt, und die Oxidationsstufe von Arsen steigt von +3 auf +5 an.
Toxikologie
Arsenhaltige Verbindungen sind hochgiftig und krebserregend . Die Anhydridform der arsenigen Säure, Arsentrioxid , wird als Herbizid , Pestizid und Rodentizid verwendet .
