Mycobacterium bovis -Mycobacterium bovis
| Mycobacterium bovis | |
|---|---|
|
|
| Abgeschwächter Stamm von M. bovis, der im Bacillus Calmette-Guérin- Impfstoff verwendet wird | |
| Wissenschaftliche Klassifikation | |
| Domain: | |
| Stamm: |
" Aktinobakterien "
|
| Klasse: | |
| Befehl: | |
| Familie: | |
| Gattung: | |
| Spezies: |
M. bovis
|
| Binomialer Name | |
|
Mycobacterium bovis Karlson & Lessel 1970, ATCC 19210
|
|
Mycobacterium bovis ( M. bovis ) ist ein langsam wachsendes ( Generationszeit von 16 bis 20 Stunden) aerobes Bakterium und der Erreger der Tuberkulose bei Rindern (bekannt als Rinder-TB ). Es ist mit Mycobacterium tuberculosis verwandt , dem Bakterium, das beim Menschen Tuberkulose verursacht. M. bovis kann die Speziesbarriere überwinden und bei Menschen und anderen Säugetieren eine tuberkuloseähnliche Infektion verursachen.
Bakterienmorphologie und Färbung
Die Bakterien sind gebogene oder gerade Stäbchen. Sie bilden manchmal Filamente, die einmal gestört in Bazillen oder Kokken zerfallen. In Geweben bilden sie schlanke Stäbchen, gerade oder gebogen oder keulenförmig. Kurze, relativ pralle Bazillen (Stäbchen) in Gewebeausstrichen, große schlanke Perlenstäbchen in Kultur. Sie haben keine Flagellen oder Fimbrien , keine Kapsel .
Bakterien der Gruppe Mycobacterium tuberculosis sind in Geweben 1,0 - 4,0 µm lang und 0,2 - 0,3 µm breit. In Kultur können sie als Kokken oder als Bazillen mit einer Länge von bis zu 6 - 8 µm auftreten.
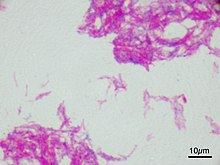
Die Bakterien färben Gram-positiv , säurefest . Die Zellwand enthält bis zu 60 % Lipid, was den Mykobakterien ihre hydrophoben Eigenschaften, ihr langsames Wachstum und ihre Beständigkeit gegen Austrocknung, Desinfektionsmittel, Säuren und Antikörper verleiht. ( Mycobacterium- Familie). Sie sind nicht leicht mit Analinfarbstoffen zu färben; Obwohl sie Gram-positiv sind, ist es möglicherweise nicht einfach, dies zu bestätigen. Ziehl-Neelsen-Färbung führt zu einer rosa Färbung mit heißem Carbolfuscin und widersteht dann einer Entfärbung mit 3 % Salzsäure in 95 % Alkohol (dh sie sind säure-alkoholecht); nach dem Waschen wird der Objektträger zB mit Methylenblau gegengefärbt.
Sie sind nicht sporenbildend .
Kultur und biochemische Merkmale
Wachstumsanforderungen
Mycobacterium bovis ist ein fakultativ intrazellulärer Parasit . Für das In-vitro- Wachstum sind spezielle Kulturmedien erforderlich, beispielsweise enthält das Eimedium von Dorset Eigelb, Phosphatpuffer, Magnesiumsalze und Natriumpyruvat; Aminosäuren können hinzugefügt werden, aber Glycerin ist nicht enthalten, da es hemmend wirkt. Es wird durch Glycerin gehemmt. Die Kultur benötigt im Allgemeinen mehrere Wochen bei 37 °C, um Kolonien zu erreichen, die mit dem bloßen menschlichen Auge sichtbar sind. Streng aerob. Wächst bei 37 °C, wächst nicht bei 25 °C. Optimales Wachstum bei 37-38 °C. Reduziert Nitrat nicht, reduziert Niacin nicht. Beständig gegen Pyrazinamid. Empfindlich gegen Thiophen-2-carbonsäurehydrazid.
Aussehen der Kolonien
Anfangs (nach 3–4 Wochen) winzige matte Flocken, die sich zu trockenen, unregelmäßigen Massen verdicken, die hoch über der Nährbodenoberfläche stehen. Schließlich konfluierendes Wachstum über die gesamte Kulturoberfläche, wobei eine raue wachsartige Decke gebildet wird, die dick und faltig wird und die Seiten des Behälters hinaufreicht. Gelb, wenn sie zum ersten Mal sichtbar sind, verdunkeln sich zu tiefem Gelb und schließlich ziegelrot, wenn sie Licht ausgesetzt werden. In flüssigen Medien Wachstum nur auf der Oberfläche, es sei denn, dem Medium wird ein Netzmittel (zB Tween 80) zugesetzt.
Zellstruktur und Stoffwechsel
M. bovis ist in Struktur und Stoffwechsel dem M. tuberculosis ähnlich . M. bovis ist ein grampositives, säurefestes, stäbchenförmiges, aerobes Bakterium. Im Gegensatz zu M. tuberculosis , bovis M. fehlt Pyruvat - Kinase - Aktivität aufgrund pykA- eine Punktmutation enthält , die aus Mg Affekt Bindung 2+ Cofaktor. Pyruvatkinase katalysiert den letzten Schritt der Glykolyse, die Dephosphorylierung von Phosphorenolpyruvat zu Pyruvat. Daher sind bei M. bovis glykolytische Zwischenprodukte nicht in der Lage, in den oxidativen Metabolismus einzutreten. Obwohl keine spezifischen Studien durchgeführt wurden, scheint es, dass M. bovis auf Aminosäuren oder Fettsäuren als alternative Kohlenstoffquelle für den Energiestoffwechsel angewiesen ist.
Pathogenese

In der ersten Hälfte des 20. Jahrhunderts soll M. bovis für mehr Verluste bei Nutztieren verantwortlich gewesen sein als alle anderen Infektionskrankheiten zusammen. Eine Infektion tritt auf, wenn das Bakterium aufgenommen oder eingeatmet wird.
M. bovis wird in der Regel durch den Verzehr von Rohmilch infizierter Kühe auf den Menschen übertragen, kann sich aber auch über Aerosoltröpfchen verbreiten. Tatsächliche Infektionen beim Menschen sind heutzutage in Industrieländern selten, hauptsächlich weil die Pasteurisierung M. bovis- Bakterien in infizierter Milch abtötet . Im Vereinigten Königreich werden Rinder im Rahmen eines Tilgungsprogramms auf die Krankheit getestet und bei positivem Test getötet. Solche Rinder können immer noch in die menschliche Nahrungskette gelangen, jedoch erst, nachdem ein Fleischinspektor oder ein staatlicher Tierarzt den Kadaver inspiziert und bestätigt hat, dass er für den menschlichen Verzehr geeignet ist. In Gebieten der Entwicklungsländer, in denen die Pasteurisierung nicht routinemäßig erfolgt, ist M. bovis jedoch eine relativ häufige Ursache für Tuberkulose beim Menschen.
Rindertuberkulose ist eine chronische Infektionskrankheit, die ein breites Spektrum von Säugetierwirten befällt, darunter Menschen, Rinder , Hirsche , Lamas , Schweine , Hauskatzen , wilde Fleischfresser ( Füchse , Kojoten ) und Allesfresser ( Gross-Opossum , Musteliden und Nagetiere ); es betrifft selten Equiden oder Schafe . Die Krankheit kann auf verschiedene Weise übertragen werden; Beispielsweise kann es in Ausatemluft, Sputum, Urin, Kot und Eiter übertragen werden, sodass die Krankheit je nach Art durch direkten Kontakt, Kontakt mit den Ausscheidungen eines infizierten Tieres oder Inhalation von Aerosolen übertragen werden kann.
Anwendung in der Biotechnologie
M. bovis ist der Vorfahre des am häufigsten verwendeten Impfstoffs gegen Tuberkulose, M. bovis- Bazillus Calmette-Guérin. Der BCG- Stamm wurde nach 239-maliger Subkultivierung auf Glycerin-Kartoffel-Medium während 13 Jahren isoliert, ausgehend von einem anfänglich virulenten Stamm.
Epidemiologie und Kontrolle
Neuseeland
In Neuseeland ist das eingeschleppte Buschschwanz-Opossum ein Vektor für die Verbreitung von M. bovis . Der Biosecurity Act von 1993 , der eine nationale Schädlingsbekämpfungsstrategie festlegte, ist die Gesetzgebung zur Bekämpfung der Krankheit in Neuseeland. Das Animal Health Board betreibt ein landesweites Programm für Rindertests und Opossum-Kontrolle mit dem Ziel, M. bovis von wilden Vektorarten auf 2,5 Millionen Hektar – oder einem Viertel – der neuseeländischen Risikogebiete bis 2026 und schließlich . auszurotten , die Krankheit vollständig auszurotten.
Das TB-freie Neuseeland-Programm gilt als "weltweit führend". Es hat erfolgreich die Infektionsraten von Rinder- und Hirschherden von mehr als 1700 im Jahr 1994 auf weniger als 100 Herden im Juli 2011 reduziert. Ein Großteil dieses Erfolgs kann auf die anhaltenden Rinderkontrollen zurückgeführt werden, die Kreuzinfektionen reduzieren und den Krankheitszyklus durchbrechen. In Hohotaka, auf der zentralen Nordinsel Neuseelands , wurde beispielsweise durch Kontrollarbeiten von 1988 bis 1994 eine anhaltende durchschnittliche Verringerung der Dichte von TB‐infizierten Opossums um 87,5% erreicht. Die jährliche Tuberkulose-Inzidenz in lokalen Rinderherden ging daher erwartungsgemäß um einen ähnlichen Betrag zurück (83,4%).
Opossums werden durch eine Kombination aus Fangen , Bodenködern und, wo andere Methoden unpraktisch sind, Luftbehandlung mit 1080-Gift bekämpft .
Von 1979 bis 1984 wurde die Opossum-Kontrolle aus Geldmangel eingestellt. Von diesem Zeitpunkt an bis 1994 stiegen die TB-Raten in den Herden stetig an. Das Gebiet Neuseelands, in dem TB-infizierte Wildtiere leben, vergrößerte sich von etwa 10 % des Landes auf 40 %.
Dass Opossums solch wirksame Überträger von TB sind, scheint durch ihr Verhalten erleichtert zu werden, sobald sie die Krankheit bekommen.
Vereinigtes Königreich
In den 1930er Jahren waren 40 % der Rinder im Vereinigten Königreich mit M. bovis infiziert, und jedes Jahr wurden 50.000 neue Fälle von M. bovis- Infektionen beim Menschen gemeldet. Laut DEFRA und der Health Protection Agency wäre das Risiko für Menschen, sich von Rindern an Tuberkulose zu erkranken, in Großbritannien gering.
Dachse ( Meles meles ) wurden erstmals 1971 als Träger von M. bovis identifiziert , aber der Bericht eines unabhängigen Überprüfungsausschusses aus dem Jahr 1997 (der Krebs-Bericht) kam zu dem Schluss: "starke Indizien [existieren], die darauf hindeuten, dass Dachse eine bedeutende Quelle von M. bovis- Infektion bei Rindern... [j]edoch ist der kausale Zusammenhang... nicht bewiesen". Im Wesentlichen war der Beitrag von Dachsen „zum TB-Problem bei britischen Rindern“ zu diesem Zeitpunkt eine Hypothese, die dem Bericht zufolge getestet werden musste. Der anschließende Randomized Badger Culling Trial (entworfen, beaufsichtigt und analysiert von der Independent Scientific Group on Cattle TB, oder ISG ) untersuchte diese Hypothese, indem ein groß angelegter Feldversuch mit groß angelegtem (proaktivem) Keulen und lokalisiertem reaktivem Keulen durchgeführt wurde (im Vergleich zu Gebieten, die kein Dachskeulen). In ihrem Abschlussbericht kam die ISG zu dem Schluss: „Erstens, obwohl Dachse eindeutig eine Quelle von Rinder-TB sind, zeigt eine sorgfältige Auswertung unserer eigenen und anderer Daten, dass die Keulung von Dachsen keinen sinnvollen Beitrag zur Bekämpfung der Rinder-TB in Großbritannien leisten kann Die in Betracht gezogenen Maßnahmen werden die Situation wahrscheinlich eher verschlimmern als verbessern.Zweitens bedeuten Schwächen bei den Testverfahren für Rinder, dass die Rinder selbst in allen Gebieten, in denen TB auftritt, erheblich zur Persistenz und Ausbreitung von Krankheiten beitragen, und in einigen Teilen Großbritanniens wahrscheinlich auch die Hauptinfektionsquelle sein. Wissenschaftliche Erkenntnisse deuten darauf hin, dass allein durch die strikte Anwendung von Kontrollmaßnahmen auf Rinderbasis die steigende Inzidenz von Krankheiten rückgängig gemacht und die geografische Ausbreitung eingedämmt werden kann.“ Am 26. Juli 2007 sagte der Staatsminister des Ministeriums für Umwelt, Ernährung und ländliche Angelegenheiten (Lord Rooker): „Meine Herren, wir begrüßen den Abschlussbericht der Unabhängigen Wissenschaftlichen Gruppe, der die Evidenzbasis weiter verbessert die der Bericht aufwirft, und wird weiterhin mit der Industrie, Regierungsberatern und wissenschaftlichen Experten zusammenarbeiten, um politische Entscheidungen zu diesen Themen zu treffen."
Im Vereinigten Königreich wurde festgestellt, dass viele andere Säugetiere mit M. bovis infiziert sind , obwohl die Häufigkeit der Isolierung im Allgemeinen viel geringer ist als bei Rindern und Dachsen. In einigen Gebieten Südwestenglands wurden Hirsche , insbesondere Damhirsche aufgrund ihres geselligen Verhaltens, als mögliche Erhaltungswirte für die Übertragung von Rinder-TB in Betracht gezogen
In einigen lokalisierten Gebieten wird argumentiert, dass das Risiko einer Übertragung auf Rinder durch Damwild höher ist als durch Dachse.
Einer der Gründe, warum das Ministerium für Umwelt, Ernährung und ländliche Angelegenheiten die Tötung infizierter oder verdächtiger Rinder fordert, ist die Einhaltung der EU-Vorschriften für den Export von Fleisch und Milchprodukten in andere Mitgliedstaaten. Fleisch und Milchprodukte können im Vereinigten Königreich weiterhin in die menschliche Nahrungskette verkauft werden, sofern die entsprechenden Schlachtkörperkontrollen und die Milchpasteurisierung durchgeführt wurden.
Die Ausbreitung der Krankheit auf den Menschen durch Haustiere wurde im März 2014 deutlich, als Public Health England bekannt gab, dass zwei Menschen in England nach Kontakt mit einer Hauskatze bTB-Infektionen entwickelten. Die beiden Fälle beim Menschen wurden im Jahr 2013 mit 9 Fällen einer bTB-Infektion bei Katzen in Berkshire und Hampshire in Verbindung gebracht. Dies sind die ersten dokumentierten Fälle einer Übertragung von Katze zu Mensch.
In einem Meinungsartikel aus dem Jahr 2010 in Trends in Microbiology argumentierten Paul und David Torgerson, dass Rindertuberkulose im Vereinigten Königreich ein zu vernachlässigendes Problem für die öffentliche Gesundheit sei, vorausgesetzt, Milch sei pasteurisiert. Rinder-TB wird sehr selten durch Aerosole vom Rind auf den Menschen übertragen. Daher ist das Programm zur Bekämpfung der Rindertuberkulose im Vereinigten Königreich in seiner gegenwärtigen Form eine Fehlallokation von Ressourcen und bietet der Gesellschaft keinen Nutzen. Tatsächlich gibt es nur sehr wenige Beweise für einen positiven Kostenvorteil für die Viehwirtschaft, da nur wenige Studien zu den direkten Kosten der Rinder-TB für die Tierproduktion durchgeführt wurden. Die Pasteurisierung von Milch war die einzige Intervention des öffentlichen Gesundheitswesens, die die Übertragung von Rinder-TB auf den Menschen verhinderte, und es wird keine Rechtfertigung für die gegenwärtige Test- und Keulungspolitik im Vereinigten Königreich gesehen.
Im Juli 2010 wurde die zweite Ausgabe des Diskussionsdokuments Bovine TB, Time for a Rethink von Rethink Bovine TB, einer unabhängigen Forschungsgruppe, veröffentlicht. Das Papier befasst sich mit der aktuellen Politik in England und Wales. Es schlägt eine alternative Lösung vor, die sowohl praktisch als auch kostengünstig ist. In dem Papier werden Beweise aus DEFRA und den Arbeiten der Professoren Paul und David Torgerson gezogen.
Im März 2012 veröffentlichte die Denkfabrik Bow Group ein Zielpapier, in dem die Regierung aufgefordert wurde, ihre Pläne zur Tötung von Tausenden von Dachsen zur Kontrolle der Rinder-TB zu überdenken, und erklärte, dass die Ergebnisse der großen Dachs-Keulungsversuche von Labour einige Jahre zuvor nicht funktionieren . Das Papier wurde von Graham Godwin-Pearson mit einem Vorwort des Sängers Brian May und Beiträgen führender Tuberkulose-Wissenschaftler, darunter Lord Krebs, verfasst .
Im Jahr 2017 veröffentlichten Rachel Tanner und Helen McShane vom Jenner Institute, Oxford, Forschungsergebnisse zum Ersatz, zur Reduzierung und zur Verbesserung des Einsatzes von Tieren in der Tuberkulose-Impfstoffforschung.
Vereinigte Staaten

Laut Barbara Gutmann Rosenkrantz führte die Entdeckung der Beziehung zwischen Rinder- und Humantuberkulose im späten 19. Die Kampagnen für saubere Milch und Fleisch erschreckten die Stadtbewohner, Kontrollen zu unterstützen, obwohl es zu dieser Zeit kaum Beweise dafür gab, dass Tuberkulose durch infiziertes Fleisch oder Milch auf den Menschen übertragen wurde. Die Kampagnen gegen unreines Fleisch und unreine Milch führten zu Spannungen zwischen den sich entwickelnden Tierärzten und den Ärzten, die diesen Bereich jeweils als Teil ihrer eigenen Expertise beanspruchen.
Bis 1917 waren 5 Prozent der amerikanischen Rinder mit Mycobacterium bovis (Rindertuberkulose oder BTB) infiziert , darunter 10 Prozent der Milchtiere und 1-2 Prozent der Weiderinder. Die Preise stiegen. Um 1900 starben jedes Jahr 15.000 Amerikaner, meist Kinder, an BTB und viele weitere erlitten Schmerzen und Entstellungen.
Bedroht durch einen von städtischen Gesundheitsbehörden angeordneten Verkaufsstopp, starteten die Regierungsbeamten des Staates Vermont von 1877 bis 1936 eine innovative Ausrottungskampagne gegen die Rindertuberkulose auf Farmen. Sie nutzten die neuesten deutschen Forschungsergebnisse und hielten damit die Märkte New York City und Boston aufrecht . Vermont war außergewöhnlich, denn im ganzen Land wehrten sich viele Landwirte energisch gegen die Ausrottung der Rindertuberkulose als teure Verletzung ihres libertären Rechts auf Landwirtschaft.
In den letzten Jahrzehnten sind M. bovis- Infektionen in Rinderherden in den Vereinigten Staaten nicht üblich. M. bovis ist endemisch bei Weißwedelhirschen ( Odocoileus virginianus ) im nordöstlichen Teil von Michigan und im Norden von Minnesota und wird sporadisch aus Mexiko importiert. Nur der Weißwedelhirsch wurde als Erhaltungswirt beim Ausbruch der Rindertuberkulose in Michigan bestätigt, obwohl andere Säugetiere wie Waschbären ( Procyon lotor ), Opossums ( Didelphis virginiana ) und Kojoten ( Canis latrans ) als Überlauf dienen können und Sackgassen-Hosts. Die Tatsache, dass Weißwedelhirsche ein Erhaltungswirt für M. bovis sind, bleibt ein bedeutendes Hindernis für die landesweite Ausrottung der Krankheit bei Nutztieren in den USA. Im Jahr 2008 erlegten 733.998 lizenzierte Hirschjäger rund 489.922 Weißwedelhirsche, um die Ausbreitung der Krankheit zu kontrollieren. Diese Jäger kauften mehr als 1,5 Millionen Hirsch-Erntemarken. Der wirtschaftliche Wert der Hirschjagd für die Wirtschaft Michigans im Bestreben, TB auszurotten, ist beträchtlich. Im Jahr 2006 gaben Jäger beispielsweise 507 Millionen US-Dollar für die Jagd auf Weißwedelhirsche in Michigan aus.
Global
Die Krankheit wird bei Rindern auf der ganzen Welt gefunden, aber einigen Ländern ist es gelungen, das Auftreten der Krankheit durch „Testen und Keulen“ des Viehbestands zu reduzieren oder zu begrenzen. Der größte Teil Europas und mehrere karibische Länder (einschließlich Kuba) sind praktisch frei von M. bovis . Australien ist seit dem erfolgreichen BTEC-Programm offiziell frei von der Krankheit, aber in isolierten Teilen des Northern Territory könnten bei wilden Wasserbüffeln Restinfektionen vorhanden sein. In Kanada sind im und um den Riding Mountain National Park in Manitoba betroffene Wildelche und Weißwedelhirsche zu finden. Um die Kontrolle zu verbessern und Rinder-TB zu eliminieren, hat die kanadische Lebensmittelaufsichtsbehörde Manitoba in zwei Verwaltungsgebiete aufgeteilt: Das TB-Ausrottungsgebiet Riding Mountain, in dem die Krankheit festgestellt wurde, und das Manitoba-TB-Ausrottungsgebiet, der Rest der Provinz außerhalb der RMEA, wo die Krankheit wurde nicht gefunden. Die Krankheit wurde auch bei afrikanischen Büffeln in Südafrika gefunden.
M. bovis kann von Mensch zu Mensch übertragen werden; ein Ausbruch ereignete sich in Birmingham , England , im Jahr 2004, und zwar von Mensch zu Rind, aber solche Vorkommnisse sind selten.
In Mexiko ist die Krankheit weit verbreitet und nimmt unter den Menschen zu.
Zoonotische Tuberkulose
Die Infektion des Menschen mit M. bovis wird als zoonotische Tuberkulose bezeichnet. 2017 veröffentlichten die Weltgesundheitsorganisation ( WHO ), die Weltorganisation für Tiergesundheit ( OIE ), die Ernährungs- und Landwirtschaftsorganisation ( FAO ) und die Internationale Union gegen Tuberkulose und Lungenkrankheiten (The Union) den ersten Fahrplan für Zoonotische Tuberkulose. Anerkennung der zoonotischen Tuberkulose als ein bedeutendes globales Gesundheitsproblem. Der Hauptübertragungsweg erfolgt durch den Verzehr von nicht pasteurisierter Milch oder anderen Milchprodukten, obwohl auch eine Übertragung durch Inhalation und durch den Verzehr von schlecht gekochtem Fleisch berichtet wurde. Im Jahr 2018 traten laut dem jüngsten Global Tuberculosis Report schätzungsweise 142.000 neue Fälle von zoonotischer Tuberkulose und 12.500 Todesfälle aufgrund der Krankheit auf. Fälle von zoonotischer Tuberkulose wurden aus Afrika, Amerika, Europa, dem östlichen Mittelmeerraum und dem westlichen Pazifik gemeldet. Fälle von zoonotischer Tuberkulose beim Menschen sind mit dem Vorkommen von Rindertuberkulose bei Rindern verbunden, und Regionen ohne angemessene Seuchenbekämpfungsmaßnahmen und/oder Seuchenüberwachung sind einem höheren Risiko ausgesetzt. Es ist schwierig, eine zoonotische Tuberkulose von einer durch Mycobacterium tuberculosis verursachten Tuberkulose beim Menschen klinisch zu unterscheiden , und die derzeit am häufigsten verwendete Diagnostik kann nicht effektiv zwischen M. bovis und M. tuberculosis unterscheiden , was zu einer Unterschätzung der Gesamtzahl der Fälle weltweit beiträgt. Die Bekämpfung dieser Krankheit erfordert die Zusammenarbeit der Sektoren Tiergesundheit, Lebensmittelsicherheit und menschliche Gesundheit im Rahmen eines One-Health- Ansatzes (multidisziplinäre Zusammenarbeit zur Verbesserung der Gesundheit von Tieren, Menschen und der Umwelt).
Im Fahrplan 2017 wurden zehn vorrangige Bereiche für die Bekämpfung der zoonotischen Tuberkulose genannt, darunter die Sammlung genauerer Daten, die Verbesserung der Diagnostik, das Schließen von Forschungslücken, die Verbesserung der Lebensmittelsicherheit, die Reduzierung von M. bovis in Tierpopulationen, die Identifizierung von Risikofaktoren für die Übertragung, die Sensibilisierung, die Entwicklung von Strategien, Durchführung von Interventionen und Erhöhung der Investitionen. Um sich an den Zielen des globalen Plans zur Beendigung der TB-Partnerschaft 2016-2020 auszurichten, skizziert die Roadmap spezifische Meilensteine und Ziele, die innerhalb dieses Zeitrahmens erreicht werden müssen.
Behandlung
M. bovis ist von Natur aus resistent gegen Pyrazinamid ; daher ist die Standardbehandlung beim Menschen Isoniazid und Rifampicin für 9 Monate. Die meisten positiv getesteten Rinder werden getötet.
Siehe auch
Verweise
Externe Links
- TB-freies Neuseeland - TB-Kontrollprogramm in Neuseeland
- Bovine TB-Informationen auf der Website des Department of Conservation - Die Verwendung von 1080 zur Schädlingsbekämpfung in Neuseeland - Opossums als Reservoir für Rindertuberkulose
- Informationen über bovine TB auf 1080: The Facts Website - Fakten darüber, wie 1080-Gift zur Bekämpfung von boviner TB in Neuseeland verwendet wird
- Hintergrund zur Immunologie und Testung auf Rindertuberkulose - Hintergrund zur Immunologie und Testung auf Rindertuberkulose.
- Mycobacterium bovis in afrikanischen Wildtieren Mycobacterium bovis in afrikanischen Wildtieren
