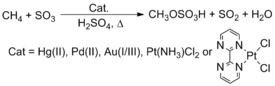Aktivierung von Kohlenstoff-Wasserstoff-Bindungen - Carbon–hydrogen bond activation
Die Kohlenstoff-Wasserstoff-Bindungsfunktionalisierung ( CH-Funktionalisierung ) ist eine Art von Reaktion, bei der eine Kohlenstoff-Wasserstoff-Bindung gespalten und durch eine Kohlenstoff-X-Bindung ersetzt wird (wobei X normalerweise Kohlenstoff, Sauerstoff oder Stickstoff ist). Der Begriff impliziert normalerweise, dass ein Übergangsmetall am CH-Spaltungsprozess beteiligt ist. Reaktionen, die durch den Begriff klassifiziert werden, beinhalten typischerweise, dass der Kohlenwasserstoff zuerst mit einem Metallkatalysator reagiert, um einen metallorganischen Komplex zu erzeugen, in dem der Kohlenwasserstoff entweder über einen intermediären "Alkan- oder Arenkomplex " oder als Übergang an die innere Sphäre eines Metalls koordiniert ist Zustand, der zu einem "M - C" -Zwischenprodukt führt. Das Zwischenprodukt dieses ersten Schritts (bekannt als CH -Aktivierung und manchmal austauschbar mit der CH-Funktionalisierung verwendet) kann dann nachfolgende Reaktionen eingehen, um das funktionalisierte Produkt herzustellen. Wichtig für diese Definition ist die Anforderung, dass die Kohlenwasserstoffspezies während des CH-Spaltungsereignisses in der inneren Sphäre und unter dem Einfluss von "M" assoziiert bleibt.
Als alternative Definition verwenden andere Autoren den Begriff CH-Funktionalisierung , um jede organische Umwandlung zu bezeichnen, bei der das Nettoergebnis die Umwandlung einer relativ inerten CH-Bindung in eine CH-Bindung (dh eine funktionelle Gruppe ) ist, unabhängig davon des Mechanismus (oder mit einer agnostischen Haltung dazu). Insbesondere erfordert diese Definition keine Übergangsmetallkoordination an den Kohlenwasserstoff im Reaktionsmechanismus. Diese breitere Definition schließt die oben angegebene engere Definition als Teilmenge ein. Diese Definition würde jedoch auch eine eisenkatalysierte Alkanfunktionalisierungsreaktion einschließen, die über den Sauerstoffrückprallmechanismus abläuft (z. B. Cytochrom P450- Enzyme und ihre synthetischen Analoga), an der vermutlich keine Metall-Kohlenstoff-Bindung beteiligt ist. Ebenso würde die auf Liganden basierende Reaktivität vieler Metallcarbenspezies mit Kohlenwasserstoffen unter diese Kategorie fallen, obwohl einige Fälle mechanistisch nicht eindeutig sind. Einige Autoren definieren die CH-Aktivierung in ähnlicher Weise allgemein als den CH-Spaltungsschritt eines Mechanismus, der zur Funktionalisierung einer Kohlenwasserstoffgruppe führt (oder als beobachtbare Folge einer CH-Bindungsspaltung wie dem H / D-Austausch). Wieder andere behalten die ursprüngliche enge Definition des Begriffs CH-Aktivierung bei, während sie die CH-Funktionalisierung im weiteren Sinne verwenden.
Einstufung
Mechanismen für CH-Aktivierungen können in drei allgemeine Kategorien eingeteilt werden:
- (i) oxidative Addition , bei der ein niedrigwertiges Metallzentrum in eine Kohlenstoff-Wasserstoff-Bindung einfügt, die die Bindung spaltet und das Metall oxidiert .
- L n M + RH → L n MR (H)
- (ii) Elektrophile Aktivierung, bei der ein elektrophiles Metall den Kohlenwasserstoff angreift und ein Proton verdrängt:
- L n M + + RH → L n MR + H +
Das Substrat unterliegt einem Mechanismus vom Typ S E Ar .
- (iii) Sigma-Bindungsmetathese , die einen "vierzentrierten" Übergangszustand durchläuft, in dem Bindungen in einem einzigen Schritt brechen und sich bilden:
- L n MR + R'H → L n MR '+ RH
Historischer Überblick
Die erste CH-Aktivierungsreaktion wird häufig Otto Dimroth zugeschrieben , der 1902 berichtete, dass Benzol mit Quecksilber (II) -acetat reagierte (siehe: Organomercury ). Viele elektrophile Metallzentren unterliegen dieser Friedel-Crafts-ähnlichen Reaktion. Joseph Chatt beobachtete die Addition von CH-Bindungen von Naphthalin durch Ru (0) -Komplexe.
Chelat-unterstützte CH-Aktivierungen sind weit verbreitet. Shunsuke Murahashi berichtete über eine Kobalt- katalysierte Chelat- unterstützte CH-Funktionalisierung von 2-Phenylisoindolin-1-on aus ( E ) -N, 1-Diphenylmethanimin.
1969 berichtete AE Shilov , dass Kaliumtetrachloroplatinat ein Isotopen-Scrambling zwischen Methan und schwerem Wasser induzierte . Es wurde vorgeschlagen, dass der Weg die Bindung von Methan an Pt (II) beinhaltet. 1972 konnte die Shilov-Gruppe in einer ähnlichen Reaktion Methanol und Methylchlorid herstellen, an der eine stöchiometrische Menge Kaliumtetrachloroplatinat , katalytisches Kaliumhexachloroplatinat , Methan und Wasser beteiligt waren. Aufgrund der Tatsache, dass Shilov während des Kalten Krieges in der Sowjetunion arbeitete und veröffentlichte , wurde seine Arbeit von westlichen Wissenschaftlern weitgehend ignoriert. Dieses sogenannte Shilov-System ist heute eines der wenigen echten katalytischen Systeme für Alkanfunktionalisierungen .
In einigen Fällen wurden Entdeckungen bei der CH-Aktivierung in Verbindung mit denen der Kreuzkopplung gemacht . 1969 berichtete Yuzo Fujiwara über die Synthese von ( E ) -1,2-Diphenylethen aus Benzol und Styrol mit Pd (OAc) 2 und Cu (OAc) 2 , ein Verfahren, das dem der Kreuzkupplung sehr ähnlich ist. In Bezug auf die Kategorie der oxidativen Addition berichtete MLH Green 1970 über die photochemische Insertion von Wolfram (als Cp 2 WH 2 -Komplex) in eine Benzol -CH-Bindung, und George M. Whitesides führte 1979 als erster ein intramolekulares Aliphat durch CH-Aktivierung
Der nächste Durchbruch wurde 1982 von zwei Forschungsgruppen unabhängig voneinander berichtet. RG Bergman berichtete über die erste übergangsmetallvermittelte intermolekulare CH-Aktivierung von nicht aktivierten und vollständig gesättigten Kohlenwasserstoffen durch oxidative Addition. Unter Verwendung eines photochemischen Ansatzes führte die Photolyse von Cp * Ir (PMe 3 ) H 2 , wobei Cp * ein Pentamethylcyclopentadienylligand ist , zu der koordinativ ungesättigten Spezies Cp * Ir (PMe 3 ), die über oxidative Addition mit Cyclohexan und Neopentan unter Bildung des reagierte entsprechende Hydridoalkylkomplexe, Cp * Ir (PMe 3 ) HR, wobei R = Cyclohexyl bzw. Neopentyl. WAG Graham fand heraus, dass dieselben Kohlenwasserstoffe bei Bestrahlung mit Cp * Ir (CO) 2 reagieren und die verwandten Alkylhydridokomplexe Cp * Ir (CO) HR ergeben, wobei R = Cyclohexyl bzw. Neopentyl. Im letzteren Beispiel wird angenommen, dass die Reaktion über die oxidative Addition von Alkan an ein 16-Elektronen-Iridium (I) -Zwischenprodukt, Cp * Ir (CO), verläuft, das durch Bestrahlung von Cp * Ir (CO) 2 gebildet wird .
Die selektive Aktivierung und Funktionalisierung von Alkan- CH -Bindungen wurde unter Verwendung eines Wolframkomplexes beschrieben , der mit Pentamethylcyclopentadienyl- , Nitrosyl- , Allyl- und Neopentylliganden, Cp * W (NO) (η 3 -allyl) (CH 2 CMe 3 ), ausgestattet war.
In einem Beispiel dieses System beinhalten, das Alkan Pentan wird selektiv auf das umgewandelte Halogenkohlenstoff- 1-Iodpentan . Diese Umwandlung wurde durch die Thermolyse von Cp * W (NO) (η 3 -Allyl) (CH 2 CMe 3 ) in Pentan bei Raumtemperatur erreicht , was zur Eliminierung von Neopentan durch einen Prozess pseudoerster Ordnung führte und ein elektronisch nicht nachweisbares erzeugte und sterisch ungesättigte 16-Elektronen - Zwischenprodukt , das durch eine koordinierten η 2 - Butadien - Liganden. Die anschließende intermolekulare Aktivierung eines Pentan-Lösungsmittelmoleküls ergibt dann einen 18-Elektronen- Komplex mit einem n- Pentylliganden. In einem separaten Schritt setzt die Reaktion mit Iod bei –60 ° C 1-Iodpentan aus dem Komplex frei.
Gerichtete CH-Aktivierung
Bei der gerichteten, chelatunterstützten oder "geführten" CH-Aktivierung werden Gruppen geleitet , die die Regio- und Stereochemie beeinflussen. Dies ist der nützlichste Stil der CH-Aktivierung in der organischen Synthese. N, N-Dimethylbenzylamin erfährt Cyclometallierung leicht durch viele Übergangsmetalle. Eine semi-praktische Implementierung beinhaltet eine schwache Koordination von Direktionsgruppen, wie die Murai-Reaktion zeigt .

Der Mechanismus für die Pd-katalysierten CH-Aktivierungsreaktionen von 2-Phenylpyridin beinhaltet ein Metallacyclus-Zwischenprodukt. Das Zwischenprodukt wird oxidiert, um eine Pd IV- Spezies zu bilden , gefolgt von einer reduktiven Eliminierung, um die CO-Bindung zu bilden und das Produkt freizusetzen.
Borylierung
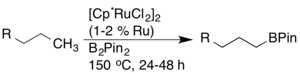
Die Umwandlung von CH-Bindungen in CB-Bindungen durch Borylierung wurde aufgrund ihrer Nützlichkeit bei der Synthese (dh für Kreuzkupplungsreaktionen) gründlich untersucht. John F. Hartwig berichtete über eine hochregioselektive Aren- und Alkan-Borylierung, die durch einen Rhodiumkomplex katalysiert wird. Im Fall von Alkanen wurde eine ausschließliche terminale Funktionalisierung beobachtet.
Später wurde entdeckt, dass Rutheniumkatalysatoren eine höhere Aktivität und funktionelle Gruppenverträglichkeit aufweisen.
Es wurden auch andere Borylierungskatalysatoren entwickelt, einschließlich Katalysatoren auf Iridiumbasis, die CH-Bindungen mit hoher Verträglichkeit erfolgreich aktivieren.
Weitere Informationen finden Sie unter Borylierung .
Erdgas
Natürlich vorkommendes Methan wird trotz seiner Fülle und geringen Kosten nicht als chemisches Ausgangsmaterial verwendet. Gegenwärtige Technologie nutzt Methan in erstaunlicher Weise durch Dampfreformierung, um Synthesegas , ein Gemisch aus Kohlenmonoxid und Wasserstoff, zu erzeugen . Dieses Synthesegas wird dann in Fischer-Tropsch-Reaktionen verwendet, um Produkte mit längerer Kohlenstoffkette oder Methanol herzustellen, eines der wichtigsten industriellen chemischen Ausgangsmaterialien. Eine faszinierende Methode zur Umwandlung dieser Kohlenwasserstoffe ist die CH-Aktivierung. Roy A. Periana zum Beispiel berichtet , dass Komplexe mit späten Übergangsmetalle, wie beispielsweise Pt , Pd , Au und Hg , reagieren mit Methan (CH 4 ) in H 2 SO 4 , um die Ausbeute methyl Bisulfat . Das Verfahren wurde jedoch nicht kommerziell implementiert.
Asymmetrische CH-Aktivierungen

Die Totalsynthese von Lithospermsäure verwendet eine geführte CH-Funktionalisierung im späten Stadium zu einem hochfunktionalisierten System. Die dirigierende Gruppe, ein chirales nichtracemisches Imin, kann eine intramolekulare Alkylierung durchführen, die die Rhodium-katalysierte Umwandlung von Imin zu Dihydrobenzofuran ermöglicht.
Die Totalsynthese von Calothrixin A und B zeigt eine intramolekulare Pd-katalysierte Kreuzkupplungsreaktion über CH-Aktivierung, ein Beispiel für eine geführte CH-Aktivierung. Eine Kreuzkopplung tritt zwischen Aryl-CI- und CH-Bindungen auf, um eine CC-Bindung zu bilden. Die Synthese eines Meskalinanalogons nutzt die Rhodium- katalysierte enantioselektive Anellierung eines Arylimins über eine CH-Aktivierung.
Siehe auch
- Oxidative Kupplung von Methan
- Kreuzdehydrierende Kupplung [CDC-Reaktion]
- Shilov-System
- Metaselektive CH-Funktionalisierung
Ältere Bewertungen
- Vor 2004
- Arndtsen, BA; Bergman, RG; Mobley, TA; Peterson, TH (1995). "Selektive intermolekulare Kohlenstoff-Wasserstoff-Bindungsaktivierung durch synthetische Metallkomplexe in homogener Lösung". Berichte über chemische Forschung . 28 (3): 154–162. doi : 10.1021 / ar00051a009 .
- Crabtree, RH (2001). "Alkan-CH-Aktivierung und -Funktionalisierung mit homogenen Übergangsmetallkatalysatoren: ein Jahrhundert Fortschritt - ein neues Jahrtausend in Aussicht". J. Chem. Soc., Dalton Trans . 17 (17): 2437–2450. doi : 10.1039 / B103147N .
- 2004-7
- Crabtree, RH (2004). "Metallorganische Alkan-CH-Aktivierung". J. Organomet. Chem . 689 (24): 4083–4091. doi : 10.1016 / j.jorganchem.2004.07.034 .
- Organometallische CH-Bindungsaktivierung: Eine Einführung Alan S. Goldman und Karen I. Goldberg ACS Symposium Series 885, Aktivierung und Funktionalisierung von CH-Bindungen, 2004 , 1–43
- Periana, RA; Bhalla, G.; Tenn, WJ; III; Young, KJH; Liu, XY; Mironov, O.; Jones, C.; Ziatdinov, VR (2004). "Perspektiven auf einige Herausforderungen und Ansätze für die Entwicklung der nächsten Generation selektiver Niedertemperatur-Oxidationskatalysatoren für die Alkanhydroxylierung auf der Grundlage der CH-Aktivierungsreaktion". Journal of Molecular Catalysis A: Chemisch . 220 (1): 7–25. doi : 10.1016 / j.molcata.2004.05.036 .
- Lersch, M. Tilset (2005). "Mechanistische Aspekte der CH-Aktivierung durch Pt-Komplexe". Chem. Rev . 105 (6): 2471–2526. doi : 10.1021 / cr030710y . PMID 15941220 . , Vedernikov, AN (2007). "Jüngste Fortschritte bei der Platin-vermittelten CH-Bindungsfunktionalisierung". Curr. Org. Chem . 11 (16): 1401–1416. doi : 10.2174 / 138527207782418708 .
- 2008-2011
- Davies, HML; Manning, JR (2008). "Katalytische CH-Funktionalisierung durch Metallcarbenoid- und Nitrenoidinsertion" . Natur . 451 (7177): 417–424. Bibcode : 2008Natur.451..417D . doi : 10.1038 / nature06485 . PMC 3033428 . PMID 18216847 .
- Boutadla, Y.; Davies, DL; Macgregor, SA; Poblador-Bahamonde, AI (2009). "Mechanismen der CH-Bindungsaktivierung: reiche Synergie zwischen Berechnung und Experiment" . Dalton Trans . 2009 (30): 5820–5831. doi : 10.1039 / B904967C . PMID 19623381 .
- Wencel-Delord, J.; Dröge, T.; Liu, F.; Glorius, F. (2011). "Auf dem Weg zu einer milden metallkatalysierten CH-Bindungsaktivierung". Chem. Soc. Rev. 40 (9): 4740–4761. doi : 10.1039 / C1CS15083A . PMID 21666903 .
- Shulpin, GB (2010). "Verbesserung der Selektivität bei der Funktionalisierung von CH-Bindungen: Ein Überblick". Org. Biomol. Chem . 8 (19): 4217–4228. doi : 10.1039 / c004223d . PMID 20593075 .
- Lyon, TW; Sanford, MS (2010). "Palladiumkatalysierte ligandengesteuerte CH-Funktionalisierungsreaktionen" . Chem. Rev . 110 (2): 1147–1169. doi : 10.1021 / cr900184e . PMC 2836499 . PMID 20078038 . * Balcells, D.; Clot, E.; Eisenstein, O. (2010). "CH-Bindungsaktivierung in Übergangsmetallspezies aus rechnerischer Sicht". Chem. Rev . 110 (2): 749–823. doi : 10.1021 / cr900315k . PMID 20067255 .
- 2012-2015
- Hashiguchi, BG; Bischof, SM; Konnick, MM; Periana, RA (2012). "Entwurf von Katalysatoren zur Funktionalisierung nicht aktivierter CH-Bindungen basierend auf der CH-Aktivierungsreaktion". Acc. Chem. Res . 45 (6): 885–898. doi : 10.1021 / ar200250r . PMID 22482496 .
- Kuhl, N.; Hopkinson, MN; Wencel-Delord, J.; Glorius, F. (2012). "Beyond Directing Groups: Übergangsmetallkatalysierte CH-Aktivierung einfacher Arene". Angew. Chem. Int. Ed . 51 (41): 10236–10254. doi : 10.1002 / anie.201203269 . PMID 22996679 .
- Wencel-Delord, J.; Glorius, F. (2013). "Die Aktivierung von CH-Bindungen ermöglicht den schnellen Aufbau und die Diversifizierung funktioneller Moleküle im späten Stadium". Naturchemie . 5 (5): 369–375. Bibcode : 2013NatCh ... 5..369W . doi : 10.1038 / nchem.1607 . PMID 23609086 .
Zusätzliche Quellen
- Bergman FAQ in Nature zur CH-Aktivierung (2007)
- Literaturpräsentation von Ramtohul in der Stoltz-Gruppe zu Anwendungen der CH-Aktivierung
- Powerpoint zu John Bercaws Arbeit
- Zentrum für selektive CH-Funktionalisierung