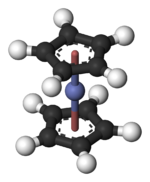
Kobaltozän - Cobaltocene
|
|
|||
| Namen | |||
|---|---|---|---|
|
IUPAC-Namen
Cobaltocen-
Bis ( η 5 -cyclopentadienyl) cobalt |
|||
| Andere Namen
Cp 2 Co.
|
|||
| Kennungen | |||
|
3D-Modell ( JSmol )
|
|||
| ChEBI | |||
| ChemSpider | |||
| ECHA InfoCard | 100.013.692 | ||
| EG-Nummer | |||
|
PubChem CID
|
|||
| RTECS-Nummer | |||
| UNII | |||
|
CompTox Dashboard ( EPA )
|
|||
|
|||
|
|||
| Eigenschaften | |||
| [Co ( η 5 -C 5 H 5 ) 2 ] | |||
| Molmasse | 189,12 g / mol | ||
| Aussehen | Dunkelvioletter Feststoff | ||
| Schmelzpunkt | 171–173 ° C (340–343 ° F; 444–446 K) | ||
| Unlöslich | |||
| Struktur | |||
| Sandwich | |||
| Null | |||
| Thermochemie | |||
|
Std molare
Entropie ( S |
236 JK −1 mol −1 | ||
|
Std Enthalpie der
Bildung (Δ f H ⦵ 298 ) |
+237 kJ / mol (unsicher) | ||
|
Std Enthalpie der
Verbrennungs (Δ c H ⦵ 298 ) |
–5839 kJ / mol | ||
| Gefahren | |||
| Sicherheitsdatenblatt | Externes Sicherheitsdatenblatt | ||
| GHS-Piktogramme |
 
|
||
| GHS Signalwort | Achtung | ||
| H228 , H317 , H351 | |||
| P210 , P261 , P280 , P363 , P405 , P501 | |||
| NFPA 704 (Feuerdiamant) | |||
| Verwandte Verbindungen | |||
|
Verwandte Metallocene
|
Ferrocen- Nickelozän- Rhodozän |
||
|
Sofern nicht anders angegeben, werden Daten für Materialien in ihrem Standardzustand (bei 25 ° C, 100 kPa) angegeben. |
|||
|
|
|||
| Infobox-Referenzen | |||
Cobaltocen , auch bekannt als Bis (cyclopentadienyl) cobalt (II) oder sogar "Bis-Cp-Cobalt", ist eine Organocobaltverbindung mit der Formel Co (C 5 H 5 ) 2 . Es ist ein dunkelvioletter Feststoff, der leicht über Raumtemperatur sublimiert. Kobaltozän wurde kurz nach Ferrocen , dem ersten Metallozän, entdeckt . Aufgrund der Leichtigkeit, mit der es mit Sauerstoff reagiert, muss die Verbindung mit luftfreien Techniken gehandhabt und gelagert werden .
Synthese
Cobaltocen wird durch Umsetzung von Natriumcyclopentadienid (NaC 5 H 5 ) mit wasserfreiem Cobalt (II) -chlorid in THF- Lösung hergestellt. Natriumchlorid wird kogeneriert und das metallorganische Produkt wird üblicherweise durch Vakuumsublimation gereinigt .
Struktur und Bindung
In Co (C 5 H 5 ) 2 ist das Co-Zentrum zwischen zwei Cyclopentadienyl (Cp) -Ringen "eingeklemmt" . Die Co-C-Bindungslängen betragen etwa 2.1 Å und sind damit etwas länger als die Fe-C-Bindung in Ferrocen.
Co (C 5 H 5 ) 2 gehört zu einer Gruppe von metallorganischen Verbindungen, die als Metallocene oder Sandwichverbindungen bezeichnet werden. Kobaltozän hat 19 Valenzelektronen, eines mehr als gewöhnlich in Organotransitionsmetallkomplexen wie seinem sehr stabilen relativen Ferrocen. (Siehe 18-Elektronen-Regel .) Dieses zusätzliche Elektron besetzt ein Orbital, das in Bezug auf die Co-C-Bindungen antibindend ist. Folglich sind die Co-C-Abstände etwas länger als die Fe-C-Bindungen in Ferrocen. Viele chemische Reaktionen von Co (C 5 H 5 ) 2 sind durch seine Tendenz gekennzeichnet, dieses "zusätzliche" Elektron zu verlieren, was ein 18-Elektronen-Kation ergibt, das als Cobaltocenium bekannt ist:
Der ansonsten nahe Verwandte von Cobaltocen, Rhodocen, existiert nicht als Monomer, sondern dimerisiert spontan durch Bildung einer CC-Bindung zwischen Cp-Ringen.
Reaktionen
Redoxeigenschaften
Co (C 5 H 5 ) 2 ist ein im Labor übliches Einelektronenreduktionsmittel. Tatsächlich ist die Reversibilität des Co (C 5 H 5 ) 2 -Redoxpaares so gut, dass Co (C 5 H 5 ) 2 in der Cyclovoltammetrie als interner Standard verwendet werden kann . Sein permethyliertes Analogon Decamethylcobaltocen (Co (C 5 Me 5 ) 2 ) ist aufgrund der induktiven Abgabe der Elektronendichte aus den 10 Methylgruppen ein besonders starkes Reduktionsmittel, was das Cobalt dazu veranlasst, sein "zusätzliches" Elektron noch mehr aufzugeben. Diese beiden Verbindungen sind seltene Beispiele für Reduktionsmittel, die sich in unpolaren organischen Lösungsmitteln lösen. Die Reduktionspotentiale dieser Verbindungen folgen unter Verwendung des Ferrocen- Ferrocenium- Paares als Referenz:
| Halbreaktion | E 0 (V) |
|---|---|
|
Fe (C. 5H. 5)+ 2+ e - ⇌ Fe (C 5 H 5 ) 2 |
0,00 (per Definition) |
|
Fe (C. 5Mich 5)+ 2+ e - ⇌ Fe (C 5 Me 5 ) 2 |
–0,59 |
|
Co (C. 5H. 5)+ 2+ e - ⇌ Co (C 5 H 5 ) 2 |
-1,33 |
|
Co (C. 5Mich 5)+ 2+ e - ⇌ Co (C 5 Me 5 ) 2 |
–1,94 |
Die Daten zeigen, dass die Decamethylverbindungen etwa 600 mV stärker reduzieren als die Ausgangsmetallocene. Dieser Substituenteneffekt wird jedoch durch den Einfluss des Metalls überschattet: Der Wechsel von Fe zu Co macht die Reduktion um über 1,3 Volt günstiger.
Carbonylierung
Die Behandlung von Co (C 5 H 5 ) 2 mit Kohlenmonoxid ergibt das Cobalt (I) -Derivat Co (C 5 H 5 ) (CO) 2 , was mit dem Verlust eines Cp-Liganden einhergeht. Diese Umwandlung wird nahe 130ºC mit 500 psi CO durchgeführt.