Kryoablation - Cryoablation
| Kryoablation | |
|---|---|
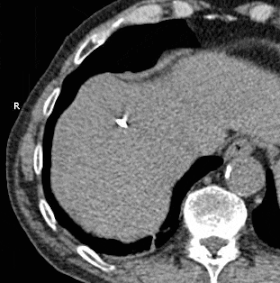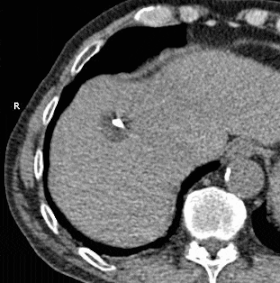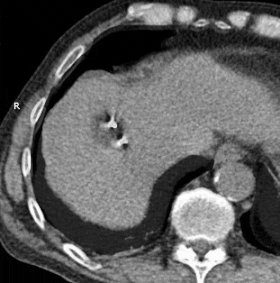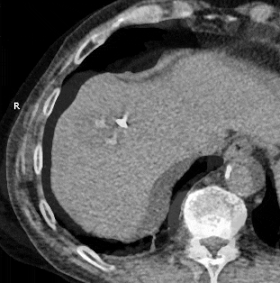 Animiertes GIF, das die Kryoablation der Masse im rechten Leberlappen mit zwei Sonden zeigt. Die verstrichene Zeit beträgt ungefähr 30 Minuten.
| |
| ICD-9-CM | 37,33 , 37,34 , 60,62 |
| Gittergewebe | D003452 |
Kryoablation ist ein Verfahren, bei dem extreme Kälte verwendet wird , um Gewebe zu zerstören . Die Kryoablation wird mit Hohlnadeln (Kryosonden) durchgeführt, durch die gekühlte, wärmeleitende Flüssigkeiten zirkuliert werden. Kryosonden werden neben dem Target so positioniert, dass der Einfrierprozess das erkrankte Gewebe zerstört. Sobald die Sonden an Ort und Stelle sind, führt die angeschlossene kryogene Gefriereinheit Wärme von der Spitze der Sonde und damit von dem umgebenden Gewebe ab ("kühlt").
Die Ablation erfolgt in Gewebe, das durch mindestens drei Mechanismen eingefroren wurde:
- Bildung von Eiskristallen innerhalb von Zellen, wodurch Membranen zerstört werden und unter anderem der Zellstoffwechsel unterbrochen wird;
- Blutgerinnung, wodurch der Blutfluss zum Gewebe unterbrochen wird, was wiederum Ischämie und Zelltod verursacht; und
- Induktion der Apoptose , der sogenannten programmierten Zelltodkaskade.
Die häufigste Anwendung der Kryoablation ist die Ablation von soliden Tumoren in Lunge, Leber, Brust, Niere und Prostata. Die Verwendung bei Prostata- und Nierenkryoablation ist am häufigsten. Obwohl sie manchmal in der Kryochirurgie durch laparoskopische oder offene chirurgische Zugänge angewendet wird , wird die Kryoablation meistens perkutan (durch die Haut und in das Zielgewebe, das den Tumor enthält) von einem Facharzt, beispielsweise einem interventionellen Radiologen, durchgeführt . Der Begriff stammt von Kryo- + Ablation .
Prostata
Die Kryoablation der Prostata ist mäßig wirksam, kann aber wie bei jedem Verfahren zur Entfernung der Prostata auch zu Impotenz führen. Die Kryoablation der Prostata wird bei drei Patientenkategorien eingesetzt:
- als Primärtherapie bei Patienten, bei denen die Sexualfunktion weniger wichtig ist oder die schlechte Kandidaten für eine radikale retropubische Prostatektomie (RRP, operative Entfernung der Prostata) sind;
- als Salvage-Therapie bei Patienten, bei denen die Brachytherapie (die Verwendung von implantierten radioaktiven "Seeds", die in die Prostata eingebracht werden) oder die externe Strahlentherapie (EBRT) versagt haben; und
- fokale Therapie bei kleineren, diskreten Tumoren bei jüngeren Patienten.
Knochenkrebs
Die Kryoablation wurde als Alternative zur Radiofrequenzablation bei der Behandlung mäßiger bis starker Schmerzen bei Patienten mit metastasierenden Knochenerkrankungen untersucht . Der durch diese Technik erzeugte Bereich der Gewebezerstörung kann durch CT effektiver überwacht werden als durch RFA, ein potenzieller Vorteil bei der Behandlung von Tumoren in der Nähe kritischer Strukturen.
Nieren
Die Kryoablation hat bei der Behandlung von Nierenzellkarzinomen ähnliche Ergebnisse wie die Radiofrequenzablation .
Brustkrebs
Kryoablation bei Brustkrebs ist typischerweise nur bei kleinen Tumoren möglich. Häufig wird nach der Kryoablation eine Operation durchgeführt. Ab 2014 ist weitere Forschung erforderlich, bevor sie die Lumpektomie ersetzen kann .
Herz
Eine andere Art der Kryoablation wird verwendet, um die normale elektrische Leitung wiederherzustellen, indem Gewebe oder Herzbahnen eingefroren werden, die die normale Verteilung der elektrischen Impulse des Herzens stören. Kryoablation wird bei zwei Arten von Eingriffen zur Behandlung von Arrhythmien verwendet : (1) katheterbasierte Verfahren und (2) chirurgische Eingriffe.
Ein Katheter ist ein sehr dünner Schlauch, der in eine Vene im Bein des Patienten eingeführt und zum Herzen gefädelt wird, wo er Energie liefert, um die Arrhythmie des Patienten zu behandeln. Bei chirurgischen Eingriffen wird eine flexible Sonde direkt auf ein freiliegendes Herz angewendet, um die Energie zu applizieren, die die Arrhythmie unterbricht. Durch das Abkühlen der Spitze eines Kryoablationskatheters ( Kardiologie ) oder Sonde ( Herzchirurgie ) auf Minustemperaturen werden die Zellen im Herzen, die die Herzrhythmusstörungen leiten, so verändert, dass sie keine elektrischen Impulse mehr leiten.
Fibroadenom
Kryoablation wird derzeit auch zur Behandlung von Fibroadenomen der Brust eingesetzt. Fibroadenome sind gutartige Brusttumore, die bei etwa 10 % der Frauen (hauptsächlich im Alter von 15 bis 30 Jahren) auftreten.
Bei diesem von der US-amerikanischen Food and Drug Administration (FDA) zugelassenen Verfahren wird eine ultraschallgeführte Sonde in das Fibroadenom eingeführt und anschließend mit extrem kalten Temperaturen die abnormen Zellen zerstört. Im Laufe der Zeit werden die Zellen wieder in den Körper resorbiert. Der Eingriff kann in einer Arztpraxis mit örtlicher Betäubung durchgeführt werden und hinterlässt im Vergleich zu offenen chirurgischen Verfahren nur sehr wenige Narben.
Katheterbasierte Verfahren
Es können verschiedene katheterbasierte Ablationstechniken verwendet werden, die im Allgemeinen in zwei Kategorien eingeteilt werden: (1) kältebasierte Verfahren, bei denen Gewebekühlung verwendet wird, um die Arrhythmie zu behandeln, und (2) wärmebasierte Verfahren, bei denen hohe Temperaturen verwendet werden, um die Arrhythmie zu verändern anormal leitfähiges Gewebe im Herzen.
Kryoablation
Kalte Temperaturen werden bei der Kryoablation verwendet, um Zellen zu kühlen oder einzufrieren, die Herzrhythmusstörungen verursachen. Der Katheter entzieht dem Gewebe Wärme, um es auf Temperaturen von bis zu -75 °C abzukühlen. Dies verursacht eine lokale Narbenbildung, die unerwünschte Leitungswege schneidet.
Dies ist eine viel neuere Behandlung für supraventrikuläre Tachykardie (SVT), die den atrioventikulären (AV) Knoten direkt betrifft. Eine SVT mit Beteiligung des AV-Knotens ist oft eine Kontraindikation für die Anwendung der Radiofrequenzablation, da das Risiko einer Verletzung des AV-Knotens besteht und die Patienten gezwungen sind, einen permanenten Schrittmacher zu erhalten. Bei der Kryoablation können Gewebebereiche durch begrenztes, reversibles Einfrieren (zB auf –10°C) kartiert werden. Ist das Ergebnis unerwünscht, kann das Gewebe ohne bleibende Schäden wieder aufgewärmt werden. Andernfalls kann das Gewebe dauerhaft abgetragen werden, indem es auf eine niedrigere Temperatur (zB -73 °C) eingefroren wird.
Diese Therapie hat die AV-Knoten-Reentry-Tachykardie (AVNRT) und andere AV-Knoten-Tachyarrhythmien revolutioniert . Es hat Menschen, die ansonsten kein Kandidat für eine Radiofrequenzablation waren, eine Chance auf eine Heilung ihres Problems gegeben. Diese Technologie wurde Ende der 1990er Jahre am Montreal Heart Institute entwickelt. Die Therapie wurde 2001 in Europa und 2004 nach dem "Frosty Trial" in den USA erfolgreich eingeführt.
Im Jahr 2004 wurde die Technologie im Mittleren Westen der USA im Miami Valley Hospital in Dayton, Ohio, von Mark Krebs, MD, FACC, Matthew Hoskins, RN, BSN und Ken Peterman, RN, BSN, eingeführt. Diese Elektrophysiologie-Experten konnten die ersten 12 Kandidaten in ihrer Einrichtung erfolgreich heilen.
Kryoablation bei AVNRT und anderen Arrhythmien hat einige Nachteile. Eine kürzlich durchgeführte Studie kam zu dem Schluss, dass die Eingriffszeiten bei der Kryoablation im Durchschnitt etwas länger sind als bei der traditionellen Radiofrequenz-Ablation (auf Wärmebasis). Außerdem wurde mit dieser Technik eine höhere Rate von Geräteausfällen aufgezeichnet. Obwohl die kurzfristige Erfolgsrate der HF-Behandlung entspricht, scheint die Kryoablation eine signifikant höhere langfristige Rezidivrate zu haben.
Site-Tests
Die Kryotherapie ist in der Lage, eine vorübergehende elektrische Blockade zu erzeugen, indem das Gewebe, von dem angenommen wird, dass es die Arrhythmie leitet, abgekühlt wird. Auf diese Weise kann der Arzt sicherstellen, dass dies die richtige Stelle ist, bevor er dauerhaft deaktiviert wird. Die Möglichkeit, eine Site auf diese Weise zu testen, wird als Site Testing oder Cryomap bezeichnet .
Beim Abtragen von Gewebe in der Nähe des AV-Knotens (ein spezielles Reizleitungszentrum, das elektrische Impulse von den Vorhöfen zu den Ventrikeln überträgt) besteht die Gefahr einer Herzblockade, d. h. eine normale Reizleitung von den Vorhöfen kann nicht auf die Ventrikel übertragen werden. Das Einfrieren von Gewebe in der Nähe des AV-Knotens provoziert weniger wahrscheinlich einen irreversiblen Herzblock als eine Ablation mit Wärme.
Chirurgische Maßnahmen
Wie bei katheterbasierten Verfahren können Techniken verwendet werden, die Heiz- oder Kühltemperaturen verwenden, um Arrhythmien während einer Herzoperation zu behandeln. Es gibt auch Techniken, bei denen Einschnitte im offenen Herzen verwendet werden, um eine abnormale elektrische Leitung zu unterbrechen ( Maze-Verfahren ). Kryochirurgie umfasst die Verwendung von Gefriertechniken zur Behandlung von Herzrhythmusstörungen während der Operation.
Ein Arzt kann die Kryochirurgie während einer Herzoperation als sekundäres Verfahren empfehlen, um eine Arrhythmie zu behandeln, die vorhanden war oder während des primären Eingriffs am offenen Brustkorb auftreten kann. Die häufigsten Herzoperationen, bei denen Kryochirurgie auf diese Weise verwendet werden kann, sind Mitralklappenreparaturen und Koronararterienbypasstransplantationen . Während des Eingriffs wird eine flexible Kryosonde auf oder um das Herz herum platziert und liefert kalte Energie, die das Gewebe, das für die Leitung der Arrhythmie verantwortlich ist, deaktiviert.
Gefäßfehlbildungen
Die Kryoablation wurde kürzlich zur Behandlung von vaskulären Fehlbildungen mit niedrigem Durchfluss wie venösen Malformationen (VM) und fibroadipose vaskulären Anomalien (FAVA) eingesetzt. Die Kryoablation hat sich zur Behandlung dieser Erkrankungen sowohl als Primärtherapie als auch nach Sklerotherapie als wirksam erwiesen .
Kryoimmuntherapie
Die Kryoimmuntherapie ist eine onkologische Behandlung für verschiedene Krebsarten, die die Kryoablation von Tumoren mit einer immuntherapeutischen Behandlung kombiniert . Die alleinige In-vivo-Kryoablation eines Tumors kann eine immunstimulierende, systemische Antitumorantwort auslösen, die zu einem Krebsimpfstoff führt – dem abskopalen Effekt . Die alleinige Kryoablation kann jedoch in Abhängigkeit von verschiedenen Faktoren, wie z. B. einer hohen Gefrierrate, eine unzureichende Immunantwort hervorrufen. Die Kombination der Kryotherapie mit der Immuntherapie verstärkt die immunstimulierende Reaktion und hat synergistische Wirkungen für die Krebsbehandlung.
Geschichte
Die Verwendung von Kälte zur Schmerzlinderung und als entzündungshemmendes Mittel ist seit Hippokrates (460–377 v. Chr.) bekannt. Seitdem gibt es zahlreiche Berichte über Eis, das zur Schmerzlinderung verwendet wurde, einschließlich der alten Ägypter und Avicenna von Persien (AD 982-1070). Seit 1899 verwendet Dr. Campbell White Kältemittel zur Behandlung einer Vielzahl von Erkrankungen, darunter: Lupus erythematodes, Herpes Zoster, Schanker, Nävi, Warzen, Krampfadergeschwüre, Karbunkel, Karzinome und Epitheliome. De Quervain nutzte 1917 erfolgreich Kohlensäure zur Behandlung von Blasenpapillomen und Blasenkrebs. Dr. Irving S. Cooper brachte 1913 das Gebiet der Kryotherapie voran, indem er eine Flüssigstickstoffsonde entwickelte, die Temperaturen von -196 °C erreichen konnte, und es zur Behandlung der Parkinson-Krankheit und zuvor inoperablem Krebs. Coopers Kryosonde hat die Kryotherapie vorangetrieben, was zu einem wachsenden Interesse und an der Praxis der Kryotherapie führte. 1964 setzte Dr. Cahan seine Erfindung der Flüssigstickstoffsonde erfolgreich zur Behandlung von Uterusmyomen und Gebärmutterhalskrebs ein. Die Kryotherapie machte weiter Fortschritte, als Dr. Amoils 1967 eine Flüssigstickstoffsonde entwickelte, die eine kühlende Expansion erreichen konnte.
Mit den technologischen Fortschritten der Kryosonden in den 1960er Jahren kam eine breitere Akzeptanz und Praxis der Kryotherapie. Seit den 1960er Jahren wurden in vielen Teilen der Welt Leber-, Prostata-, Brust-, Knochen- und andere Krebsarten mit Kryoablation behandelt. Der japanische Arzt Dr. Tanaka begann 1968 mit der Behandlung von metastasierendem Brustkrebs mit Kryoablation. In den nächsten drei Jahrzehnten behandelte Dr. Tanaka erfolgreich kleinen und lokalisierten sowie fortgeschrittenen und nicht resezierbaren Brustkrebs mit minimal-invasiver Kryoablation. Alle Brustkrebsfälle von Dr. Tanaka galten als unheilbar: fortgeschritten, inoperabel und resistent gegen Strahlentherapie, Chemotherapie und endokrine Therapie. Gleichzeitig begannen Ärzte, darunter Dr. Ablin und Dr. Gage, Kryoablation zur Behandlung von Prostata- und Knochenkrebs einzusetzen . Dr. Paul J. Wang MD und Dr. Peter L. Friedman MD, PhD erfanden 1988 die Kryoablation für das Herz und Herzrhythmusstörungen. Ihre Patente betrafen den Kryoablationskatheter und das kryogene Mapping (US-Patente 5147355A und 5423807A).
In den 1980er und 1990er Jahren wurden mit der Einführung von CMS Cryoprobe und Accuprobe dramatische Fortschritte bei Geräten und Bildgebungstechniken erzielt. CT , MRI , Ultraschall geführt cryoprobes zur Verfügung standen und verbessert die Fähigkeiten von Kryosonden in Behandlung. Begeistert von den neuesten Fortschritten in der Kryotherapie hat China in den 1990er Jahren die Kryotherapie eingeführt, um viele onkologische Erkrankungen zu behandeln. Da die Vorteile bekannt sind, genehmigte die FDA 1998 die Behandlung von Prostatakrebs mit Kryoablation.
