Dess-Martin Periodinane - Dess–Martin periodinane
|
|

|
|
| Namen | |
|---|---|
|
Bevorzugter IUPAC-Name
3-Oxo-1λ 5 , 2-benziodoxole-1,1,1 (3 H ) -triyl Triacetat |
|
| Andere Namen
Dess-Martin-Periodinane
|
|
| Kennungen | |
|
3D-Modell ( JSmol )
|
|
| ChemSpider | |
| ECHA InfoCard |
100.197.885 |
|
PubChem CID
|
|
| UNII | |
|
CompTox Dashboard ( EPA )
|
|
|
|
|
|
| Eigenschaften | |
| C 13 H 13 IO 8 | |
| Molmasse | 424,14 g / mol |
| Aussehen | weißes Pulver, Chips, Kristalle oder kristallines Pulver und / oder Brocken |
| Dichte | 1,362 g / cm 3 Feststoff |
| Schmelzpunkt | 103 bis 133 ° C (217 bis 271 ° F; 376 bis 406 K) |
| Verwandte Verbindungen | |
|
Verwandte Verbindungen
|
2-Iodoxybenzoesäure |
|
Sofern nicht anders angegeben, werden Daten für Materialien in ihrem Standardzustand (bei 25 ° C, 100 kPa) angegeben. |
|
| Infobox-Referenzen | |
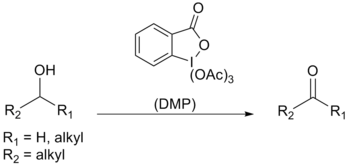
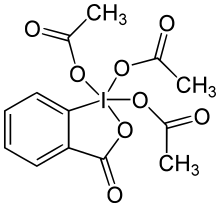
Dess-Martin-Periodinan ( DMP ) ist ein chemisches Reagenz, das bei der Dess-Martin-Oxidation verwendet wird und primäre Alkohole zu Aldehyden und sekundäre Alkohole zu Ketonen oxidiert . Dieses Periodinan hat gegenüber Oxidationsmitteln auf Chrom- und DMSO- Basis mehrere Vorteile , darunter mildere Bedingungen (Raumtemperatur, neutraler pH-Wert), kürzere Reaktionszeiten, höhere Ausbeuten, vereinfachte Aufarbeitung, hohe Chemoselektivität, Toleranz gegenüber empfindlichen funktionellen Gruppen und eine lange Haltbarkeit. Die Verwendung im industriellen Maßstab wird jedoch durch ihre Kosten und ihre potenziell explosive Natur erschwert. Es ist nach den amerikanischen Chemikern Daniel Benjamin Dess und James Cullen Martin benannt , die das Reagenz 1983 entwickelt haben. Es basiert auf IBX , aber aufgrund der an das zentrale Iodatom gebundenen Acetatgruppen ist DMP viel reaktiver als IBX und viel löslicher in organischen Lösungsmitteln.
Vorbereitung
Es wurde festgestellt, dass die freundlichste Synthese von IBX darin besteht, 2-Iodbenzoesäure mit Oxon in Wasser bei erhöhten Temperaturen 3 Stunden lang zu behandeln. IBX wird dann unter Verwendung der Modifikationen von Irland und Liu gegenüber dem ursprünglichen Verfahren acyliert. Diese Modifikationen ermöglichten höhere Ausbeuten und ein vereinfachtes Aufarbeitungsverfahren. Die resultierenden Feststoffe können durch Filtration und Waschen mit Ether erhalten werden. Irland und Liu verwendeten eine katalytische Menge Tosylsäure , wodurch die Reaktion in weniger als 2 Stunden (im Vergleich zur klassischen Synthese unter Verwendung von 24 Stunden) und in Ausbeuten von mehr als 90% abgeschlossen werden konnte.
Das von Boeckman und Mullins vorgestellte klassische Verfahren umfasste das Erhitzen einer Lösung von Kaliumbromat , Schwefelsäure , 2-Iodbenzoesäure, um IBX (1-Hydroxy-1,2-benziodoxol-3 (1H) -on-1-oxid, 2-iodoxybenzoesäure zu ergeben Säure ). IBX wurde dann unter Verwendung von Essigsäure und Essigsäureanhydrid acyliert .
Oxidationsmechanismus
Dess-Martin-Periodinan wird hauptsächlich als Oxidationsmittel für komplexe, empfindliche und multifunktionelle Alkohole verwendet . Einer der Gründe für seine Wirksamkeit ist seine hohe Selektivität für die Komplexierung der Hydroxylgruppe , die es Alkoholen ermöglicht, schnell einen Ligandenaustausch durchzuführen ; der erste Schritt in der Oxidationsreaktion.
Protonen-NMR hat gezeigt, dass unter Verwendung eines Äquivalents Alkohol das Zwischenprodukt Diacetoxyalkoxyperiodinan bildet. Das Acetat wirkt dann als Base, um das α-H aus dem Alkohol zu deprotonieren, um die Carbonylverbindung , Iodinan und Essigsäure zu ergeben .
Wenn ein Diol oder mehr als ein Äquivalent Alkohol verwendet wird, wird stattdessen Acetoxydialkoxyperiodinan gebildet. Aufgrund der labilen Natur dieses speziellen Periodinans erfolgt die Oxidation viel schneller.
Schreiber und Mitarbeiter haben gezeigt, dass Wasser die Geschwindigkeit der Oxidationsreaktion erhöht. Dess und Martin hatten ursprünglich beobachtet, dass die Oxidation von Ethanol erhöht war, wenn ein zusätzliches Äquivalent Ethanol vorhanden war. Es wird angenommen, dass die Dissoziationsrate des endgültigen Acetatliganden vom Iod aufgrund der Elektronendonorfähigkeit der Hydroxylgruppe (wodurch die I-OAc-Bindung geschwächt wird) erhöht ist .
Chemoselektivität
Unter den Standardbedingungen von Dess-Martin-Periodinan können Alkohole zu Aldehyden / Ketonen oxidiert werden, ohne Furanringe , Sulfide , Vinylether und sekundäre Amide zu beeinflussen . Allylalkohole lassen sich leicht mit DMP oxidieren, die sich mit den typischen Oxidationsmitteln typischerweise nur schwer in ihre jeweiligen Carbonyle umwandeln lassen.
Myers und Mitarbeiter stellten fest, dass DMP N-geschützte Aminoalkohole ohne Epimerisierung oxidieren kann (im Gegensatz zu den meisten anderen Oxidationsmitteln, einschließlich der Swern-Oxidation). Diese geschützten Aminoalkohole können in der pharmazeutischen Industrie sehr wichtig sein.
Benzyl- und Allylalkohole reagieren schneller als gesättigte Alkohole, während DMP Aldoxime und Ketoxime zu ihren jeweiligen Aldehyden und Ketonen oxidiert, schneller als ein primärer, sekundärer oder benzylischer Alkohol zu seinem jeweiligen Carbonyl.
In einem Beispiel der Dess-Martin-Oxidation wird ein empfindlicher α-β-ungesättigter Alkohol in seinen entsprechenden Aldehyd umgewandelt. Diese Einheit wurde in mehreren Naturstoffen gefunden und könnte aufgrund ihrer hohen Funktionalität ein wertvoller synthetischer Baustein in der organischen Synthese sein. Thongsornkleeb und Danheiser oxidierten diesen empfindlichen Alkohol unter Verwendung der Dess-Martin-Oxidation und änderten das Aufarbeitungsverfahren (Verdünnen mit Pentanen, Waschen mit Poly ( 4-vinylpyridin ), um die während der Reaktion erzeugte Essigsäure zu entfernen, filtrieren und konzentrieren durch Destillation.
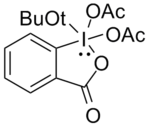
t- Butyl-DMP
Difluor- und Monofluoralkohole sind schwieriger zu oxidieren. Swern-Oxidation wurde verwendet, aber ein großer Überschuss des Oxidationsmittels musste eingesetzt werden, und in einigen Fällen ergaben sich keine reproduzierbaren Ergebnisse. Linderman und Graves stellten fest, dass DMP in den meisten Fällen erfolgreich war, jedoch das Vorhandensein von nukleophilen funktionellen Gruppen im Alkohol nicht tolerieren konnte , da diese mit DMP durch Verdrängung von Acetat reagierten. Die Verwendung der unten gezeigten Verbindung ergab die gewünschten Carbonyle in hohen Ausbeuten, da die Addition der tert- Butoxygruppe aufgrund ihrer sterischen Masse diese Nebenreaktionen minimiert.
Siehe auch
- Alkoholoxidation
- Pyridiniumchlorochromat
- Jones-Oxidation
- Oppenauer Oxidation
- Pfitzner-Moffatt-Oxidation
- Parikh-Doering-Oxidation
- Albright-Goldman-Oxidation
- Swern Oxidation
- Corey-Kim-Oxidation
- Ley-Oxidation ( TPAP- Oxidation)
- TEMPO- Oxidation