Koordinationssphäre - Coordination sphere
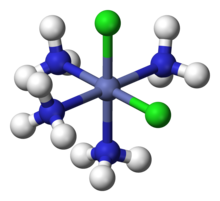
Die NH 3 - und Cl-Gruppen bilden eine Koordinationssphäre um das zentrale Kobaltion .
In der Koordinationschemie , die erste Koordinationssphäre bezieht sich auf die Anordnung von Molekülen und Ionen (die Liganden ) direkt an das Metallzentralatom gebunden ist . Die zweite Koordinationssphäre besteht aus Molekülen und Ionen, die auf verschiedene Weise an die erste Koordinationssphäre gebunden sind.
Erste Koordinationssphäre
Die erste Koordinationssphäre bezieht sich auf die Moleküle, die direkt an das Metall gebunden sind. Die Wechselwirkungen zwischen der ersten und der zweiten Koordinationssphäre beinhalten üblicherweise Wasserstoffbrücken. Für geladene Komplexe ist die Ionenpaarung wichtig.

In Hexammincobalt (III) chlorid ([Co (NH 3 ) 6 ] Cl 3 )) bilden das Cobaltkation plus die 6 Ammoniakliganden die erste Koordinationssphäre. Die Koordinationssphäre dieses Ions besteht somit aus einem zentralen MN 6 -Kern, der durch 18 nach außen strahlende NH-Bindungen "dekoriert" ist.
Zweite Koordinationssphäre

Metallionen können so beschrieben werden, dass sie aus einer Reihe von zwei konzentrischen Koordinationskugeln bestehen, der ersten und der zweiten. Weiter entfernt von der zweiten Koordinationssphäre verhalten sich die Lösungsmittelmoleküle eher wie " Bulk-Lösungsmittel ". Die Simulation der zweiten Koordinationssphäre ist in der Computerchemie von Interesse . Die zweite Koordinationssphäre kann aus Ionen (insbesondere in geladenen Komplexen), Molekülen (insbesondere solchen, die Wasserstoff an Liganden in der ersten Koordinationssphäre binden) und Teilen eines Ligandenrückgrats bestehen. Im Vergleich zur ersten Koordinationssphäre hat die zweite Koordinationssphäre einen weniger direkten Einfluss auf die Reaktivität und die chemischen Eigenschaften des Metallkomplexes. Dennoch ist die zweite Koordinationssphäre relevant für das Verständnis der Reaktionen des Metallkomplexes, einschließlich der Mechanismen des Ligandenaustauschs und der Katalyse.
Rolle in der Katalyse
Mechanismen von Metalloproteinen rufen häufig eine Modulation der zweiten Koordinationssphäre durch das Protein hervor.

Rolle in der mechanistischen anorganischen Chemie
Die Geschwindigkeit, mit der Liganden zwischen der ersten und der zweiten Koordinationssphäre ausgetauscht werden, ist der erste Schritt bei Ligandensubstitutionsreaktionen. Bei der assoziativen Ligandensubstitution befindet sich das eintretende Nucleophil in der zweiten Koordinationssphäre. Diese Effekte sind für praktische Anwendungen wie Kontrastmittel in der MRT relevant .
Die Energetik von Elektronentransferreaktionen in der inneren Sphäre wird im Hinblick auf die zweite Koordinationssphäre diskutiert. Einige protonengekoppelte Elektronentransferreaktionen beinhalten einen Atomtransfer zwischen den zweiten Koordinationssphären der Reaktanten:
- [Fe * (H 2 O) 6 ] 2+ + [Fe (H 2 O) 5 (OH)] 2+ → [Fe (H 2 O) 6 ] 3+ + [Fe * (H 2 O) 5 ( OH)] 2+
Rolle in der Spektroskopie
Lösungsmitteleffekte auf Farben und Stabilität sind häufig auf Veränderungen in der zweiten Koordinationssphäre zurückzuführen. Solche Effekte können in Komplexen ausgeprägt sein, in denen die Liganden in der ersten Koordinationssphäre starke Wasserstoffbrückenbindungsdonoren und -akzeptoren sind, z. B. [Co (NH 3 ) 6 ] 3+ bzw. [Fe (CN) 6 ] 3− . Kronenether binden über ihre zweite Koordinationssphäre an Polyaminkomplexe. Polyammoniumkationen binden an die Stickstoffzentren von Cyanometallaten.
Rolle in der supramolekularen Chemie
Makrocyclische Moleküle wie Cyclodextrine fungieren häufig als zweite Koordinationssphäre für Metallkomplexe.
Siehe auch
Weiterführende Literatur
Verweise
- ^ Zhao, Meng; Wang, Hai-Bo; Ji, Liang-Nian; Mao, Zong-Wan (2013). "Einblicke in Metalloenzym-Mikroumgebungen: biomimetische Metallkomplexe mit einer funktionellen zweiten Koordinationssphäre" . Bewertungen der Chemical Society . 42 (21): 8360. doi : 10.1039 / c3cs60162e . ISSN 0306-0012 .
- ^ Yang, JY; Chen, S.; Dougherty, WG; Kassel, WS; Bullock, RM; DuBois, DL; Raugei, S.; Rousseau, R.; Dupuis, M.; Rakowski DuBois, M. (2010). "Wasserstoffoxidationskatalyse durch einen Nickeldiphosphinkomplex mit anhängenden tert-Butylaminen". Chem. Kommun . 46 (45): 8618–8620. doi : 10.1039 / c0cc03246h . PMID 20938535 .
- ^ Bullock, RM; Helm, ML (2015). "Molekulare Elektrokatalysatoren zur Oxidation von Wasserstoff mit erdreichen Metallen: Protonenrelais mit Protonenrelais herumschieben" . Acc. Chem. Res . 48 (7): 2017–2026. doi : 10.1021 / acs.accounts.5b00069 . OSTI 1582563 . PMID 26079983 .
- ^ RM Supkowski, W. DeW. Horrocks Jr. "Zur Bestimmung der Anzahl der an Europium (III) -Ionen in Lösung koordinierten Wassermoleküle q aus Lumineszenzzerfallslebensdauern" Inorganic Chimica Acta 2002, Band 340, S. 44–48. doi : 10.1016 / S0020-1693 (02) 01022-8
- ^ Lehn, JM Supramolekulare Chemie: Konzepte und Perspektiven; VCH: Weinhiem, 1995.
- ^ Z. Liu, ST Schneebeli, JF Stoddart "Koordination der zweiten Sphäre überarbeitet" Chimia 2014, 68, 315-320. doi : 10.2533 / chimia.2014.315
- ^ Z. Liu, M. Frasconi, J. Lei, ZJ Brown, Z. Zhu, D. Cao, J. Iehl, G. Liu, AC Fahrenbach, OK Farha, JT Hupp, CA Mirkin, YY Botros, JF Stoddart " Selektive Isolierung von Gold durch Koordination der zweiten Sphäre mit Alpha-Cyclodextrin "Nature Communications 2013, 4, 1855. doi : 10.1038 / ncomms2891
