Ledipasvir - Ledipasvir
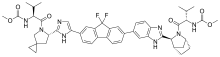 | |
| Klinische Daten | |
|---|---|
| Namen austauschen | Harvoni (Kombination mit Sofosbuvir ) |
| Andere Namen | GS-5885 |
| Lizenzdaten | |
| Wege Verwaltung |
Mit dem Mund |
| ATC-Code | |
| Rechtsstellung | |
| Rechtsstellung | |
| Pharmakokinetische Daten | |
| Bioverfügbarkeit | 76 % |
| Proteinbindung | >99 % |
| Stoffwechsel | Kein Cytochrom- Stoffwechsel |
| Beseitigung Halbwertszeit | 47 Stunden |
| Identifikatoren | |
| |
| CAS-Nummer | |
| PubChem- CID | |
| Arzneimittelbank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEBI | |
| CompTox-Dashboard ( EPA ) | |
| Chemische und physikalische Daten | |
| Formel | C 49 H 54 F 2 N 8 O 6 |
| Molmasse | 889.018 g·mol -1 |
| 3D-Modell ( JSmol ) | |
| |
| |
Ledipasvir ist ein Medikament zur Behandlung von Hepatitis C , das von Gilead Sciences entwickelt wurde . Nach Abschluss der klinischen Phase-III-Studien beantragte Gilead am 10. Februar 2014 die US-Zulassung einer Ledipasvir/Sofosbuvir -Fixkombinationstablette für Hepatitis C vom Genotyp 1. Die Ledipasvir/Sofosbuvir-Kombination ist ein direkt wirkendes antivirales Mittel, das die HCV-Replikation stört und kann zur Behandlung von Patienten mit Genotyp 1a oder 1b ohne PEG-Interferon oder Ribavirin verwendet werden .
Ledipasvir ist ein Inhibitor von NS5A , einem Protein des Hepatitis-C-Virus .
Daten präsentiert auf der 20. Konferenz über Retroviren und opportunistische Infektionen März 2013 zeigte , dass eine Dreifachtherapie des Nukleotids analogen Inhibitor Sofosbuvir, ledipasvir und Ribavirin produzierte eine 12-Wochen nach der Behandlung für beide virologischen Reaktion (SVR12) von 100% aufrechterhalten therapienaive Patienten und frühere Non-Responder mit HCV-Genotyp 1. Die Sofosbuvir/Ledipasvir-Koformulierung wird mit und ohne Ribavirin getestet. Im Februar 2014 beantragte Gilead die Zulassung der US-amerikanischen Food and Drug Administration (FDA) für die orale Behandlung mit Ledipasvir/Sofosbuvir ohne Interferon und Ribavirin.
Am 10. Oktober 2014 hat die FDA das Kombinationspräparat Ledipasvir/Sofosbuvir namens Harvoni zugelassen .
Medizinische Anwendungen
Ledipasvir wird am häufigsten in Kombination mit Sofosbuvir zur Behandlung von Patienten mit chronischer Hepatitis C Genotyp 1 angewendet. Dieses Medikament wurde bei behandlungsnaiven und behandlungserfahrenen Patienten getestet und zeigt seine Wirksamkeit.
Nebenwirkungen
Laut klinischen Studien wurde Ledipasvir/Sofosbuvir sehr gut vertragen, wobei die häufigsten Nebenwirkungen Müdigkeit und Kopfschmerzen sind.
Interaktionen
Die meisten Arzneimittelwechselwirkungen mit Harvoni beinhalten Pgp- Induktoren wie Johanniskraut oder Rifampicin . Die gleichzeitige Anwendung verringert die Blutkonzentration von Harvoni und hat somit eine verringerte therapeutische Wirkung.
Wirkmechanismus
Ledipasvir hemmt ein wichtiges virales Phosphoprotein, NS5A , das an der viralen Replikation, Assemblierung und Sekretion beteiligt ist.
Sofosbuvir, andererseits mit einem metabolisiert Uridin - Triphosphat mimic, die als wirkt RNA Kettenabbrecher , wenn sie in RNA inkorporiert durch NS5B - Polymerase.
Kosten
Ähnlich wie bei Sofosbuvir sind die Kosten von Harvoni ein umstrittenes Thema. Es kostet 1.125 US-Dollar pro Pille in den USA, was 63.000 US-Dollar für einen 8-wöchigen Behandlungskurs, 94.500 US-Dollar für einen 12-wöchigen Behandlungskurs oder 189.000 US-Dollar für einen 24-wöchigen Behandlungskurs entspricht. Gilead rechtfertigt die Kosten, indem es den Nutzen der Heilung von Hepatitis C gegenüber den doppelten Ausgaben für Lebertransplantationen oder die vorübergehende Behandlung von Lebererkrankungen aufwiegt. Gilead hat ein Ledipasvir/Sofosbuvir-Hilfsprogramm für berechtigte unterversorgte oder unterversicherte Hepatitis-C-Patienten bereitgestellt, die sich die Behandlungskosten nicht leisten können.
Im Juli 2015 änderte Gilead die Anspruchskriterien für den Bezug von Support Path-Leistungen für HCV-Patienten in den USA.
