Megakaryozyten - Megakaryocyte
| Megakaryozyten | |
|---|---|
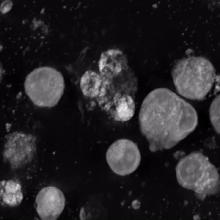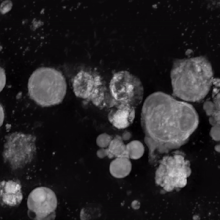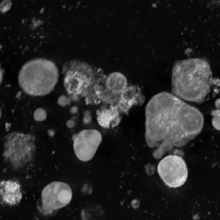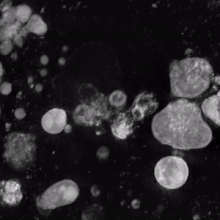
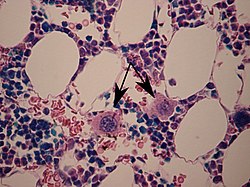 Zwei Megakaryozyten im Knochenmark, mit Pfeilen markiert.
| |
| Einzelheiten | |
| Standort | Knochenmark |
| Funktion | Platelet Produktion |
| Identifikatoren | |
| Latein | Megakaryozytur |
| Gittergewebe | D008533 |
| NS | H2.00.04.3.05003 |
| FMA | 83555 |
|
Anatomische Begriffe der Mikroanatomie | |
Ein Megakaryozyten ( Mega- + karyo- + -cyte , „large-Kern - Zelle“) ist eine großen Knochenmarkszellen mit einem gelappten Nucleus verantwortlich für die Produktion von Blut Thrombozyten ( Blutplättchen ), die für die normale Blut notwendig ist Blutgerinnung . Beim Menschen machen Megakaryozyten normalerweise 1 von 10.000 Knochenmarkszellen aus, können aber im Verlauf bestimmter Krankheiten ihre Zahl fast um das 10-fache erhöhen. Aufgrund von Variationen in der Kombination von Formen und Schreibweise umfassen Synonyme Megalokaryozyten und Megakaryozyten .
Struktur
Im Allgemeinen sind Megakaryozyten 10 bis 15 Mal größer als ein typisches rotes Blutkörperchen und haben einen durchschnittlichen Durchmesser von 50–100 μm. Während seiner Reifung wächst der Megakaryozyten an Größe und repliziert seine DNA ohne Zytokinese in einem Prozess namens Endomitose . Dadurch kann der Kern des Megakaryozyten sehr groß und gelappt werden, was unter dem Lichtmikroskop den falschen Eindruck erwecken kann, dass es sich um mehrere Kerne handelt. In einigen Fällen kann der Kern bis zu 64 N DNA oder 32 Kopien des normalen DNA-Komplements in einer menschlichen Zelle enthalten.
Das Zytoplasma enthält ebenso wie die daraus hervorgehenden Blutplättchen α-Granula und Dense Bodies .
Entwicklung
Megakaryozyten werden aus Vorläuferzellen von hämatopoetischen Stammzellen im Knochenmark gewonnen. Sie werden hauptsächlich von Leber, Niere, Milz und Knochenmark produziert. Diese multipotenten Stammzellen leben in den Knochenmarksinusoiden und sind in der Lage, je nach Signal, das sie erhalten, alle Arten von Blutzellen zu produzieren. Das primäre Signal für die Megakaryozytenproduktion ist Thrombopoietin oder TPO. TPO ist ausreichend, aber nicht unbedingt notwendig, um die Differenzierung von Vorläuferzellen im Knochenmark zu einem endgültigen Megakaryozyten- Phänotyp zu induzieren . Andere molekulare Signale für die Megakaryozytendifferenzierung umfassen GM-CSF , IL-3 , IL-6 , IL-11 , Chemokine ( SDF-1 , FGF-4 ). und Erythropoietin . Der Megakaryozyten entwickelt sich durch die folgende Abstammungslinie:
CFU-Me ( pluripotente hämatopoetische Stammzelle oder Hämozytoblast) → Megakaryoblast → Promegakaryozyten → Megakaryozyten.
Die Zelle erreicht schließlich das Megakaryozyten-Stadium und verliert ihre Fähigkeit, sich zu teilen. Es ist jedoch immer noch in der Lage, seine DNA zu replizieren und sich weiterzuentwickeln, wodurch es polyploid wird . Das Zytoplasma dehnt sich weiter aus und die DNA-Menge kann beim Menschen bis auf 64n und bei Mäusen auf 256n ansteigen. Viele der morphologischen Merkmale der Megakaryozyten-Differenzierung können in nicht-hämatopoetischen Zellen durch die Expression von Klasse-VI-β-Tubulin (β6) rekapituliert werden und bieten eine mechanistische Grundlage für das Verständnis dieser Veränderungen.
Funktion
Thrombozytenfreisetzung
Sobald die Zelle die Differenzierung abgeschlossen und zu einem reifen Megakaryozyten geworden ist, beginnt sie mit der Produktion von Blutplättchen. Der Reifungsprozess erfolgt über endomitotische synchrone Replikation, wobei sich das Zytoplasmavolumen mit der Vermehrung der Chromosomen ohne Zellteilung vergrößert. Die Zelle hört bei 4N, 8N oder 16N auf zu wachsen, wird körnig und beginnt, Blutplättchen zu produzieren. Thrombopoietin spielt eine Rolle bei der Induktion der Megakaryozyten, um kleine Proto-Blutplättchen-Prozesse zu bilden. Thrombozyten werden innerhalb dieser inneren Membranen im Zytoplasma von Megakaryozyten gehalten. Es gibt zwei vorgeschlagene Mechanismen für die Freisetzung von Blutplättchen. In einem Szenario brechen diese Proto-Blutplättchen-Prozesse explosionsartig auf, um Blutplättchen zu werden. Es ist möglich , die spontane Freisetzung von Thrombozyten mit Hilfe der holotomographischen Bildgebung lebender Zellen zu visualisieren . Alternativ kann die Zelle Blutplättchenbänder zu Blutgefäßen bilden. Die Bänder werden über Pseudopodien gebildet und sind in der Lage, kontinuierlich Blutplättchen in den Kreislauf abzugeben. In jedem Szenario kann jeder dieser Proto-Blutplättchen-Prozesse beim Aufbrechen 2000–5000 neue Blutplättchen erzeugen. Insgesamt bleiben 2/3 dieser neu produzierten Blutplättchen im Umlauf, während 1/3 von der Milz sequestriert werden.
Thrombopoietin (TPO) ist ein 353-Aminosäuren-Protein, das auf Chromosom 3p 27 kodiert ist . TPO wird hauptsächlich in der Leber synthetisiert, kann aber von Nieren, Hoden, Gehirn und sogar Knochenmarksstromazellen hergestellt werden. Es weist eine hohe Homologie mit Erythropoietin auf . Es ist wichtig für die Bildung einer ausreichenden Menge an Blutplättchen.
Nach dem Ausknospen der Thrombozyten bleibt hauptsächlich der Zellkern übrig. Dieses passiert die Knochenmarkbarriere zum Blut und wird in der Lunge von alveolären Makrophagen aufgenommen .
Wirkungen von Zytokinen
Zytokine sind Signale, die im Immunsystem für die interzelluläre Kommunikation verwendet werden. Es gibt viele Zytokine , die Megakaryozyten beeinflussen. Bestimmte Zytokine wie IL-3 , IL-6 , IL-11 , LIF , Erythropoietin und Thrombopoietin stimulieren alle die Reifung von megakaryozytischen Vorläuferzellen. Andere Signale wie PF4 , CXCL5 , CXCL7 und CCL5 hemmen die Blutplättchenbildung.
Klinische Bedeutung
Megakaryozyten sind direkt für die Produktion von Blutplättchen verantwortlich, die für die Bildung eines Thrombus oder Blutgerinnsels benötigt werden. Es gibt mehrere Krankheiten, die direkt auf eine abnormale Megakaryozytenfunktion oder eine abnormale Thrombozytenfunktion zurückzuführen sind.
Essentielle Thrombozytose
Essentielle Thrombozytose (ET), auch als essentielle Thrombozythämie bekannt , ist eine Erkrankung, die durch eine erhöhte Anzahl zirkulierender Blutplättchen gekennzeichnet ist. Die Krankheit tritt bei 1–2 pro 100.000 Menschen auf. Die WHO-Anforderungen für die Diagnose von 2016 umfassen > 450.000 Thrombozyten/μl Blut (normal 150.000–400.000) und eine Knochenmarkbiopsie . Einige der Folgen einer so hohen Anzahl von Blutplättchen sind Thrombosen oder Gerinnsel im ganzen Körper. Thromben bilden sich häufiger in Arterien als in Venen. Es erscheint ironisch, dass eine Thrombozytenzahl über 1.000.000 Thrombozyten/μl zu hämorrhagischen Ereignissen führen kann. Jüngste Hinweise deuten darauf hin, dass die Mehrheit der ET-Fälle auf eine Mutation im JAK2- Protein zurückzuführen ist, einem Mitglied des JAK-STAT-Signalwegs . Es gibt Hinweise darauf, dass diese Mutation die Megakaryozyten überempfindlich gegenüber Thrombopoietin macht und eine klonale Proliferation von Megakaryozyten verursacht. Bei dieser Erkrankung besteht ein erhebliches Risiko einer Transformation in Leukämie . Die primäre Behandlung besteht in Anagrelid oder Hydroxyharnstoff , um die Thrombozytenwerte zu senken.
Angeborene amegakaryozytäre Thrombozytopenie
Die angeborene amegakaryozytäre Thrombozytopenie (CAMT) ist eine seltene Erbkrankheit . Die primären Manifestationen sind Thrombozytopenie und Megakaryozytopenie, dh geringe Anzahl von Thrombozyten und Megakaryozyten. Im Knochenmark fehlen Megakaryozyten ohne damit verbundene körperliche Anomalien. Die Ursache für diese Störung scheint trotz hoher Serum-TPO-Spiegel eine Mutation im Gen für den TPO-Rezeptor, c-mpl , zu sein. Darüber hinaus kann es zu Anomalien des zentralen Nervensystems einschließlich des Groß- und Kleinhirns kommen , die Symptome verursachen können. Die primäre Behandlung der CAMT ist die Knochenmarktransplantation .
Eine Knochenmark-/Stammzelltransplantation ist das einzige Heilmittel für diese genetische Erkrankung. Häufige Blutplättchentransfusionen sind erforderlich, um zu verhindern, dass der Patient verblutet, bis die Transplantation abgeschlossen ist, obwohl dies nicht immer der Fall ist.
Es scheint keine generische Ressource für CAMT-Patienten im Internet zu geben, was möglicherweise auf die Seltenheit der Krankheit zurückzuführen ist.
Geschichte
1906 lieferte James Homer Wright den Beweis, dass Megakaryozyten Blutplättchen bilden.
Kelemen prägte zuerst den Begriff „ Thrombopoietin “, um die humorale Substanz zu beschreiben, die für die Produktion von Blutplättchen verantwortlich ist.
Verweise
Externe Links
- Megakaryozyten: Reife Viele mikroskopische Bilder von reifen Megakaryozyten, auch in Krankheitssituationen.
- Megakaryozyten
- Vergleich der Zellgröße
- CAMT-spezifisches Journal für Knochenmarktransplantationen bei Säuglingen

