Metallocen - Metallocene
Ein Metallocen ist eine Verbindung, die typischerweise aus zwei Cyclopentadienylanionen ( C
5h−
5, abgekürzt Cp) an ein Metallzentrum (M) in der Oxidationsstufe II gebunden , mit der resultierenden allgemeinen Formel (C 5 H 5 ) 2 M. Eng verwandt mit den Metallocenen sind die Metallocen-Derivate, zB Titanocendichlorid , Vanadocendichlorid . Bestimmte Metallocene und ihre Derivate weisen katalytische Eigenschaften auf, obwohl Metallocene selten industriell verwendet werden. Mit [Cp 2 ZrCH 3 ] + verwandte kationische Gruppe-4-Metallocenderivate katalysieren die Olefinpolymerisation .
Einige Metallocene bestehen aus Metall plus zwei Cyclooctatetraenidanionen ( C
8h2−
8, abgekürzt cot 2− ), nämlich die Lanthanocene und die Actinocene ( Uranocene und andere).
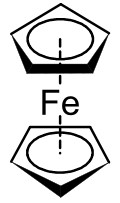
Metallocene sind eine Untergruppe einer breiteren Klasse von Verbindungen, die als Sandwich-Verbindungen bezeichnet werden . In der rechts gezeigten Struktur sind die beiden Fünfecke die Cyclopentadienylanionen mit Kreisen darin, die darauf hinweisen, dass sie aromatisch stabilisiert sind. Hier sind sie in einer gestaffelten Konformation dargestellt .
Geschichte
Das erste klassifizierte Metallocen war Ferrocen und wurde 1951 gleichzeitig von Kealy und Pauson sowie Miller et al. entdeckt. Kealy und Pauson wurden zum Synthetisieren versuchen Fulvalen durch die Oxidation eines cyclopentadienyl Salzes mit wasserfreiem FeCl 3 , sondern der Substanz C erhaltenen 10 H 10 Fe Zur gleichen Zeit, Miller et al berichtete das gleiche Eisenprodukt aus einer Reaktion von Cyclopentadien mit Eisen in das Vorhandensein von Aluminium-, Kalium- oder Molybdänoxiden. Die Struktur von "C 10 H 10 Fe" wurde von Geoffrey Wilkinson et al. und von Ernst Otto Fischer et al. Diese beiden erhielten 1973 den Nobelpreis für Chemie für ihre Arbeiten zu Sandwich-Verbindungen, einschließlich der Strukturaufklärung von Ferrocen. Sie stellten fest, dass die Kohlenstoffatome des Cyclopentadienyl(Cp) -Liganden gleichermaßen zur Bindung beitragen und dass die Bindung durch die Metall- d-Orbitale und die π- Elektronen in den p-Orbitalen der Cp-Liganden erfolgt. Dieser Komplex ist heute als Ferrocen bekannt, und die Gruppe der Übergangsmetall- Dicyclopentadienyl-Verbindungen ist als Metallocene bekannt. Metallocene haben die allgemeine Formel [( η 5 -C 5 H 5 ) 2 M]. Fischeret al. stellten zunächst die Ferrocenderivate mit Co und Ni her. Oft von substituierten Cyclopentadienid- Derivaten abgeleitet , wurden Metallocene vieler Elemente hergestellt.
Einer der ersten kommerziellen Hersteller von Metallocenen war Arapahoe Chemicals in Boulder, Colorado
Definition

Der allgemeine Name Metallocen leitet sich von Ferrocen , (C 5 H 5 ) 2 Fe oder Cp 2 Fe ab, das systematisch als Bis( η 5 - cyclopentadienyl )eisen(II) bezeichnet wird. Gemäß der Definition der International Union of Pure and Applied Chemistry enthält ein Metallocen ein Übergangsmetall und zwei Cyclopentadienylliganden, die in einer Sandwichstruktur koordiniert sind, dh die beiden Cyclopentadienyl-Anionen liegen auf parallelen Ebenen mit gleichen Bindungslängen und -stärken. Unter Verwendung der Nomenklatur der „ Haptizität “, die äquivalente Bindung aller 5 Kohlenstoffatomen eines Cyclopentadienylring ist bezeichnet als η 5 , ausgesprochen „pentahapto“. Es gibt Ausnahmen, wie zum Beispiel Uranocen , das zwei Cyclooctatetraen- Ringe aufweist, die ein Uranatom einschließen.
In Metallocennamen gibt das Präfix vor der -ocen- Endung an, welches metallische Element zwischen den Cp-Gruppen ist. Beispielsweise liegt in Ferrocen, Eisen(II), Eisen(II) vor.
Im Gegensatz zur strengeren Definition der International Union of Pure and Applied Chemistry, die ein d-Block-Metall und eine Sandwich-Struktur erfordert, wird der Begriff Metallocen und damit die Bezeichnung -Ocen in der chemischen Literatur auch für Nicht-Übergänge verwendet Metallverbindungen wie Barocen (Cp 2 Ba) oder Strukturen, bei denen die aromatischen Ringe nicht parallel sind, wie sie in Manganocen oder Titanocendichlorid (Cp 2 TiCl 2 ) gefunden werden.
Es wurden einige Metallocenkomplexe von Actiniden beschrieben , bei denen es drei Cyclopentadienylliganden für einen monometallischen Komplex gibt, von denen alle drei an η 5 gebunden sind .
Einstufung
Es gibt viele ( η 5 -C 5 H 5 )-Metallkomplexe und sie können nach den folgenden Formeln klassifiziert werden:
| Formel | Beschreibung |
|---|---|
| [( η 5 -C 5 H 5 ) 2 M] | Symmetrische, klassische „Sandwich“-Struktur |
| [( η 5 -C 5 H 5 ) 2 ml x ] | Gebogene oder geneigte Cp-Ringe mit zusätzlichen Liganden, L |
| [( η 5 -C 5 H 5 )ML x ] | Nur ein Cp-Ligand mit zusätzlichen Liganden, L ('Klavierstuhl'-Struktur) |
Metallocenkomplexe können auch nach Typ klassifiziert werden:
- Parallel
- Mehrdecker
- Halb-Sandwich-Compound
- Metallocen gebogen oder gekippt
- Mehr als zwei Cp-Liganden
Synthese
Bei der Bildung dieser Arten von Verbindungen werden normalerweise drei Hauptwege verwendet:
Verwendung eines Metallsalzes und Cyclopentadienyl-Reagenzien
Natriumcyclopentadienid (NaCp) ist das bevorzugte Reagens für diese Reaktionstypen. Es wird am einfachsten durch die Reaktion von geschmolzenem Natrium und Dicyclopentadien erhalten. Ausgangspunkt ist traditionell das Cracken von Dicyclopentadien , dem Dimer von Cyclopentadien. Cyclopentadien wird durch starke Basen oder Alkalimetalle deprotoniert.
- MCl 2 + 2 NaC 5 H 5 → (C 5 H 5 ) 2 M + 2 NaCl (M = V, Cr, Mn, Fe, Co; Lösungsmittel = THF, DME, NH 3 )
- CrCl 3 + 3 NaC 5 H 5 → [(C 5 H 5 ) 2 Cr] + 1 ⁄ 2 "C 10 H 10 " + 3 NaCl
NaCp wirkt bei dieser Reaktion als Reduktionsmittel und Ligand.
Mit einem Metall und Cyclopentadien
Diese Technik sieht die Verwendung von Metallatomen in der Gasphase anstelle des festen Metalls vor. Die hochreaktiven Atome oder Moleküle werden bei hoher Temperatur im Vakuum erzeugt und mit ausgewählten Reaktanten auf einer kalten Oberfläche zusammengebracht.
- M + C 5 H 6 → MC 5 H 5 + 1 ⁄ 2 H 2 (M = Li, Na, K)
- M + 2 C 5 H 6 → [(C 5 H 5 ) 2 M] + H 2 (M = Mg, Fe)
Verwendung von Cyclopentadienyl-Reagenzien
Es wurde eine Vielzahl von Reagenzien entwickelt, die Cp auf Metalle übertragen. Einst beliebt war Thalliumcyclopentadienid . Es reagiert mit Metallhalogeniden zum schwerlöslichen Thalliumchlorid und zum Cyclopentadienylkomplex . Trialkyl - Zinn - Derivate von Cp - wird ebenfalls verwendet.
Viele andere Methoden wurden entwickelt. Chromocen kann aus Chromhexacarbonyl durch direkte Reaktion mit Cyclopentadien in Gegenwart von Diethylamin hergestellt werden ; in diesem Fall folgt auf die formale Deprotonierung des Cyclopentadiens die Reduktion der resultierenden Protonen zu Wasserstoffgas , was die Oxidation des Metallzentrums erleichtert .
- Cr(CO) 6 + 2 C 5 H 6 → Cr(C 5 H 5 ) 2 + 6 CO + H 2
Metallocene weisen im Allgemeinen eine hohe thermische Stabilität auf. Ferrocen kann an der Luft bei über 100 °C ohne Zersetzung sublimiert werden; Metallocene werden im Labor durch Vakuum allgemeine gereinigt Sublimation . Industriell ist Sublimation nicht praktikabel, daher werden Metallocene durch Kristallisation isoliert oder als Teil einer Kohlenwasserstofflösung hergestellt. Für Metallocene der Gruppe IV sind Donorlösungsmittel wie Ether oder THF für die Polyolefinkatalyse deutlich unerwünscht. Ladungsneutrale Metallocene sind in gängigen organischen Lösungsmitteln löslich. Die Alkylsubstitution am Metallocen erhöht die Löslichkeit in Kohlenwasserstofflösungsmitteln.
Struktur
Ein struktureller Trend für die Reihe MCp 2 betrifft die Variation der MC-Bindungen, die sich verlängern, wenn die Valenzelektronenzahl von 18 abweicht.
| M(C 5 H 5 ) 2 | r M–C (pm) | Valenzelektronenzahl |
|---|---|---|
| Fe | 203,3 | 18 |
| Co | 209,6 | 19 |
| Cr | 215.1 | 16 |
| Ni | 218,5 | 20 |
| V | 226 | fünfzehn |
In Metallocenen des Typs (C 5 R 5 ) 2 M rotieren die Cyclopentadienylringe mit sehr geringen Barrieren. Einkristall -Röntgenbeugungsstudien zeigen sowohl verfinsterte als auch versetzte Rotamere. Bei nicht substituierten Metallocenen beträgt der Energieunterschied zwischen der gestaffelten und der ekliptischen Konformation nur wenige kJ/mol . Kristalle von Ferrocen und Osmocen zeigen bei niedrigen Temperaturen ekliptische Konformationen, während in den verwandten Bis(pentamethylcyclopentadienyl)-Komplexen die Ringe normalerweise in einer versetzten Konformation kristallisieren, anscheinend um die sterische Hinderung zwischen den Methylgruppen zu minimieren .
Spektroskopische Eigenschaften
Schwingungsspektroskopie (Infrarot und Raman) von Metallocenen
Infrarot- und Raman- Spektroskopie haben sich bei der Analyse cyclischer Polyenylmetall-Sandwichspezies als wichtig erwiesen, insbesondere bei der Aufklärung kovalenter oder ionischer M-Ring-Bindungen und der Unterscheidung zwischen zentralen und koordinierten Ringen. Einige typische Spektralbänder und Zuordnungen von Metallocenen der Eisengruppe sind in der folgenden Tabelle aufgeführt:
| Ferrocen (cm −1 ) | Ruthenozän (cm −1 ) | Osmocen (cm −1 ) | |
|---|---|---|---|
| C–H-Streckung | 3085 | 3100 | 3095 |
| C–C-Streckung | 1411 | 1413 | 1405 |
| Ringverformung | 1108 | 1103 | 1096 |
| C–H-Verformung | 1002 | 1002 | 995 |
| C–H Biegung außerhalb der Ebene | 811 | 806 | 819 |
| Ringneigung | 492 | 528 | 428 |
| M–Ringdehnung | 478 | 446 | 353 |
| M–Ringbogen | 170 | 185 | – |
NMR ( 1 H und 13 C) Spektroskopie von Metallocenen
Kernspinresonanz (NMR) ist das am häufigsten verwendete Werkzeug bei der Untersuchung von Metall-Sandwich-Verbindungen und metallorganischen Spezies und liefert Informationen über Kernstrukturen in Lösung, als Flüssigkeiten, Gase und im Festkörper. 1 H-NMR-chemische Verschiebungen für paramagnetische Organoübergangsmetallverbindungen werden normalerweise zwischen 25 und 40 ppm beobachtet, aber dieser Bereich ist für diamagnetische Metallocenkomplexe viel enger, wobei chemische Verschiebungen normalerweise zwischen 3 und 7 ppm beobachtet werden.
Massenspektrometrie von Metallocenen
Die Massenspektrometrie von Metallocenkomplexen wurde sehr gut untersucht und der Einfluss des Metalls auf die Fragmentierung der organischen Einheit hat beträchtliche Aufmerksamkeit erregt, und die Identifizierung metallhaltiger Fragmente wird oft durch die Isotopenverteilung des Metalls erleichtert . Die drei Hauptfragmente, die in der Massenspektrometrie beobachtet werden, sind der Molekülionenpeak [C 10 H 10 M] + und die Fragmentionen [C 5 H 5 M] + und M + .
Derivate
Nach der Entdeckung des Ferrocens weckte die Synthese und Charakterisierung von Derivaten des Metallocens und anderer Sandwich-Verbindungen das Interesse der Forscher.
Metallocenophane
Metallocenophane zeichnen sich durch die Verknüpfung der Cyclopentadienyl- oder Polyarenylringe durch die Einführung einer oder mehrerer heteroringförmiger Brücken aus. Einige dieser Verbindungen unterliegen thermischen Ringöffnungspolymerisationen , um lösliche Polymere mit hohem Molekulargewicht mit Übergangsmetallen in der Polymerhauptkette zu ergeben. Ansa-Metallocene sind Derivate von Metallocenen mit einer intramolekularen Brücke zwischen den beiden Cyclopentadienylringen.
Mehrkernige und heterobimetallische Metallocene
- Ferrocenderivate: biferrocenophanes wurde für ihre gemischten studierte Valenz Eigenschaften. Bei der Ein-Elektronen-Oxidation einer Verbindung mit zwei oder mehr äquivalenten Ferrocen-Einheiten könnte die Elektronenfehlstelle auf einer Ferrocen-Einheit lokalisiert oder vollständig delokalisiert werden .
- Ruthenocen- Derivate: Im Festkörper ist Biruthenocen fehlgeordnet und nimmt die transoide Konformation mit der gegenseitigen Orientierung der Cp-Ringe in Abhängigkeit von den intermolekularen Wechselwirkungen an.
- Vanadocen- und Rhodocen- Derivate: Vanadocen-Komplexe wurden als Ausgangsmaterialien für die Synthese heterobimetallischer Komplexe verwendet. Die 18 Valenzelektronen- Ionen [Cp 2 Rh] + sind sehr stabil, im Gegensatz zu den neutralen Monomeren Cp 2 Rh, die bei Raumtemperatur sofort dimerisieren und bei der Matrixisolation beobachtet wurden .
Multidecker-Sandwich-Compounds
Tripeldeckerkomplexe bestehen aus drei Cp-Anionen und zwei Metallkationen in alternierender Reihenfolge. Der erste Triple-Decker-Sandwich-Komplex, [Ni
2Cp
3] + , wurde 1972 beschrieben. Später wurden viele Beispiele beschrieben, oft mit borhaltigen Ringen .
Metallocenium-Kationen
Das bekannteste Beispiel ist Ferrocenium , [Fe(C
5h
5)
2] + , der blaue Eisen(III)-Komplex, der aus der Oxidation von orangefarbenem Eisen(II)-Ferrocen stammt (wenige Metallocen-Anionen sind bekannt).
Anwendungen
Viele Derivate früher Metallocene sind aktive Katalysatoren für die Olefinpolymerisation . Im Gegensatz zu herkömmlichen und immer noch dominierenden heterogenen Ziegler-Natta- Katalysatoren sind Metallocenkatalysatoren homogen. Frühe Metall-Metallocen-Derivate, zB Tebbe's Reagens , Petasis 's Reagens und Schwartz's Reagens, sind in speziellen organischen Syntheseverfahren nützlich.
Anwendungsmöglichkeiten
Der Ferrocen/ Ferrocenium- Biosensor wurde zur elektrochemischen Bestimmung des Glucosespiegels in einer Probe durch eine Reihe verbundener Redoxzyklen diskutiert .
Metallocendihalogenide [Cp 2 MX 2 ] (M = Ti, Mo, Nb) weisen Antitumoreigenschaften auf, obwohl keine in klinischen Studien weit fortgeschritten ist.
Siehe auch
Verweise
Weitere Referenzen
- Salzer, A. (1999). "Nomenklatur der metallorganischen Verbindungen der Übergangselemente" . Reine Appl. Chem.-Nr. 71 (8): 1557–1585. doi : 10.1351/pac199971081557 . S2CID 14367196 . Archiviert vom Original am 16.07.2007.
- Crabtree, Robert H. (2005). Die metallorganische Chemie der Übergangsmetalle (4. Aufl.). Wiley-Interscience.ISBN 0470257628
- Mießler, Gary L.; Tarr, Donald A. (2004). Anorganische Chemie . Upper Saddle River, NJ: Pearson Education. ISBN 978-0-13-035471-6.
- Baumwolle, FA ; Wilkinson, G. (1988). Anorganische Chemie (5. Aufl.). Wiley. S. 626–7.
- Togni, A.; Haltermann, RL (1998). Metallocene . Wiley-VCH.