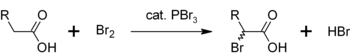Phosphortribromid - Phosphorus tribromide

|
|

|
|

|
|
| Namen | |
|---|---|
|
IUPAC-Name
Phosphortribromid
|
|
| Andere Namen
Phosphor(III)-bromid,
Phosphorbromid, Tribromphosphin |
|
| Bezeichner | |
|
3D-Modell ( JSmol )
|
|
| ChemSpider | |
| ECHA-Infokarte |
100.029.253 |
| EG-Nummer | |
|
PubChem- CID
|
|
| RTECS-Nummer | |
| UNII | |
|
CompTox-Dashboard ( EPA )
|
|
|
|
|
|
| Eigenschaften | |
| PBr 3 | |
| Molmasse | 270,69 g/mol |
| Aussehen | klare, farblose Flüssigkeit |
| Dichte | 2.852 g / cm 3 |
| Schmelzpunkt | −41,5 °C (−42,7 °F; 231,7 K) |
| Siedepunkt | 173,2 °C (343,8 °F; 446,3 K) |
| schnelle Hydrolyse | |
|
Brechungsindex ( n D )
|
1,697 |
| Viskosität | 0,001302 Pa |
| Struktur | |
| trigonal pyramidenförmig | |
| Gefahren | |
| Sicherheitsdatenblatt | Siehe: Datenseite |
|
EU-Klassifizierung (DSD) (veraltet)
|
|
| R-Sätze (veraltet) | R14 , R34 , R37 |
| S-Sätze (veraltet) | (S1/2) , S26 , S45 |
| NFPA 704 (Feuerdiamant) | |
| Verwandte Verbindungen | |
|
Andere Anionen
|
Phosphortrifluorid Phosphortrichlorid Phosphortriiodid |
|
Andere Kationen
|
Stickstofftribromid Arsentribromid Antimontribromid |
|
Verwandte Verbindungen
|
Phosphorpentabromid Phosphoroxybromid |
| Ergänzende Datenseite | |
|
Brechungsindex ( n ), Dielektrizitätskonstante (ε r ) usw. |
|
|
Thermodynamische
Daten |
Phasenverhalten fest-flüssig-gas |
| UV , IR , NMR , MS | |
|
Sofern nicht anders angegeben, beziehen sich die Daten auf Materialien im Standardzustand (bei 25 °C [77 °F], 100 kPa). |
|
|
|
|
| Infobox-Referenzen | |
Phosphortribromid ist eine farblose Flüssigkeit mit der Formel P Br 3 . Die Flüssigkeit dampft an feuchter Luft durch Hydrolyse und hat einen penetranten Geruch. Es wird im Labor zur Umwandlung von Alkoholen in Alkylbromide verwendet .
Vorbereitung
PBr 3 wird durch Behandeln von rotem Phosphor mit Brom hergestellt . Ein Überschuss an Phosphor wird verwendet, um die Bildung von PBr 5 zu verhindern :
- 2 P + 3 Br 2 → 2 PBr 3
Da die Reaktion stark exotherm ist, wird sie oft in Gegenwart eines Verdünnungsmittels wie PBr 3 durchgeführt .
Reaktionen
Phosphortribromid hat wie PCl 3 und PF 3 sowohl die Eigenschaften einer Lewis-Base als auch einer Lewis-Säure . Mit einer Lewis-Säure wie Bortribromid bildet es beispielsweise stabile 1:1-Addukte wie Br 3 B · PBr 3 . Gleichzeitig kann PBr 3 in vielen seiner Reaktionen, beispielsweise mit Aminen, als Elektrophil oder Lewis-Säure reagieren .
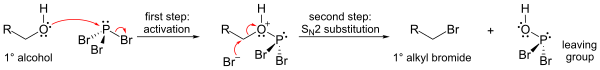
Die wichtigste Reaktion von PBr 3 ist mit Alkoholen , wo es eine OH- Gruppe durch ein Bromatom ersetzt, um ein Alkylbromid zu erzeugen . Alle drei Bromide können übertragen werden.
- PBr 3 + 3 ROH → 3 RBr + HP(O)(OH) 2
Der Mechanismus (für einen primären Alkohol gezeigt) beinhaltet die Bildung eines Phosphoresters (um eine gute Abgangsgruppe zu bilden), gefolgt von einer S N 2 -Substitution .
Aufgrund des S N 2 -Substitutionsschritts funktioniert die Reaktion im Allgemeinen gut für primäre und sekundäre Alkohole , scheitert jedoch für tertiäre Alkohole. Wenn das reagierende Kohlenstoffzentrum chiral ist , erfolgt die Reaktion gewöhnlich unter Inversion der Konfiguration am Alpha-Kohlenstoff des Alkohols , wie es bei einer S N 2 -Reaktion üblich ist.
In einer ähnlichen Reaktion wandelt PBr 3 auch Carbonsäuren in Acylbromide um .
- PBr 3 + 3 RCOOH → 3 RCOBr + HP(O)(OH) 2
Anwendungen
Die Hauptverwendung von Phosphortribromid ist die Umwandlung von primären oder sekundären Alkoholen in Alkylbromide , wie oben beschrieben . PBr 3 liefert normalerweise höhere Ausbeuten als Bromwasserstoffsäure und vermeidet Probleme der Carbokation- Umlagerung – zum Beispiel kann sogar Neopentylbromid aus dem Alkohol in 60% Ausbeute hergestellt werden.
Eine weitere Verwendung für PBr 3 ist als Katalysator für die α-Bromierung von Carbonsäuren . Obwohl Acylbromide selten im Vergleich zu Acylchloriden hergestellt werden , werden sie als Zwischenprodukte bei der Hell-Volhard-Zelinsky-Halogenierung verwendet . Zunächst reagiert PBr 3 mit der Carbonsäure zum Acylbromid, das gegenüber der Bromierung reaktiver ist. Der Gesamtprozess lässt sich darstellen als
Im kommerziellen Maßstab wird Phosphortribromid bei der Herstellung von Pharmazeutika wie Alprazolam , Methohexital und Fenoprofen verwendet . Es ist auch ein starkes Feuerlöschmittel, das unter dem Namen PhostrEx vermarktet wird .
Vorsichtsmaßnahmen
PBr 3 entwickelt ätzendes HBr, das giftig ist und heftig mit Wasser und Alkoholen reagiert.
- PBr 3 + 3 H 2 O → H 3 PO 3 + 3 HBr
Bei Reaktionen, bei denen als Nebenprodukt phosphorige Säure entsteht , ist bei der destillativen Aufarbeitung zu beachten, dass sich diese oberhalb von ca. 160 °C zu Phosphin zersetzen kann, das in Kontakt mit Luft Explosionen verursachen kann.
Verweise
Weiterlesen
- Greenwood, Norman N .; Earnshaw, Alan (1997). Chemie der Elemente (2. Aufl.). Butterworth-Heinemann . ISBN 978-0-08-037941-8.
- Lide, DR, hrsg. (1990). Handbuch der Chemie und Physik (71. Aufl.). Ann Arbor, MI: CRC-Presse. ISBN 978-0849304712.
- März, J. (1992). Fortgeschrittene organische Chemie (4. Aufl.). New York: Wiley. s. 723 . ISBN 978-0471601807.
- Stecher, PG, hrsg. (1960). Der Merck-Index (7. Aufl.). Rahway, NJ, USA: Merck & Co.
- Holmes, RR (1960). „Eine Untersuchung der grundlegenden Natur der Trihalogenide von Phosphor, Arsen und Antimon“. Zeitschrift für Anorganische und Nuklearchemie . 12 (3–4): 266–275. doi : 10.1016/0022-1902(60)80372-7 .