Natriumperoxid - Sodium peroxide

|
|
|
|

|
|
| Namen | |
|---|---|
| Andere Namen
Dinatriumdioxid
Flocool Solozone Dinatriumperoxid |
|
| Bezeichner | |
|
3D-Modell ( JSmol )
|
|
| ChemSpider | |
| ECHA-InfoCard |
100.013.828 |
| EG-Nummer | |
|
PubChem- CID
|
|
| RTECS-Nummer | |
| UNII | |
| UN-Nummer | 1504 |
|
CompTox-Dashboard ( EPA )
|
|
|
|
|
|
| Eigenschaften | |
| Na 2 O 2 | |
| Molmasse | 77,98 g/mol |
| Aussehen | gelbes bis weißes Pulver |
| Dichte | 2,805 g / cm 3 |
| Schmelzpunkt | 460 °C (860 °F; 733 K) (zersetzt) |
| Siedepunkt | 657 °C (1.215 °F; 930 K) (zersetzt) |
| reagiert heftig | |
| Löslichkeit | löslich in Säure unlöslich in Base reagiert mit Ethanol |
| −28,10·10 −6 cm 3 /mol | |
| Struktur | |
| sechseckig | |
| Thermochemie | |
|
Wärmekapazität ( C )
|
89,37 J/(mol·K) |
|
Std molare
Entropie ( S |
95 J/(Mol·K) |
|
Std
Bildungsenthalpie (Δ f H ⦵ 298 ) |
−515 kJ·mol −1 |
|
Gibbs freie Energie (Δ f G ˚)
|
−446.9 kJ/mol |
| Gefahren | |
| Sicherheitsdatenblatt | Externes Sicherheitsdatenblatt |
|
EU-Klassifizierung (DSD) (veraltet)
|
|
| R-Sätze (veraltet) | R8 , R35 |
| S-Sätze (veraltet) | (S1/2) , S8 , S27 , S39 , S45 |
| NFPA 704 (Feuerdiamant) | |
| Flammpunkt | Nicht brennbar |
| Verwandte Verbindungen | |
|
Andere Kationen
|
Lithiumperoxid Kaliumperoxid Rubidiumperoxid Cäsiumperoxid |
|
Natriumoxid Natriumsuperoxid |
|
|
Verwandte Verbindungen
|
Natriumhydroxid Wasserstoffperoxid |
|
Sofern nicht anders angegeben, beziehen sich die Daten auf Materialien im Standardzustand (bei 25 °C [77 °F], 100 kPa). |
|
|
|
|
| Infobox-Referenzen | |
Natriumperoxid ist die anorganische Verbindung mit der Formel Na 2 O 2 . Dieser gelbliche Feststoff ist das Produkt von Natrium, das in überschüssigem Sauerstoff entzündet wird. Es ist eine starke Basis. Dieses Metallperoxid existiert in mehreren Hydraten und Peroxyhydraten, einschließlich Na 2 O 2 ·2H 2 O 2 ·4H 2 O, Na 2 O 2 ·2H 2 O, Na 2 O 2 ·2H 2 O 2 und Na 2 O 2 ·8H 2 O. Das einfach herzustellende Octahydrat ist im Gegensatz zum wasserfreien Material weiß.
Eigenschaften
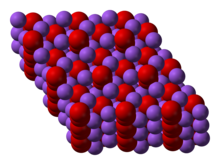
Natriumperoxid kristallisiert mit hexagonaler Symmetrie. Beim Erhitzen geht die hexagonale Form bei 512 °C in eine Phase unbekannter Symmetrie über. Bei weiterem Erhitzen über den Siedepunkt von 657 °C zersetzt sich die Verbindung zu Na 2 O, wobei O 2 freigesetzt wird .
- 2 Na 2 O 2 → 2 Na 2 O + O 2
Vorbereitung
Das Octahydrat wird durch Behandeln von Natriumhydroxid mit Wasserstoffperoxid hergestellt.
Natriumperoxid kann in großem Maßstab durch die Reaktion von metallischem Natrium mit Sauerstoff bei 130–200 °C hergestellt werden, ein Prozess, bei dem Natriumoxid erzeugt wird , das in einer separaten Stufe Sauerstoff absorbiert:
- 4 Na + O 2 → 2 Na 2 O
- 2 Na 2 O + O 2 → 2 Na 2 O 2
Es kann auch hergestellt werden, indem Ozongas über festes Natriumjodid in einem Platin- oder Palladiumrohr geleitet wird. Das Ozon oxidiert das Natrium zu Natriumperoxid. Das Jod kann durch mildes Erhitzen sublimiert werden. Das Platin oder Palladium katalysiert die Reaktion und wird vom Natriumperoxid nicht angegriffen.
Verwendet
Natriumperoxid hydrolisiert zu geben , Natriumhydroxid und Wasserstoffperoxid gemäß der Reaktion
- Na 2 O 2 + 2 H 2 O → 2 NaOH + H 2 O 2
Natriumperoxid wurde zum Bleichen von Zellstoff für die Papier- und Textilherstellung verwendet. Gegenwärtig wird es hauptsächlich für spezialisierte Laborarbeiten verwendet, zB zur Gewinnung von Mineralien aus verschiedenen Erzen. Natriumperoxid kann unter den Handelsnamen Solozone und Flocool geführt werden . In chemischen Präparaten wird Natriumperoxid als Oxidationsmittel verwendet. Es wird auch als Sauerstoffquelle verwendet, indem es mit Kohlendioxid reagiert, um Sauerstoff und Natriumcarbonat zu produzieren:
- 2 Na 2 O 2 + 2 CO 2 → 2 Na 2 CO 3 + O 2
Es ist daher besonders nützlich in Tauchausrüstung, U-Booten usw. Lithiumperoxid und Kaliumsuperoxid haben ähnliche Verwendungen.

