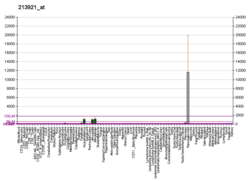
Somatostatin - Somatostatin
Somatostatin , auch bekannt als Wachstumshormon-inhibierendes Hormon ( GHIH ) oder unter mehreren anderen Namen , ist ein Peptidhormon , das das endokrine System reguliert und die Neurotransmission und Zellproliferation durch Interaktion mit G-Protein-gekoppelten Somatostatin-Rezeptoren und Hemmung der Freisetzung zahlreicher sekundäre Hormone. Somatostatin hemmt die Insulin- und Glukagonsekretion.
Somatostatin hat zwei aktive Formen, die durch die alternative Spaltung eines einzelnen Präproproteins hergestellt werden: eine besteht aus 14 Aminosäuren (siehe Infobox rechts), die andere besteht aus 28 Aminosäuren.
Unter den Wirbeltieren existieren sechs verschiedene Somatostatin-Gene, die als SS1, SS2, SS3, SS4, SS5 und SS6 bezeichnet werden . Zebrafische haben alle sechs. Die sechs verschiedenen Gene, zusammen mit den fünf verschiedenen Somatostatin-Rezeptoren , verleihen Somatostatin eine große Bandbreite an Funktionen. Der Mensch hat nur ein Somatostatin-Gen, SST .
Nomenklatur
Synonyme von "Somatostatin" umfassen:
- Wachstumshormon-hemmendes Hormon (GHIH)
- Wachstumshormonfreisetzungs-hemmendes Hormon (GHRIH)
- Somatotropin-Freisetzungs-Hemmfaktor (SRIF)
- Somatotropin-Freisetzungs-hemmendes Hormon (SRIH)
Produktion
Verdauungstrakt
Somatostatin wird von Delta-Zellen an mehreren Stellen im Verdauungssystem sezerniert , nämlich im Pylorusantrum , im Duodenum und in den Pankreasinseln .
Somatostatin, das im Pylorusantrum freigesetzt wird, wandert über das Pfortadersystem zum Herzen, gelangt dann in den systemischen Kreislauf, um die Stellen zu erreichen, an denen es seine hemmende Wirkung entfalten wird. Darüber hinaus kann die Somatostatinfreisetzung aus Deltazellen parakrin wirken .
Im Magen wirkt Somatostatin über einen G-Protein-gekoppelten Rezeptor (der die Adenylatcyclase hemmt und somit der stimulierenden Wirkung von Histamin effektiv entgegenwirkt) direkt auf die säureproduzierenden Belegzellen , um die Säuresekretion zu reduzieren. Somatostatin kann auch indirekt die Magensäureproduktion verringern, indem es die Freisetzung anderer Hormone, einschließlich Gastrin und Histamin, verhindert, was den Verdauungsprozess effektiv verlangsamt.
Gehirn

Sst wird in Interneuronen im Telencephalon der embryonalen Maus am Tag 15,5 exprimiert. Allen Gehirnatlanten
|
Somatostatin wird von neuroendokrinen Neuronen des ventromedialen Nucleus des Hypothalamus produziert . Diese Neuronen projizieren zur mittleren Eminenz , wo Somatostatin von neurosekretorischen Nervenenden in das Hypothalamohypophysensystem durch Neuronen-Axone freigesetzt wird . Somatostatin wird dann zum Hypophysenvorderlappen transportiert , wo es die Sekretion von Wachstumshormonen aus somatotropen Zellen hemmt . Die Somatostatin-Neuronen im periventrikulären Kern vermitteln negative Rückkopplungseffekte des Wachstumshormons auf seine eigene Freisetzung; die Somatostatin-Neuronen reagieren auf hohe zirkulierende Konzentrationen von Wachstumshormon und Somatomedinen, indem sie die Freisetzung von Somatostatin erhöhen, wodurch die Sekretionsrate von Wachstumshormon verringert wird.
Somatostatin wird auch von mehreren anderen Populationen produziert, die zentral, dh in andere Bereiche des Gehirns, projizieren, und Somatostatinrezeptoren werden an vielen verschiedenen Stellen im Gehirn exprimiert. Insbesondere treten Populationen von Somatostatin-Neuronen im Nucleus arcuatus , im Hippocampus und im Hirnstammkern des Trakts solitär auf .
Funktionen
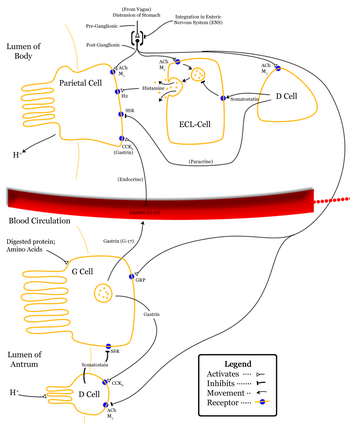
Somatostatin wird als hemmendes Hormon klassifiziert und wird durch einen niedrigen pH-Wert induziert. Seine Aktionen verteilen sich auf verschiedene Körperteile. Die Somatostatinfreisetzung wird durch den Vagusnerv gehemmt .
Hypophysenvorderlappen
Im Hypophysenvorderlappen sind die Wirkungen von Somatostatin:
- Hemmung der Freisetzung von Wachstumshormon (GH) (und wirkt so den Wirkungen des Wachstumshormon-Releasing-Hormons (GHRH) entgegen)
- Hemmung der Freisetzung von Schilddrüsen-stimulierendem Hormon (TSH)
- Hemmung der Adenylylcyclase in Belegzellen
- Hemmung der Freisetzung von Prolaktin (PRL)
Magen-Darm-System
- Somatostatin ist homolog zu Cortistatin (siehe Somatostatin-Familie ) und unterdrückt die Ausschüttung von Magen-Darm-Hormonen
- Verringert die Magenentleerung und reduziert die Kontraktionen der glatten Muskulatur und den Blutfluss im Darm
- Unterdrückt die Ausschüttung von Pankreashormonen
- Somatostatin Freisetzung wird durch die Beta - Zelle ausgelöst Peptid urocortin3 (Ucn3) zu hemmen Insulin - Release.
- Hemmt die Freisetzung von Glucagon
- Unterdrückt die exokrine sekretorische Wirkung der Bauchspeicheldrüse
Synthetische Ersatzstoffe
Octreotid (Markenname Sandostatin, Novartis Pharmaceuticals ) ist ein Octapeptid , das pharmakologisch natürliches Somatostatin nachahmt, obwohl es ein stärkerer Inhibitor von Wachstumshormon, Glucagon und Insulin als das natürliche Hormon ist und eine viel längere Halbwertszeit (etwa 90 Minuten, im Vergleich zu 2–3 Minuten für Somatostatin). Da es schlecht aus dem Darm resorbiert wird, wird es parenteral (subkutan, intramuskulär oder intravenös) verabreicht. Es ist angezeigt zur symptomatischen Behandlung des Karzinoidsyndroms und der Akromegalie . Es findet auch vermehrt Anwendung bei polyzystischen Erkrankungen der Leber und Niere.
Lanreotid (Somatulin, Ipsen Pharmaceuticals ) ist ein Medikament zur Behandlung von Akromegalie und Symptomen, die durch neuroendokrine Tumoren, insbesondere das Karzinoid-Syndrom, verursacht werden. Es ist ein langwirksames Analogon von Somatostatin, wie Octreotid. Es ist in mehreren Ländern erhältlich, darunter Großbritannien, Australien und Kanada, und wurde am 30. August 2007 von der Food and Drug Administration in den Vereinigten Staaten zum Verkauf zugelassen.
Pasireotid , das unter dem Markennamen Signifor vertrieben wird, ist ein in den Vereinigten Staaten und der Europäischen Union zugelassenes Arzneimittel für seltene Leiden zur Behandlung des Morbus Cushing bei Patienten, bei denen eine chirurgische Therapie versagt oder nicht geeignet ist. Es wurde von Novartis entwickelt . Pasireotid ist ein Somatostatin- Analogon mit einer 40-fach erhöhten Affinität zum Somatostatin-Rezeptor 5 im Vergleich zu anderen Somatostatin-Analoga.
Evolutionsgeschichte
Bei Wirbeltieren wurden sechs Somatostatin-Gene entdeckt . Die gegenwärtig vorgeschlagene Geschichte, wie diese sechs Gene entstanden basiert auf den drei Voll Genomduplikation Ereignisse, die sich in der Wirbeltierevolution zusammen mit lokalen Verdoppelungen in Teleostier Fisch. Ein angestammtes Somatostatin-Gen wurde während des ersten Gesamtgenom-Duplikationsereignisses (1R) dupliziert , um SS1 und SS2 zu erzeugen . Diese beiden Gene wurden während des zweiten Duplikationsereignisses des gesamten Genoms (2R) dupliziert, um vier neue Somatostatin-Gene zu erzeugen: SS1, SS2, SS3 und ein Gen, das während der Evolution der Wirbeltiere verloren ging. Tetrapoden behielten SS1 (auch bekannt als SS-14 und SS-28 ) und SS2 (auch bekannt als Cortistatin ) nach der Aufteilung in die Aufteilung der Sarcopterygii- und Actinopterygii- Linie bei. In Teleostier Fisch, SS1, SS2 und SS3 wurden während der dritten gesamten Genoms Duplikationsereignis (3R) dupliziert erstellen SS1, SS2, SS4, SS5, und zwei Gene , die bei der Entwicklung von Knochenfischen verloren. SS1 und SS2 durchliefen lokale Duplizierungen, um zu SS6 und SS3 zu führen .
Siehe auch
Verweise
Weiterlesen
- Florio T., Schettini G (September 2001). „[Somatostatin und seine Rezeptoren. Rolle bei der Kontrolle der Zellproliferation]“. Minerva Endocrinologica . 26 (3): 91-102. PMID 11753230 .
- Y. Yamada, T. Reisine, SF Law, Y. Ihara, A. Kubota, S. Kagimoto, M. Seino, Y. Seino, GI Bell, S. Seino (Dezember 1992). „Somatostatin-Rezeptoren, eine wachsende Genfamilie: Klonierung und funktionelle Charakterisierung von humanem SSTR3, einem Protein, das an Adenylylcyclase gekoppelt ist“. Molekulare Endokrinologie . 6 (12): 2136–42. doi : 10.1210/me.6.12.2136 . PMID 1337145 .
- Yamada Y, Post SR, Wang K, Tager HS, Bell GI, Seino S (Januar 1992). "Klonierung und funktionelle Charakterisierung einer Familie von Somatostatinrezeptoren von Mensch und Maus, die in Gehirn, Magen-Darm-Trakt und Niere exprimiert werden" . Proceedings of the National Academy of Sciences of the United States of America . 89 (1): 251–5. Bibcode : 1992PNAS...89..251Y . doi : 10.1073/pnas.89.1.251 . PMC 48214 . PMID 1346068 .
- P. Brazeau, W. Vale, R. Burgus, N. Ling, M. Butcher, J. Rivier, R. Guillemin (Januar 1973). „Hypothalamisches Polypeptid, das die Sekretion von immunreaktivem Hypophysen-Wachstumshormon hemmt“. Wissenschaft . 179 (4068): 77–9. Bibcode : 1973Sci...179...77B . doi : 10.1126/science.179.4068.77 . PMID 4682131 . S2CID 10997771 .
- Shen LP, Pictet RL, Rutter WJ (August 1982). "Humanes Somatostatin I: Sequenz der cDNA" . Proceedings of the National Academy of Sciences of the United States of America . 79 (15): 4575–9. Bibcode : 1982PNAS...79.4575S . doi : 10.1073/pnas.79.15.4575 . PMC 346.717 . PMID 6126875 .
- Shen LP, Rutter WJ (April 1984). „Sequenz des menschlichen Somatostatin I-Gens“. Wissenschaft . 224 (4645): 168–71. Bibcode : 1984Sci...224..168S . doi : 10.1126/science.6142531 . PMID 6142531 .
- Montminy MR, Goodman RH, Horovitch SJ, Habener JF (Juni 1984). "Primäre Struktur des Gens, das Ratten-Preprosomatostatin codiert" . Proceedings of the National Academy of Sciences of the United States of America . 81 (11): 3337–40. Bibcode : 1984PNAS...81.3337M . doi : 10.1073/pnas.81.11.3337 . PMC 345.502 . PMID 6145156 .
- Zabel BU, Naylor SL, Sakaguchi AY, Bell GI, zeigt TB (November 1983). "Hochauflösende chromosomale Lokalisierung menschlicher Gene für Amylase, Proopiomelanocortin, Somatostatin und ein DNA-Fragment (D3S1) durch in-situ-Hybridisierung" . Proceedings of the National Academy of Sciences of the United States of America . 80 (22): 6932–6. Bibcode : 1983PNAS...80.6932Z . doi : 10.1073/pnas.80.22.6932 . PMC 390100 . PMID 6196780 .
- Panetta R, Greenwood MT, Warszynska A, Demchyshyn LL, Day R, Niznik HB, Srikant CB, Patel YC (März 1994). „Molekulare Klonierung, funktionelle Charakterisierung und chromosomale Lokalisation eines menschlichen Somatostatinrezeptors (Somatostatinrezeptor Typ 5) mit bevorzugter Affinität für Somatostatin-28“. Molekulare Pharmakologie . 45 (3): 417–27. PMID 7908405 .
- Demchyshyn LL, Srikant CB, Sunahara RK, Kent G, Seeman P, Van Tol HH, Panetta R, Patel YC, Niznik HB (Juni 1993). „Klonierung und Expression einer humanen Somatostatin-14-selektiven Rezeptorvariante (Somatostatinrezeptor 4) auf Chromosom 20“. Molekulare Pharmakologie . 43 (6): 894–901. PMID 8100352 .
- Kaupmann K, Bruns C, Hoyer D, Seuwen K, Lübbert H (September 1993). "Verteilung und Second-Messenger-Kopplung von vier im Gehirn exprimierten Somatostatinrezeptor-Subtypen" . FEBS-Briefe . 331 (1–2): 53–9. doi : 10.1016/0014-5793(93)80296-7 . PMID 8405411 . S2CID 22557713 .
- Aguila MC, Rodriguez AM, Aguila-Mansilla HN, Lee WT (Mai 1996). "Somatostatin-Antisense-Oligodesoxynukleotid-vermittelte Stimulation der Lymphozytenproliferation in Kultur" . Endokrinologie . 137 (5): 1585–90. doi : 10.1210/de.137.5.1585 . PMID 8612489 .
- Sharma K, Patel YC, Srikant CB (Dezember 1996). „Subtyp-selektive Induktion von Wildtyp-p53 und Apoptose, aber nicht Zellzyklusarrest, durch den menschlichen Somatostatin-Rezeptor 3“. Molekulare Endokrinologie . 10 (12): 1688–96. doi : 10.1210/me.10.12.1688 . PMID 8961277 .
- Dournaud P, Boudin H, Schönbrunn A, Tannenbaum GS, Beaudet A (Februar 1998). „Wechselbeziehungen zwischen Somatostatin-sst2A-Rezeptoren und Somatostatin-enthaltenden Axonen im Rattenhirn: Beweise für die Regulierung von Zelloberflächenrezeptoren durch endogenes Somatostatin“ . Die Zeitschrift für Neurowissenschaften . 18 (3): 1056–71. doi : 10.1523/JNEUROSCI.18-03-01056.1998 . PMC 6792775 . PMID 9437026 .
- Barnea A, Roberts J, Ho RH (Januar 1999). „Beweise für eine synergistische Wirkung des HIV-1-Hüllproteins gp120 und des aus dem Gehirn stammenden neurotrophen Faktors (BDNF), der zu einer verstärkten Expression von Somatostatin-Neuronen in Aggregatkulturen aus dem menschlichen fetalen Kortex führt“. Gehirnforschung . 815 (2): 349–57. doi : 10.1016/S0006-8993(98)01098-1 . PMID 9878821 . S2CID 21793593 .
- Ferone D, van Hagen PM, van Koetsveld PM, Zuijderwijk J, Mooy DM, Lichtenauer-Kaligis EG, Colao A, Bogers AJ, Lombardi G, Lamberts SW, Hofland LJ (Januar 1999). "In-vitro-Charakterisierung von Somatostatinrezeptoren im menschlichen Thymus und Wirkungen von Somatostatin und Octreotid auf kultivierte Thymusepithelzellen" . Endokrinologie . 140 (1): 373–80. doi : 10.1210/en.140.1.373 . PMID 9886848 .
- N. Brakch, N. Lazar, M. Panchal, F. Allemandou, G. Boileau, P. Cohen, M. Rholam (Februar 2002). „Die Somatostatin-28(1-12)-NPAMAP-Sequenz: ein wesentliches helix-förderndes Motiv, das die Prosomatostatin-Verarbeitung an mono- und dibasischen Stellen steuert“. Biochemie . 41 (5): 1630–9. doi : 10.1021/bi011928m . PMID 11814357 .
- Oomen SP, van Hennik PB, Antonissen C, Lichtenauer-Kaligis EG, Hofland LJ, Lamberts SW, Löwenberg B, Touw IP (Februar 2002). „Somatostatin ist ein selektiver Chemoattraktant für primitive (CD34(+)) hämatopoetische Vorläuferzellen“. Experimentelle Hämatologie . 30 (2): 116–25. doi : 10.1016/S0301-472X(01)00772-X . PMID 11823046 .
- Simonetti M, Di BC (Februar 2002). „Strukturmotive im Reifungsprozess von Peptidhormonen. Der Somatostatin-Vorläufer. I. Eine CD-Konformationsstudie“. Zeitschrift für Peptidwissenschaft . 8 (2): 66–79. doi : 10.1002/psc.370 . PMID 11860030 . S2CID 20438890 .