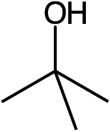
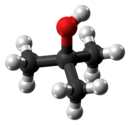
tert- Butanol - tert-Butyl alcohol
|
|
|||

|
|||
| Namen | |||
|---|---|---|---|
|
Bevorzugter IUPAC-Name
2-Methylpropan-2-ol |
|||
Andere Namen
|
|||
| Bezeichner | |||
|
3D-Modell ( JSmol )
|
|||
| 906698 | |||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| Arzneimittelbank | |||
| ECHA-Infokarte |
100.000.809 |
||
| EG-Nummer | |||
| 1833 | |||
| Gittergewebe | tert-Butyl+Alkohol | ||
|
PubChem- CID
|
|||
| RTECS-Nummer | |||
| UNII | |||
| UN-Nummer | 1120 | ||
|
CompTox-Dashboard ( EPA )
|
|||
|
|||
|
|||
| Eigenschaften | |||
| C 4 H 10 O | |||
| Molmasse | 74,123 g·mol -1 | ||
| Aussehen | Farbloser Feststoff | ||
| Geruch | Kampfer | ||
| Dichte | 0,775 g/ml | ||
| Schmelzpunkt | 25 bis 26 °C; 77 bis 79 °F; 298 bis 299 K | ||
| Siedepunkt | 82 bis 83 °C; 179 bis 181 °F; 355 bis 356 K | ||
| mischbar | |||
| log P | 0,584 | ||
| Dampfdruck | 4,1 kPa (bei 20 °C) | ||
| Säure (p K a ) | 16.54 | ||
| 5,742 × 10 -5 cm 3 /mol | |||
|
Brechungsindex ( n D )
|
1.387 | ||
| 1,31 D | |||
| Thermochemie | |||
|
Wärmekapazität ( C )
|
215,37 JK −1 mol −1 | ||
|
Std molare
Entropie ( S |
189,5 JK −1 mol −1 | ||
|
Std
Bildungsenthalpie (Δ f H ⦵ 298 ) |
−360,04 bis −358.36 kJ mol −1 | ||
|
Std.
Verbrennungsenthalpie (Δ c H ⦵ 298 ) |
−2.64479 bis −2.64321 MJ mol −1 | ||
| Gefahren | |||
| Sicherheitsdatenblatt | inchem.org | ||
| GHS-Piktogramme |
 
|
||
| GHS-Signalwort | Achtung | ||
| H225 , H319 , H332 , H335 | |||
| P210 , P261 , P305+351+338 | |||
| NFPA 704 (Feuerdiamant) | |||
| Flammpunkt | 11 °C (52 °F; 284 K) | ||
| 480 °C (896 °F; 753 K) | |||
| Explosionsgrenzen | 2,4–8,0% | ||
| Letale Dosis oder Konzentration (LD, LC): | |||
|
LD 50 ( mediane Dosis )
|
3559 mg/kg (Kaninchen, oral) 3500 mg/kg (Ratte, oral) |
||
| NIOSH (US-Grenzwerte für die Gesundheitsbelastung): | |||
|
PEL (zulässig)
|
TWA 100 ppm (300 mg/m 3 ) | ||
|
REL (empfohlen)
|
TWA 100 ppm (300 mg/m 3 ) ST 150 ppm (450 mg/m 3 ) | ||
|
IDLH (unmittelbare Gefahr)
|
1600 ppm | ||
| Verwandte Verbindungen | |||
|
Verwandte Butanole
|
2-Butanol |
||
|
Verwandte Verbindungen
|
2-Methyl-2-butanol Trimethylsilanol |
||
|
Sofern nicht anders angegeben, beziehen sich die Daten auf Materialien im Standardzustand (bei 25 °C [77 °F], 100 kPa). |
|||
|
|
|||
| Infobox-Referenzen | |||
tert -Butylalkohol ist der einfachste tertiäre Alkohol mit einer Formel von (CH 3 ) 3 COH (manchmal dargestellt als t - BuOH). Es ist eines der vier Isomere von Butanol . tert- Butanol ist ein farbloser Feststoff, der bei Raumtemperatur schmilzt und einen kampferartigen Geruch hat. Es ist mischbar mit Wasser , Ethanol und Diethylether .
Natürliches Vorkommen
tert- Butanol wurde in Bier und Kichererbsen nachgewiesen . Es kommt auch in Maniok vor , das als Gärungszutat in bestimmten alkoholischen Getränken verwendet wird .
Vorbereitung
tert- Butanol wird kommerziell von Isobutan als Nebenprodukt der Propylenoxid- Produktion abgeleitet. Es kann auch durch die katalytische Hydratation von Isobutylen oder durch eine Grignard-Reaktion zwischen Aceton und Methylmagnesiumchlorid hergestellt werden .
Die Reinigung kann aufgrund der Bildung eines Azeotrops mit Wasser nicht durch einfache Destillation durchgeführt werden , obwohl das anfängliche Trocknen des Lösungsmittels, das große Mengen Wasser enthält, durch Zugabe von Benzol unter Bildung eines tertiären Azeotrops und Abdestillieren des Wassers durchgeführt wird. Kleinere Wassermengen werden durch Trocknen mit Calciumoxid (CaO), Kaliumcarbonat (K 2 CO 3 ), Calciumsulfat (CaSO 4 ) oder Magnesiumsulfat (MgSO 4 ) und anschließender fraktionierter Destillation entfernt. Wasserfreier tert- Butylalkohol wird durch weiteres Erhitzen unter Rückfluss und Destillieren von mit Jod aktiviertem Magnesium oder Alkalimetallen wie Natrium oder Kalium erhalten. Andere Verfahren umfassen die Verwendung von 4 Å Molekularsiebe , Aluminium - tert - butylat , Calciumhydrid (CaH 2 ), oder durch fraktionierte Kristallisation unter Inertatmosphäre.
Anwendungen
tert -Butylalkohol als Lösungsmittel verwendet, Ethanol Denaturierungsmittel , Abbeizmittel Bestandteil und Benzinoktanverstärker und Oxygenat . Es ist ein chemisches Zwischenprodukt, das verwendet wird, um Methyl- tert- butylether (MTBE) und Ethyl- tert- butylether (ETBE) durch Reaktion mit Methanol bzw. Ethanol und tert- Butylhydroperoxid (TBHP) durch Reaktion mit Wasserstoffperoxid herzustellen .
Reaktionen
Als tertiärer Alkohol ist tert- Butylalkohol oxidationsbeständiger als die anderen Isomere von Butanol.
tert- Butanol wird mit einer starken Base zum Alkoxid deprotoniert . Besonders verbreitet ist Kalium- tert- butoxid , das durch Behandeln von tert- Butanol mit Kaliummetall hergestellt wird.
- K + t -BuOH → t -BuO − K + + 1/2 H 2
Das tert- Butoxid ist eine starke, nicht- nukleophile Base in der organischen Chemie. Es abstrahiert leicht saure Protonen von Substraten, aber sein sterischer Anspruch verhindert, dass die Gruppe an nukleophilen Substitutionen wie in einer Williamson-Ethersynthese oder einer S N 2 -Reaktion teilnimmt .
tert- Butylalkohol reagiert mit Chlorwasserstoff zu tert- Butylchlorid .
O-Chlorierung von tert-Butylalkohol mit hypochloriger Säure zu tert-Butylhypochlorit :
- (CH 3 ) 3 COH + HOCl → (CH 3 ) 3 COCl + H 2 O
Pharmakologie und Toxikologie
Zur Pharmakologie und Toxikologie von tert-Butanol beim Menschen und anderen Tieren liegen nur begrenzte Daten vor. Eine Exposition des Menschen kann aufgrund des Brennstoff-Sauerstoffstoffwechsels auftreten. Tert-Butanol wird schlecht durch die Haut resorbiert, aber schnell resorbiert, wenn es eingeatmet oder verschluckt wird. Tert-Butanol reizt die Haut oder die Augen. Die Toxizität von Einzeldosen ist normalerweise gering, hohe Dosen können jedoch eine sedierende oder anästhetische Wirkung haben.
Anmerkungen
Verweise
Externe Links
- Internationale Chemikaliensicherheitskarte 0114
- NIOSH Pocket Guide zu chemischen Gefahren. "#0078" . Nationales Institut für Arbeitssicherheit und Gesundheitsschutz (NIOSH).
- IPCS Environmental Health Criteria 65: Butanole: vier Isomere
- IPCS Gesundheits- und Sicherheitsleitfaden 7: tert- Butanol