Thallium (I) iodid - Thallium(I) iodide
|
|
| Namen | |
|---|---|
| Andere Namen
Thalliummonoiodid Thallous
Iodid |
|
| Kennungen | |
|
3D-Modell ( JSmol )
|
|
| ChemSpider | |
| ECHA InfoCard |
100.029.272 |
|
PubChem CID
|
|
| UNII | |
|
CompTox Dashboard ( EPA )
|
|
|
|
|
|
| Eigenschaften | |
| TlI | |
| Molmasse | 331,287 g / mol |
| Aussehen | gelbe Kristalle |
| Dichte | 7,1 g / cm 3 |
| Schmelzpunkt | 441,7 ° C (827,1 ° F; 714,8 K) |
| Siedepunkt | 824 ° C (1.515 ° F; 1.097 K) |
| 0,085 g / l (25 ° C) | |
| Löslichkeit | unlöslich in Alkohol |
| –82,2 · 10 –6 cm 3 / mol | |
| Gefahren | |
|
EU-Klassifikation (DSD) (veraltet)
|
Sehr giftig ( T + ) Umweltgefährlich ( N ) |
| R-Sätze (veraltet) | R26 / 28 , R33 , R51 / 53 |
| S-Sätze (veraltet) | (S1 / 2) , S13 , S28 , S45 , S61 |
| Flammpunkt | Nicht brennbar |
| Verwandte Verbindungen | |
|
Andere Anionen
|
Thallium (I) fluorid Thallium (I) chlorid Thallium (I) bromid |
|
Andere Kationen
|
Gallium (I) -iodid Indium (I) -iodid |
|
Verwandte Verbindungen
|
Quecksilber (II) -iodid Blei (II) -iodid |
|
Sofern nicht anders angegeben, werden Daten für Materialien in ihrem Standardzustand (bei 25 ° C, 100 kPa) angegeben. |
|
|
|
|
| Infobox-Referenzen | |
Thallium (I) -iodid ist eine chemische Verbindung mit der Formel TlI . Es ist ungewöhnlich , in einer der wenigen wasserunlösliches Metall ist Iodide , zusammen mit AgI , CuI , SnI 2 , SnI 4 , PbI 2 und HgI 2 .
Chemie
TlI kann in wässriger Lösung durch Metathese eines beliebigen löslichen Thalliumsalzes mit Iodidionen gebildet werden. Es entsteht auch als Nebenprodukt bei der Thallium-geförderten Iodierung von Phenolen mit Thallium (I) -acetat.
Versuche oxydieren TlI zu Thallium (III) -iodid ausfallen, da die Oxidation der erzeugt Thallium (I) Triiodid , Tl + I 3 - .
Physikalische Eigenschaften
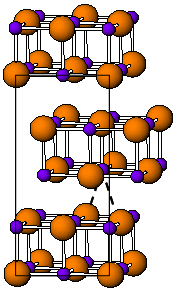
Die Raumtemperaturform von TlI ist gelb und weist eine orthorhombische Struktur auf, die als verzerrte NaCl-Struktur angesehen werden kann. Es wird angenommen, dass die verzerrte Struktur durch günstige Thallium-Thallium-Wechselwirkungen verursacht wird. Der nächste Tl-Tl-Abstand beträgt 383 pm. Bei 175 ° C wandelt sich die gelbe Form in eine rote CsCl- Form um. Dieser Phasenübergang geht mit einem Sprung der elektrischen Leitfähigkeit um etwa zwei Größenordnungen einher. Die CsI-Struktur kann durch Dotieren von TlI mit anderen Halogeniden wie RbI, CsI, KI, AgI, TlBr und TlCl bis auf Raumtemperatur stabilisiert werden . Das Vorhandensein von Verunreinigungen könnte daher für die Koexistenz der kubischen und orthorombischen TlI- Phasen bei Umgebungsbedingungen verantwortlich sein. Unter hohem Druck von 160 kbar wird TlI zu einem metallischen Leiter. Auf LiF- , NaCl- oder KBr-Substraten gewachsene nanometerdünne TlI- Filme weisen die kubische Steinsalzstruktur auf.
Anwendungen
Quecksilberbogenlampen werden Thallium (I) -iodid zugesetzt, um ihre Leistung zu verbessern. Das erzeugte Licht befindet sich hauptsächlich im blaugrünen Teil des sichtbaren Lichtspektrums, das am wenigsten von Wasser absorbiert wird. Daher wurden diese für die Unterwasserbeleuchtung verwendet. Thallium (I) -iodid wird auch in Spurenmengen mit NaI oder CsI verwendet , um Szintillatoren herzustellen, die in Strahlungsdetektoren verwendet werden.
Natürliches Vorkommen
Natürliches Thallium (I) -iodid wurde erst kürzlich als orthorhombisches Polymorph namens Nataliyamalikit gefunden. Es ist fumarolischen Ursprungs.
Sicherheit
Wie alle Thalliumverbindungen ist Thallium (I) -iodid hochgiftig.
Verweise
Zitierte Quellen
- Haynes, William M., Hrsg. (2011). CRC-Handbuch für Chemie und Physik (92. Ausgabe). Boca Raton, FL: CRC-Presse . ISBN 1439855110 .
