Unjahr - Ununennium
| Unennium | ||||||
|---|---|---|---|---|---|---|
| Aussprache |
/ ˌ uː n . û n ɛ n i ə m / ( hören ) |
|||||
| Alternative Namen | Element 119, Eka-Francium | |||||
| Ununennium im Periodensystem | ||||||
| ||||||
| Ordnungszahl ( Z ) | 119 | |||||
| Gruppe | Gruppe 1: Wasserstoff und Alkalimetalle | |||||
| Zeitraum | Periode 8 | |||||
| Block | s-block | |||||
| Elektronenkonfiguration | [ Og ] 8s 1 (vorhergesagt) | |||||
| Elektronen pro Schale | 2, 8, 18, 32, 32, 18, 8, 1 (vorhergesagt) | |||||
| Physikalische Eigenschaften | ||||||
| Phase bei STP | unbekannt (könnte fest oder flüssig sein) | |||||
| Schmelzpunkt | 273–303 K (0–30 °C, 32–86 °F) (vorhergesagt) | |||||
| Siedepunkt | 903 K (630 °C, 1166 °F) (vorhergesagt) | |||||
| Dichte (nahe rt ) | 3 g/cm 3 (vorhergesagt) | |||||
| Schmelzwärme | 2,01–2,05 kJ/mol ( hochgerechnet ) | |||||
| Atomare Eigenschaften | ||||||
| Oxidationsstufen | ( +1 ), (+3) (vorhergesagt) | |||||
| Elektronegativität | Pauling-Skala: 0,86 (vorhergesagt) | |||||
| Ionisierungsenergien | ||||||
| Atomradius | empirisch: 240 pm (vorhergesagt) | |||||
| Kovalenter Radius | 263–281 Uhr ( hochgerechnet ) | |||||
| Andere Eigenschaften | ||||||
| Kristallstruktur | kubisch raumzentrierte (bcc)
(hochgerechnet) |
|||||
| CAS-Nummer | 54846-86-5 | |||||
| Geschichte | ||||||
| Benennung | Name des systematischen IUPAC- Elements | |||||
Ununennium , auch bekannt als Eka-Francium oder Element 119 , ist das hypothetische chemische Element mit dem Symbol Uue und der Ordnungszahl 119. Ununennium und Uue sind der temporäre systematische IUPAC-Name bzw. das Symbol , die verwendet werden, bis das Element entdeckt, bestätigt und ein dauerhafter Name wird festgelegt. Im Periodensystem der Elemente wird erwartet, dass es ein S-Block- Element, ein Alkalimetall und das erste Element in der achten Periode ist . Es ist das leichteste Element, das noch nicht synthetisiert wurde.
Bei RIKEN (Japan) und dem Joint Institute for Nuclear Research ( Dubna , Russland) wurden erfolglose Versuche unternommen, das Element zu synthetisieren . Theoretische und experimentelle Beweise haben gezeigt, dass die Synthese von Ununennium wahrscheinlich weitaus schwieriger sein wird als die der vorherigen Elemente, und es könnte sogar das vorletzte Element sein, das mit der aktuellen Technologie synthetisiert werden kann.
Die Position von Ununennium als siebtes Alkalimetall deutet darauf hin, dass es ähnliche Eigenschaften wie seine leichteren Artgenossen haben würde . Allerdings relativistische Effekte können einige seiner Eigenschaften führen von denen aus einer geraden Anwendung der erwarteten abweichen periodische Trends . Zum Beispiel wird Ununennium weniger reaktiv zu sein als erwartet , Cäsium und Francium und näher im Verhalten zu sein , Kalium oder Rubidium , und während es den Merkmal +1 zeigen soll Oxidationszustand des Alkalimetalls, ist es auch die +3 zeigen vorhergesagte Oxidationsstufe, die bei keinem anderen Alkalimetall bekannt ist.
Einführung

| Externes Video | |
|---|---|
|
|
Die schwersten Atomkerne entstehen in Kernreaktionen, bei denen zwei andere Kerne ungleicher Größe zu einem zusammengefasst werden; grob gesagt, je ungleicher die beiden Kerne in Bezug auf die Masse sind, desto größer ist die Wahrscheinlichkeit, dass die beiden reagieren. Das Material aus den schwereren Kernen wird zu einem Target, das dann mit dem Strahl leichterer Kerne beschossen wird . Zwei Kerne können nur dann zu einem verschmelzen, wenn sie sich nahe genug annähern; Normalerweise stoßen sich Kerne (alle positiv geladen) aufgrund elektrostatischer Abstoßung gegenseitig ab . Die starke Wechselwirkung kann diese Abstoßung überwinden, aber nur in sehr kurzer Entfernung von einem Kern; Strahlkerne werden somit stark beschleunigt , um eine solche Abstoßung im Vergleich zur Geschwindigkeit des Strahlkerns unbedeutend zu machen. Nähern allein reicht nicht aus, damit zwei Kerne verschmelzen: Wenn sich zwei Kerne nähern, bleiben sie normalerweise für etwa 10 −20 Sekunden zusammen und trennen sich dann (nicht unbedingt in der gleichen Zusammensetzung wie vor der Reaktion) anstatt einen einzigen zu bilden Kern. Wenn eine Fusion stattfindet, ist die vorübergehende Verschmelzung – als zusammengesetzter Kern bezeichnet – ein angeregter Zustand . Um seine Anregungsenergie zu verlieren und einen stabileren Zustand zu erreichen, spaltet ein zusammengesetzter Kern entweder oder stößt ein oder mehrere Neutronen aus , die die Energie wegtragen . Dies geschieht ungefähr 10 –16 Sekunden nach der ersten Kollision.
Der Strahl durchdringt das Target und erreicht die nächste Kammer, den Separator; wenn ein neuer Kern entsteht, wird er mit diesem Strahl getragen. Im Separator wird der neu gebildete Kern von anderen Nukliden (dem des ursprünglichen Strahls und allen anderen Reaktionsprodukten) getrennt und zu einem Oberflächenbarrierendetektor transportiert , der den Kern stoppt. Der genaue Ort des bevorstehenden Aufpralls auf den Detektor ist markiert; ebenfalls gekennzeichnet sind seine Energie und der Zeitpunkt der Ankunft. Die Übertragung dauert ca. 10 -6 Sekunden; um entdeckt zu werden, muss der Kern so lange überleben. Sobald sein Zerfall registriert ist, wird der Kern erneut aufgezeichnet und der Ort, die Energie und der Zeitpunkt des Zerfalls gemessen.
Die Stabilität eines Kerns wird durch die starke Wechselwirkung gewährleistet. Seine Reichweite ist jedoch sehr kurz; wenn die Kerne größer werden, schwächt sich ihr Einfluss auf die äußersten Nukleonen ( Protonen und Neutronen) ab. Gleichzeitig wird der Kern durch elektrostatische Abstoßung zwischen Protonen zerrissen, da er eine unbegrenzte Reichweite hat. Kerne der schwersten Elemente werden daher theoretisch vorhergesagt und es wurde bisher beobachtet, dass sie hauptsächlich über Zerfallsmodi zerfallen, die durch eine solche Abstoßung verursacht werden: Alpha-Zerfall und spontane Spaltung ; diese Moden sind für Kerne superschwerer Elemente vorherrschend . Alpha-Zerfälle werden von den emittierten Alpha-Teilchen registriert , und die Zerfallsprodukte sind vor dem eigentlichen Zerfall leicht zu bestimmen; wenn ein solcher Zerfall oder eine Folge von aufeinander folgenden Zerfällen einen bekannten Kern ergibt, kann das ursprüngliche Produkt einer Reaktion arithmetisch bestimmt werden. Bei der spontanen Spaltung entstehen jedoch verschiedene Kerne als Produkte, so dass das ursprüngliche Nuklid nicht aus seinen Töchtern bestimmt werden kann.
Den Physikern, die eines der schwersten Elemente synthetisieren wollen, stehen somit die an den Detektoren gesammelten Informationen zur Verfügung: Ort, Energie und Ankunftszeit eines Teilchens am Detektor und die seines Zerfalls. Die Physiker analysieren diese Daten und versuchen daraus zu schließen, dass es tatsächlich durch ein neues Element verursacht wurde und nicht durch ein anderes Nuklid als das behauptete entstanden sein kann. Oftmals reichen die bereitgestellten Daten nicht aus, um den Schluss zu ziehen, dass definitiv ein neues Element geschaffen wurde, und es gibt keine andere Erklärung für die beobachteten Effekte; Fehler bei der Interpretation der Daten wurden gemacht.
Geschichte
Superschwere Elemente werden durch Kernfusion erzeugt . Diese Fusionsreaktionen können in Abhängigkeit von der Anregungsenergie des erzeugten Verbindungskerns in "heiße" und "kalte" Fusion unterteilt werden. Bei heißen Fusionsreaktionen werden sehr leichte, hochenergetische Projektile auf sehr schwere Ziele ( Aktiniden ) beschleunigt , wodurch zusammengesetzte Kerne mit hoher Anregungsenergie (~40–50 MeV ) entstehen, die spalten oder alternativ mehrere (3 bis 5 .) verdampfen können ) Neutronen. Bei kalten Fusionsreaktionen (die schwerere Projektile verwenden, typischerweise aus der vierten Periode , und leichtere Ziele, normalerweise Blei und Wismut ) haben die erzeugten fusionierten Kerne eine relativ niedrige Anregungsenergie (~10–20 MeV), was die Wahrscheinlichkeit verringert, dass diese Produkte unterliegen Spaltungsreaktionen. Wenn die fusionierten Kerne auf den Grundzustand abkühlen , benötigen sie nur ein oder zwei Neutronen. Heiße Fusionsreaktionen neigen jedoch dazu, mehr neutronenreiche Produkte zu erzeugen, da die Aktiniden die höchsten Neutronen-zu-Protonen-Verhältnisse aller Elemente aufweisen, die derzeit in makroskopischen Mengen hergestellt werden können.
Ununennium und Unbinilium (Elemente 119 und 120) sind die Elemente mit den niedrigsten Ordnungszahlen, die noch nicht synthetisiert wurden. Versuche, sie zu synthetisieren, würden aufgrund der abnehmenden Wirkungsquerschnitte der Produktionsreaktionen und ihrer wahrscheinlich kurzen Halbwertszeiten , die voraussichtlich in der Größenordnung von Mikrosekunden liegen , die Grenzen der aktuellen Technologie überschreiten . Elemente jenseits von Unbiunium (Element 121) wären wahrscheinlich zu kurzlebig, um mit der aktuellen Technologie entdeckt zu werden: Sie würden innerhalb einer Mikrosekunde zerfallen, bevor sie die Detektoren erreichen. Die Möglichkeit der Detektion der Elemente 121 bis 124 hängt stark von dem verwendeten theoretischen Modell ab, da ihre Halbwertszeiten sehr nahe an der Grenze von einer Mikrosekunde vorhergesagt werden. Bisher kam wichtige Hilfe (gekennzeichnet als „Silberkugeln“) bei der Synthese von superschweren Elementen aus dem verformten Kernschal herum hassium -270 , die die Stabilität des umgebenden Kerns erhöht, und die Existenz der quasi-stabilen neutronenreiche Isotop calcium- 48 , das als Projektil verwendet werden könnte, um mehr neutronenreiche Isotope superschwerer Elemente zu erzeugen. Je neutronenreicher ein superschweres Nuklid ist, desto näher dürfte es der gesuchten Stabilitätsinsel sein . Trotzdem haben die synthetisierten Isotope immer noch weniger Neutronen als diejenigen, die auf der Insel der Stabilität erwartet werden. Darüber hinaus würde die Verwendung von Calcium-48 zur Synthese von Ununennium ein Ziel von Einsteinium -253 oder -254 erfordern, die in ausreichend großen Mengen nur sehr schwer herzustellen sind (derzeit sind nur Mikrogramm verfügbar; im Vergleich dazu sind Milligramm Berkelium und Californium verfügbar). Eine praktischere Herstellung weiterer superschwerer Elemente würde Projektile erfordern, die schwerer als 48 Ca sind.
Syntheseversuche
Vergangenheit
Die Synthese von Ununennium wurde erstmals 1985 versucht, indem ein Ziel von Einsteinium-254 mit Calcium-48- Ionen am SuperHILAC-Beschleuniger in Berkeley, Kalifornien, beschossen wurde:
-
254
99Es
+ 48
20Ca
→ 302
119Uue
* → keine Atome
Keine Atome identifiziert wurden, zu einem begrenzenden führenden Querschnitt von 300 nb . Spätere Berechnungen deuten darauf hin, dass der Wirkungsquerschnitt der 3n-Reaktion (die 299 Uue und drei Neutronen als Produkte ergeben würde) mit 0,5 pb tatsächlich sechshunderttausendmal niedriger als diese Obergrenze wäre.
Da Ununennium das leichteste unentdeckte Element ist, war es in den letzten Jahren Ziel von Syntheseexperimenten deutscher, russischer und japanischer Teams. Das russische Team am Joint Institute for Nuclear Research in Dubna, Russland, plante, ein Experiment vor 2012 durchzuführen, und es wurden keine Ergebnisse veröffentlicht, was stark darauf hindeutet, dass entweder das Experiment nicht durchgeführt wurde oder keine unennium-Atome identifiziert wurden. Von April bis September 2012 wurde am GSI Helmholtz-Zentrum für Schwerionenforschung in Darmstadt ein Versuch unternommen, die Isotope 295 Uue und 296 Uue zu synthetisieren , indem ein Ziel aus Berkelium -249 mit Titan -50 beschossen wurde . Basierend auf dem theoretisch vorhergesagten Wirkungsquerschnitt wurde erwartet, dass innerhalb von fünf Monaten nach Beginn des Experiments ein ununennium-Atom synthetisiert werden würde.
-
249
97Bk
+ 50
22Ti
→ 299
119Uue
* → 296
119Uue
+ 3 1
0
n
-
249
97Bk
+ 50
22Ti
→ 299
119Uue
* → 295
119Uue
+ 4 1
0
n
Das Experiment sollte ursprünglich bis November 2012 andauern, wurde jedoch vorzeitig abgebrochen , um das 249 Bk-Target zur Bestätigung der Synthese von Tennessin zu nutzen (und damit die Projektile auf 48 Ca zu ändern ). Diese Reaktion zwischen 249 Bk und 50 Ti wurde als die günstigste praktische Reaktion für die Bildung von Ununennium vorhergesagt, da sie ziemlich asymmetrisch, aber auch etwas kalt ist. (Die Reaktion zwischen 254 Es und 48 Ca wäre überlegen, aber Milligramm-Mengen von 254 Es für ein Target vorzubereiten ist schwierig.) Trotzdem teilt der notwendige Wechsel von der "Silberkugel" 48 Ca auf 50 Ti die erwartete Ausbeute an Unennium durch etwa zwanzig, da die Ausbeute stark von der Asymmetrie der Fusionsreaktion abhängt.
Aufgrund der vorhergesagten kurzen Halbwertszeiten verwendete das GSI-Team eine neue "schnelle" Elektronik, die Zerfallsereignisse innerhalb von Mikrosekunden registrieren kann. Es wurden keine unennium-Atome identifiziert, was auf einen Grenzquerschnitt von 65 fb schließen lässt. Der vorhergesagte tatsächliche Querschnitt beträgt etwa 40 fb, was an den Grenzen der aktuellen Technologie liegt. (Der niedrigste Rekordquerschnitt einer experimentell erfolgreichen Reaktion beträgt 30 fb für die Reaktion zwischen 209 Bi und 70 Zn, die Nihonium erzeugt .)
Gegenwärtig
Das Team von RIKEN in Wakō , Japan, begann im Juni 2018 damit, Curium- 248-Ziele mit einem Vanadium- 51-Strahl zu beschießen , um nach Element 119 zu suchen. Als Ziel wurde Curium anstelle von schwererem Berkelium oder Californium gewählt , da diese schwereren Ziele schwer zu erreichen sind vorbereiten. Es wird erwartet, dass die reduzierte Asymmetrie der Reaktion den Wirkungsquerschnitt ungefähr halbiert, was eine Empfindlichkeit "in der Größenordnung von mindestens 30 fb" erfordert. Die 248 Cm-Targets wurden vom Oak Ridge National Laboratory bereitgestellt, das das erforderliche 249 Bk-Target aus der Synthese von Tennessin (Element 117) in Dubna bereitgestellt hatte . Das RIKEN-Experiment wurde zunächst in einem Zyklotron durchgeführt, während es seine Linearbeschleuniger aufrüstete; die Aufrüstung wurde im Jahr 2020 abgeschlossen. Die Bombardierung kann mit beiden Maschinen fortgesetzt werden, bis das erste Ereignis beobachtet wird; das Experiment läuft derzeit mit Unterbrechungen für mindestens 100 Tage pro Jahr. Hideto En'yo , Direktor des RIKEN Nishina Centers, sagte voraus, dass die Elemente 119 und 120 wahrscheinlich bis 2022 entdeckt werden würden. Die Bemühungen des RIKEN-Teams werden vom Kaiser von Japan finanziert .
-
248
96Cm
+ 51
23V
→ 299
119Uue
* → 296
119Uue
+ 3 1
0
n
-
248
96Cm
+ 51
23V
→ 299
119Uue
* → 295
119Uue
+ 4 1
0
n
Es wird erwartet, dass die produzierten Isotope von Ununennium zwei Alpha-Zerfälle zu bekannten Isotopen von Moscovium ( 288 Mc bzw. 287 Mc) durchlaufen , was sie an einer bekannten Sequenz von fünf weiteren Alpha-Zerfällen verankern und ihre Produktion bestätigen würde. Der vorhergesagte Wirkungsquerschnitt für diese Reaktionen beträgt etwa 10 fb.
Geplant
Nach der behaupteten Synthese von 293 Og im Jahr 1999 am Lawrence Berkeley National Laboratory aus 208 Pb und 86 Kr wurden die analogen Reaktionen 209 Bi + 86 Kr und 208 Pb + 87 Rb für die Synthese von Element 119 und seinem damals unbekannten alpha . vorgeschlagen Zerfall Töchter , Elemente 117 , 115 und 113 . Die Zurücknahme dieser Ergebnisse im Jahr 2001 und neuere Berechnungen zu den Wirkungsquerschnitten für „kalte“ Fusionsreaktionen lassen diese Möglichkeit in Zweifel ziehen; zum Beispiel wird eine maximale Ausbeute von 2 fb für die Produktion von 294 Uue in der ersten Reaktion vorhergesagt . Radioaktive Ionenstrahlen können ein alternatives Verfahren darstellen, das ein Blei- oder Wismut- Target verwendet, und können die Produktion von neutronenreicheren Isotopen ermöglichen, sollten sie mit den erforderlichen Intensitäten verfügbar werden.
Das Team des Gemeinsamen Instituts für Kernforschung in Dubna , Russland, plante, mit einem neuen experimentellen Komplex neue Experimente zur Synthese von Ununennium unter Verwendung der 249 Bk + 50 Ti-Reaktion zu beginnen . Ab November 2019 wurden Ergebnisse frühestens Mitte 2021 erwartet.
Die Labore am RIKEN in Japan und am JINR in Russland sind für diese Experimente am besten geeignet, da sie weltweit die einzigen sind, in denen lange Strahlzeiten für Reaktionen mit geringen vorhergesagten Wirkungsquerschnitten zugänglich sind.
Benennung
Nach Mendelejews Nomenklatur für unbenannte und unentdeckte Elemente sollte Ununennium als Ekafrancium bezeichnet werden . Unter Verwendung der IUPAC- Empfehlungen von 1979 sollte das Element vorübergehend als ununennium (Symbol Uue ) bezeichnet werden, bis es entdeckt, die Entdeckung bestätigt und ein dauerhafter Name gewählt wird. Obwohl weit verbreitet in der chemischen Gemeinschaft auf allen Ebenen verwendet, aus der Chemie Klassenzimmer bis zum Fortgeschrittenen Lehrbüchern werden die Empfehlungen meist unter Wissenschaftlern ignoriert , die theoretisch oder experimentell auf superschweren Elementen arbeiten, die sie als „Element 119“, mit dem Symbol E119 , (119) oder 119 .
Vorhergesagte Eigenschaften
Kernstabilität und Isotope


Die Stabilität der Kerne nimmt mit zunehmender Ordnungszahl nach Curium , Element 96, stark ab, dessen Halbwertszeit vier Größenordnungen länger ist als die aller derzeit bekannten höher nummerierten Elemente. Alle Isotope mit einer Ordnungszahl über 101 unterliegen einem radioaktiven Zerfall mit Halbwertszeiten von weniger als 30 Stunden. Keine Elemente mit Ordnungszahlen über 82 (nach Blei ) haben stabile Isotope. Dennoch kommt es aus noch nicht gut verstandenen Gründen um die Ordnungszahlen 110 – 114 zu einer leichten Zunahme der Kernstabilität , was zur Entstehung der sogenannten „ Insel der Stabilität “ in der Kernphysik führt . Dieses Konzept, das von Glenn Seaborg , Professor an der University of California , vorgeschlagen wurde , erklärt, warum superschwere Elemente länger halten als vorhergesagt.
Die für 291–307 Uue vorhergesagten Alpha-Zerfalls-Halbwertszeiten liegen in der Größenordnung von Mikrosekunden. Die längste vorhergesagte Alpha-Zerfall-Halbwertszeit beträgt ~485 Mikrosekunden für das Isotop 294 Uue. Berücksichtigt man alle Zerfallsmodi, sinken die vorhergesagten Halbwertszeiten weiter auf nur zehn Mikrosekunden. Einige schwerere Isotope können stabiler sein; Fricke und Waber prognostizierten 1971 315 Uue als das stabilste Ununennium-Isotop. Dies hat Konsequenzen für die Synthese von Ununennium, da Isotope mit Halbwertszeiten unter einer Mikrosekunde zerfallen würden, bevor sie den Detektor erreichen, und die schwereren Isotope nicht durch die Kollision jedes bekannten verwendbaren Ziels und Projektilkerne. Dennoch zeigen neue theoretische Modelle, dass die erwartete Energielücke zwischen den Protonenorbitalen 2f 7/2 (gefüllt bei Element 114) und 2f 5/2 (gefüllt bei Element 120) kleiner als erwartet ist, sodass Element 114 nicht mehr zu eine stabile kugelförmige geschlossene Kernschale sein, und diese Energielücke kann die Stabilität der Elemente 119 und 120 erhöhen. Der nächste doppelt magische Kern wird nun um die sphärische 306 Ubb ( Element 122 ) erwartet, aber die erwartete niedrige Halbwertszeit und niedriger Produktionsquerschnitt dieses Nuklid macht seine Synthese herausfordernd.
Atomar und physikalisch
Als das erste Element der 8. Periode wird Ununennium als Alkalimetall vorhergesagt, das seinen Platz im Periodensystem unterhalb von Lithium , Natrium , Kalium , Rubidium , Cäsium und Francium einnimmt . Jedes dieser Elemente hat einen Valenzelektronen in der äußersten s-Orbital (Valenzelektronen Konfiguration n s 1 ), die leicht in chemischen Reaktionen verloren wird , um die Bildung +1 Oxidationszustand : so die Alkalimetalle sind sehr reaktive Elemente. Ununennium wird den Trend voraussichtlich fortsetzen und eine Valenzelektronenkonfiguration von 8s 1 aufweisen . Es wird daher erwartet, dass es sich ähnlich wie seine leichteren Artgenossen verhält ; es wird jedoch auch vorhergesagt, dass es sich in einigen Eigenschaften von den leichteren Alkalimetallen unterscheidet.
Der Hauptgrund für die vorhergesagten Unterschiede zwischen Ununennium und den anderen Alkalimetallen ist die Spin-Bahn-Wechselwirkung (SO) – die gegenseitige Wechselwirkung zwischen der Bewegung der Elektronen und dem Spin . Die SO-Wechselwirkung ist bei den superschweren Elementen besonders stark, weil sich ihre Elektronen schneller bewegen – mit Geschwindigkeiten vergleichbar der Lichtgeschwindigkeit – als die in leichteren Atomen. In unennium-Atomen senkt es die 7p- und 8s-Elektronenenergieniveaus und stabilisiert die entsprechenden Elektronen, aber zwei der 7p-Elektronenenergieniveaus sind stabiler als die anderen vier. Der Effekt wird Subshell Splitting genannt, da er die 7p-Subshell in stärker stabilisierte und weniger stabilisierte Teile aufspaltet. Computerchemiker verstehen die Aufspaltung als Änderung der zweiten ( azimutalen ) Quantenzahl l von 1 auf 1/2 bzw. 3/2 für die stärker stabilisierten bzw. weniger stabilisierten Teile der 7p-Unterschale. Somit wird das äußere 8s-Elektron von Ununennium stabilisiert und wird schwerer als erwartet zu entfernen, während die 7p 3/2- Elektronen entsprechend destabilisiert werden, was ihnen vielleicht ermöglicht, an chemischen Reaktionen teilzunehmen. Diese Stabilisierung des äußersten s-Orbitals (in Francium bereits von Bedeutung) ist der Schlüsselfaktor, der die Chemie von Ununennium beeinflusst und bewirkt, dass sich alle Trends bei den atomaren und molekularen Eigenschaften von Alkalimetallen nach Cäsium umkehren.
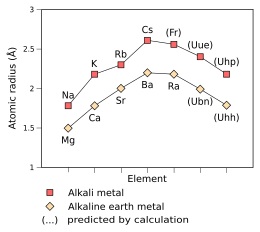
Empirische (Na–Cs, Mg–Ra) und vorhergesagte (Fr–Uhp, Ubn–Uhh) Atomradien der Alkali- und Erdalkalimetalle von der dritten bis zur neunten Periode , gemessen in Angström
|

Empirische (Na–Cs), semiempirische (Fr) und vorhergesagte (Uue) Elektronenaffinitäten der Alkalimetalle von der dritten bis zur achten Periode , gemessen in Elektronenvolt . Sie nehmen von Li auf Cs ab, aber der Fr-Wert,492 ± 10 meV , ist 20 meV höher als die von Cs, und die von Uue ist mit 662 meV noch viel höher.
|
Aufgrund der Stabilisierung seines äußeren 8s-Elektrons wird die erste Ionisierungsenergie von Ununennium – die Energie, die erforderlich ist, um ein Elektron aus einem neutralen Atom zu entfernen – mit 4,53 eV höher als die der bekannten Alkalimetalle ab Kalium vorhergesagt. Dieser Effekt ist so groß, dass für Unbiunium (Element 121) eine niedrigere Ionisierungsenergie von 4,45 eV vorhergesagt wird, so dass das Alkalimetall in Periode 8 nicht die niedrigste Ionisationsenergie in dieser Periode aufweisen würde, wie dies für alle vorherigen Perioden der Fall war. Es wird erwartet, dass die Elektronenaffinität von Ununennium weit höher ist als die von Cäsium und Francium; In der Tat wird erwartet, dass Ununennium eine höhere Elektronenaffinität hat als alle leichteren Alkalimetalle mit etwa 0,662 eV, nahe der von Kobalt (0,662 eV) und Chrom (0,676 eV). Relativistische Effekte verursachen auch einen sehr starken Abfall der Polarisierbarkeit von Unennium auf 169,7 au Tatsächlich ist die statische Dipolpolarisierbarkeit (α D ) von Ununennium, eine Größe, für die die Auswirkungen der Relativitätstheorie proportional zum Quadrat der Ordnungszahl des Elements sind, berechnet als klein und ähnlich dem von Natrium.
Das Elektron des wasserstoffähnlichen Ununennium-Atoms – oxidiert, sodass es nur ein Elektron hat, Uue 118+ – bewegt sich voraussichtlich so schnell, dass seine Masse das 1,99-fache der Masse eines nicht bewegten Elektrons beträgt, ein Merkmal, das von den relativistischen Effekten herrührt . Zum Vergleich: Für wasserstoffähnliches Francium beträgt der Wert 1,29 und für wasserstoffähnliches Cäsium 1,091. Nach einfachen Extrapolationen der Relativitätsgesetze deutet dies indirekt auf die Kontraktion des Atomradius auf etwa 240 pm hin , sehr nahe an der von Rubidium (247 pm); auch der metallische Radius wird entsprechend auf 260 pm abgesenkt. Der Ionenradius von Uue + wird voraussichtlich 180 pm betragen .
Ununennium wird vorhergesagt , einen Schmelzpunkt zwischen 0 ° C hat , und 30 ° C: damit es eine sein kann Flüssigkeit bei Raumtemperatur. Es ist nicht bekannt, ob dies den Trend sinkender Schmelzpunkte in der Gruppe fortsetzt, da der Schmelzpunkt von Cäsium bei 28,5 °C liegt und der von Francium auf etwa 8,0 °C geschätzt wird. Der Siedepunkt von Ununennium wird bei etwa 630 °C erwartet, ähnlich dem von Francium, der auf etwa 620 °C geschätzt wird; dies ist niedriger als der Siedepunkt von Cäsium von 671 °C. Die Dichte von Ununennium wurde unterschiedlich vorhergesagt zwischen 3 und 4 g/cm 3 , was den Trend der zunehmenden Dichte in der Gruppe fortsetzt: Die Dichte von Francium wird auf 2,48 g/cm 3 geschätzt , und die von Cäsium ist bekannt für 1,93 g / cm 3 .
Chemisch
| Verbindung | Bindungslänge (Å) | Bindungsdissoziationsenergie (kJ/mol) |
|---|---|---|
| Li 2 | 2.673 | 101,9 |
| Na 2 | 3.079 | 72,04 |
| K 2 | 3.924 | 53,25 |
| Rb 2 | 4.210 | 47,77 |
| Cs 2 | 4.648 | 43,66 |
| Fr 2 | ~ 4.61 | ~ 42,1 |
| Uue 2 | ~ 4,27 | ~ 53,4 |
Es wird vorhergesagt, dass die Chemie von Ununennium der der Alkalimetalle ähnlich ist, aber es würde sich wahrscheinlich eher wie Kalium oder Rubidium als Cäsium oder Francium verhalten. Dies ist auf relativistische Effekte zurückzuführen, da periodische Trends ohne sie vorhersagen würden, dass Unennium noch reaktiver ist als Cäsium und Francium. Diese verringerte Reaktivität ist auf die relativistische Stabilisierung des Valenzelektrons von Ununennium zurückzuführen, wodurch die erste Ionisierungsenergie von Unennium erhöht und die metallischen und ionischen Radien verringert werden ; dieser Effekt ist bereits für Francium zu sehen.
Die Chemie von Ununennium in der Oxidationsstufe +1 sollte der Chemie von Rubidium ähnlicher sein als der von Francium. Andererseits wird vorhergesagt, dass der Ionenradius des Uue + -Ions größer ist als der von Rb + , da die 7p-Orbitale destabilisiert und somit größer sind als die p-Orbitale der unteren Schalen. Ununennium kann neben der Oxidationsstufe +1, die für die anderen Alkalimetalle charakteristisch ist und auch die Hauptoxidationsstufe aller bekannten Alkalimetalle ist, auch die Oxidationsstufe +3 aufweisen , die bei keinem anderen Alkalimetall vorkommt: dies liegt an der Destabilisierung und Expansion des 7p 3/2- Spinors, was dazu führt, dass seine äußersten Elektronen eine niedrigere Ionisierungsenergie haben, als man es sonst erwarten würde. Von vielen Ununennium-Verbindungen wird aufgrund der Beteiligung der 7p 3/2- Elektronen an der Bindung erwartet, dass sie einen starken kovalenten Charakter haben : Dieser Effekt wird in geringerem Maße auch bei Francium beobachtet, das einen Beitrag von etwa 6p 3/2 zur Bindung zeigt in Francium Superoxid (fRO 2 ). Anstatt also, dass Ununennium das elektropositivste Element ist, wie eine einfache Extrapolation zu zeigen scheint, behält Cäsium stattdessen diese Position bei, wobei die Elektronegativität von Ununennium höchstwahrscheinlich nahe der von Natrium liegt (0,93 auf der Pauling-Skala). Das Standardreduktionspotential des Uue + /Uue-Paares wird mit -2,9 V vorhergesagt, das gleiche wie das des Fr + /Fr-Paares und knapp über dem des K + /K-Paares bei -2,931 V.
Bindungslängen und Bindungsdissoziationsenergien von MAu (M = ein Alkalimetall). Alle Daten werden vorhergesagt, mit Ausnahme der Bindungsdissoziationsenergien von KAu, RbAu und CsAu. Verbindung Bindungslänge (Å) Bindungsdissoziationsenergie (kJ/mol) KAu 2.856 2,75 RbAu 2.967 2.48 CsAu 3.050 2,53 FrAu 3.097 2,75 UueAu 3.074 2.44
In der Gasphase und bei sehr niedrigen Temperaturen in der kondensierten Phase bilden die Alkalimetalle kovalent gebundene zweiatomige Moleküle. Die Metall-Metall- Bindungslängen in diesen M 2 -Molekülen nehmen aufgrund der oben erwähnten relativistischen Effekte, die das 8s-Orbital stabilisieren, von Li 2 zu Cs 2 abwärts zu , nehmen dann aber bis Uue 2 ab . Der gegenteilige Trend zeigt sich für die Metall-Metall- Bindungsdissoziationsenergien . Die Uue-Uue-Bindung sollte etwas stärker sein als die K-K-Bindung. Aus dieser M 2 Dissoziationsenergie, die Sublimationswärme (Δ H sub ) von Ununennium vorhergesagt wird , 94 kJ / mol sein (der Wert für Francium sollte etwa 77 kJ / mol betragen).
Es wird erwartet, dass das UueF-Molekül aufgrund der hohen Elektronenaffinität von Ununennium einen signifikanten kovalenten Charakter hat. Die Bindung in UueF besteht hauptsächlich zwischen einem 7p-Orbital auf Ununennium und einem 2p-Orbital auf Fluor, mit geringeren Beiträgen vom 2s-Orbital von Fluor und dem 8s, 6d z 2 und den beiden anderen 7p-Orbitalen von Unennium. Dies unterscheidet sich stark vom Verhalten von s-Block-Elementen sowie von Gold und Quecksilber , bei denen die s-Orbitale (manchmal gemischt mit d-Orbitalen) an der Bindung beteiligt sind. Die Uue-F-Bindung wird aufgrund der Aufspaltung des 7p-Orbitals in 7p 1 / 2- und 7p 3/2- Spinoren relativistisch erweitert , wodurch die Bindungselektronen in das größte Orbital, gemessen an der radialen Ausdehnung, gezwungen werden: eine ähnliche Ausdehnung der Bindungslänge findet sich in die Hydride At H und TsH. Die Uue-Au-Bindung sollte die schwächste aller Bindungen zwischen Gold und einem Alkalimetall sein, aber dennoch stabil sein. Man erhält hochgerechneten mittlere Adsorptionsenthalpien (-Δ H ads ) von 106 kJ / mol auf Gold (der Francium Wert sollte 136 kJ / mol betragen), 76 kJ / mol auf Platin , und 63 kJ / mol auf Silber , die kleinsten aller Alkalimetalle, die zeigen, dass es möglich wäre, die chromatographische Adsorption von Ununennium an Oberflächen aus Edelmetallen zu untersuchen . Die Enthalpie der Adsorption von Ununennium auf einer Teflonoberfläche vorhergesagt wird , 17,6 kJ / mol ist, die die niedrigste unter den Alkalimetallen wären: Diese Information würde für zukünftige chemische Experimente auf Ununennium sehr nützlich sein. Der Δ H sub und -Δ H Anzeigen Werte werden für die Alkalimetalle nicht proportional verwandt, da sie in entgegengesetzten Richtungen , wie Ordnungszahl zunimmt ändern.
Siehe auch
Anmerkungen
Verweise
Literaturverzeichnis
- Audi, G.; Kondev, FG; Wang, M.; Huang, WJ; Naimi, S. (2017). "Die NUBASE2016 Bewertung der nuklearen Eigenschaften" (PDF) . Chinesische Physik C . 41 (3): 030001. Bibcode : 2017ChPhC..41c0001A . doi : 10.1088/1674-1137/41/3/030001 .
- Beiser, A. (2003). Konzepte der modernen Physik (6. Aufl.). McGraw-Hill. ISBN 978-0-07-244848-1. OCLC 48965418 .
- Hoffmann, DC ; Ghiorso, A. ; Seaborg, GT (2000). Die Transuranium-Leute: Die Insider-Geschichte . Weltwissenschaftlich . ISBN 978-1-78-326244-1.
- Kragh, H. (2018). Von transuranischen zu superschweren Elementen: Eine Geschichte von Streit und Schöpfung . Springer . ISBN 978-3-319-75813-8.
- Zagrebaev, V.; Karpow, A.; Greiner, W. (2013). "Zukunft der superschweren Elementforschung: Welche Kerne könnten in den nächsten Jahren synthetisiert werden?". Zeitschrift für Physik: Konferenzreihe . 420 (1). 012001. arXiv : 1207.5700 . Bibcode : 2013JPhCS.420a2001Z . doi : 10.1088/1742-6596/420/1/012001 . ISSN 1742-6588 . S2CID 55434734 .
Externe Links
-
 Die Wörterbuchdefinition von ununennium bei Wiktionary
Die Wörterbuchdefinition von ununennium bei Wiktionary


