Acyl-CoA - Acyl-CoA
Acyl-CoA ist eine Gruppe von Coenzymen , die Fettsäuren metabolisieren . Acyl-CoAs sind anfällig für Beta-Oxidation und bilden schließlich Acetyl-CoA . Das Acetyl-CoA tritt in den Zitronensäurezyklus ein und bildet schließlich mehrere Äquivalente von ATP . Auf diese Weise werden Fette zu ATP, dem universellen biochemischen Energieträger, umgewandelt.
Funktionen
Fettsäureaktivierung
Fette werden durch Umwandlung in Acyl-CoA abgebaut. Diese Umwandlung ist eine Reaktion auf hohen Energiebedarf, wie zum Beispiel Sport. Der oxidative Abbau von Fettsäuren ist ein zweistufiger Prozess, der durch die Acyl-CoA-Synthetase katalysiert wird . Fettsäuren werden in ihr Acylphosphat umgewandelt, die Vorstufe von Acyl-CoA. Letztere Umwandlung wird durch Acyl-CoA-Synthase vermittelt.
- Acyl-P + HS-CoA → Acyl-S-CoA + P i + H +
Abhängig von der Kettenlänge der Fettsäure werden drei Arten von Acyl-CoA-Synthasen verwendet. Zum Beispiel sind die Substrate für die mittelkettige Acyl-CoA-Synthase 4-11 Kohlenstoff-Fettsäuren. Das Enzym Acyl-CoA-Thioesterase nimmt aus dem Acyl-CoA eine freie Fettsäure und Coenzym A auf.
Beta-Oxidation von Acyl-CoA
Der zweite Schritt des Fettsäureabbaus ist die Beta-Oxidation. Beta-Oxidation findet in Mitochondrien statt. Nach der Bildung im Zytosol wird Acyl-CoA in die Mitochondrien, den Ort der Beta-Oxidation, transportiert. Der Transport von Acyl-CoA in die Mitochondrien erfordert Carnitinpalmitoyltransferase 1 (CPT1), die Acyl-CoA in Acylcarnitin umwandelt, das in die mitochondriale Matrix transportiert wird. Sobald es sich in der Matrix befindet, wird Acylcarnitin durch CPT2 wieder in Acyl-CoA umgewandelt. Die Beta-Oxidation kann jetzt beginnen, da sich Acyl-CoA in den Mitochondrien befindet.
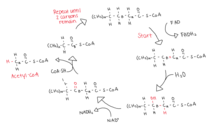
Die Beta-Oxidation von Acyl-CoA erfolgt in vier Schritten.
1. Acyl-CoA-Dehydrogenase katalysiert die Dehydrierung des Acyl-CoA, wodurch eine Doppelbindung zwischen den Alpha- und Beta-Kohlenstoffatomen entsteht. FAD ist der Wasserstoffakzeptor und ergibt FADH2.
2. Enoyl-CoA-Hydrase katalysiert die Addition von Wasser über die neu gebildete Doppelbindung, um einen Alkohol herzustellen.
3. 3-Hydroxyacyl-CoA-Dehydrogenase oxidiert die Alkoholgruppe zu einem Keton. NADH wird aus NAD+ hergestellt .
4. Thiolase spaltet zwischen Alpha-Kohlenstoff und Keton, um ein Molekül Acetyl-CoA und das Acyl-CoA freizusetzen, das jetzt 2 Kohlenstoffe kürzer ist.
Dieser vierstufige Prozess wiederholt sich, bis Acyl-CoA alle Kohlenstoffe aus der Kette entfernt hat und nur Acetyl-CoA zurückbleibt. Während eines Zyklus der Beta-Oxidation erzeugt Acyl-CoA ein Molekül Acetyl-CoA, FADH2 und NADH. Acetyl-CoA wird dann im Zitronensäurezyklus verwendet, während FADH2 und NADH an die Elektronentransportkette geschickt werden . Diese Zwischenprodukte liefern alle Energie für den Körper, da sie schließlich in ATP umgewandelt werden .
Beta-Oxidation sowie Alpha-Oxidation finden auch im Peroxisom statt . Das Peroxisom übernimmt die Beta-Oxidation von Fettsäuren mit mehr als 20 Kohlenstoffatomen in ihrer Kette, da das Peroxisom sehr langkettige Acyl-CoA-Synthetasen enthält . Diese Enzyme sind besser ausgestattet, um Acyl-CoA mit langen Ketten zu oxidieren, die die Mitochondrien nicht verarbeiten können.
Beispiel mit Stearinsäure
Beta-Oxidation entfernt 2 Kohlenstoffe gleichzeitig, so dass bei der Oxidation einer 18-Kohlenstoff-Fettsäure wie Stearinsäure 8 Zyklen ablaufen müssen, um Acyl-CoA vollständig abzubauen. Dies erzeugt 9 Acetyl-CoA mit jeweils 2 Kohlenstoffen, 8 FADH2 und 8 NADH.
Klinische Bedeutung
Der Herzmuskel verstoffwechselt hauptsächlich Fett zur Energiegewinnung und der Acyl-CoA-Stoffwechsel wurde als ein kritisches Molekül bei einem Herzmuskelpumpenversagen im Frühstadium identifiziert.
Der zelluläre Acyl-CoA-Gehalt korreliert mit der Insulinresistenz, was darauf hindeutet, dass er Lipotoxizität in nicht adipösen Geweben vermitteln kann. Acyl-CoA: Diacylglycerolacyltransferase (DGAT) spielt als Schlüsselenzym der Triglyceridbiosynthese eine wichtige Rolle im Energiestoffwechsel. Die synthetische Rolle von DGAT im Fettgewebe wie Leber und Darm, wo die endogenen Spiegel seiner Aktivität und Triglyceridsynthese hoch und vergleichsweise klar sind. Außerdem können Änderungen des Aktivitätsniveaus Änderungen der systemischen Insulinsensitivität und der Energiehomöostase verursachen.
Eine seltene Krankheit namens multipler Acyl-CoA-Dehydrogenase-Mangel (MADD) ist eine Störung des Fettsäurestoffwechsels. Acyl-CoA ist wichtig, da dieses Enzym dabei hilft, Acyl-CoA aus freien Fettsäuren herzustellen, und dies aktiviert den Stoffwechsel der Fettsäure. Diese beeinträchtigte Fettsäureoxidation führt zu vielen verschiedenen Symptomen, darunter schwere Symptome wie Kardiomyopathie und Lebererkrankungen und leichte Symptome wie episodischer Stoffwechselabbau, Muskelschwäche und Atemversagen. MADD ist eine genetische Störung, die durch eine Mutation in den ETFA-, ETFB- und ETFDH-Genen verursacht wird. MADD ist als „autosomal-rezessive Störung“ bekannt, denn um diese Störung zu bekommen, muss man dieses rezessive Gen von beiden Elternteilen erhalten.
Siehe auch
Verweise
Externe Links
- Acyl+Coenzym+A in der US National Library of Medicine Medical Subject Headings (MeSH)