Cadmiumarsenid - Cadmium arsenide
 Cd 3 As 2 -Kristalle mit (112)- und (400)-Orientierung
|
|

STM- Bild der (112)-Oberfläche
|
|
| Namen | |
|---|---|
| Andere Namen
Tricadmiumdiarsenid
|
|
| Bezeichner | |
|
3D-Modell ( JSmol )
|
|
| ChemSpider | |
| ECHA-InfoCard |
100.031.336 |
| EG-Nummer | |
|
PubChem- CID
|
|
|
CompTox-Dashboard ( EPA )
|
|
|
|
|
|
| Eigenschaften | |
| CD 3 als 2 | |
| Molmasse | 487,08 g/mol |
| Aussehen | einfarbig, dunkelgrau |
| Dichte | 3.031 |
| Schmelzpunkt | 716 °C (1.321 °F; 989 K) |
| zersetzt sich in Wasser | |
| Struktur | |
| Tetragonal, tI160 | |
| I4 1 cd, Nr. 110 | |
|
a = 1,26512(3) nm, c = 2,54435(4) nm
|
|
| Gefahren | |
| GHS-Piktogramme |
   
|
| GHS-Signalwort | Achtung |
| H301 , H312 , H330 , H350 , H400 , H410 | |
| P201 , P202 , P260 , P261 , P264 , P270 , P271 , P273 , P280 , P281 , P284 , P301 + 310 , P302 + 352 , P304 + 340 , P308 + 313 , P310 , P311 , P312 , P320 , P321 , P322 , P330 , P363 , P391 , P403+233 | |
| NFPA 704 (Feuerdiamant) | |
| Tödliche Dosis oder Konzentration (LD, LC): | |
|
LD 50 ( mediane Dosis )
|
keine Daten |
| NIOSH (US-Grenzwerte für die Gesundheitsbelastung): | |
|
PEL (zulässig)
|
[1910.1027] TWA 0,005 mg/m 3 (als Cd) |
|
REL (empfohlen)
|
Ca |
|
IDLH (unmittelbare Gefahr)
|
Ca [9 mg/m 3 (als Cd)] |
|
Sofern nicht anders angegeben, beziehen sich die Daten auf Materialien im Standardzustand (bei 25 °C [77 °F], 100 kPa). |
|
| Infobox-Referenzen | |
Cadmiumarsenid ( Cd 3 As 2 ) ist ein anorganisches Halbmetall der II-V- Familie. Es zeigt den Nernst-Effekt .
Eigenschaften
Thermal
Cd 3 As 2 dissoziiert je nach Reaktion zwischen 220 und 280 ° C.
- 2 Cd 3 As 2 (s) → 6 Cd (g) + As 4 (g)
Aufgrund der Unregelmäßigkeit der Partialdrücke mit der Temperatur wurde eine Energiebarriere für die nichtstöchiometrische Verdampfung von Arsen gefunden. Der Bereich der Energielücke reicht von 0,5 bis 0,6 eV. Cd 3 As 2 schmilzt bei 716 °C und wechselt die Phase bei 615 °C/
Phasenübergang
Reines Cadmiumarsenid durchläuft bei hohen Temperaturen mehrere Phasenübergänge, wodurch Phasen mit den Bezeichnungen α (stabil), α', α” (metastabil) und β bezeichnet werden. Bei 593° tritt der polymorphe Übergang α → β auf.
- α-Cd 3 As 2 ↔ α'-Cd 3 As 2 tritt bei ~500 K auf.
- α'-Cd 3 As 2 α''-Cd 3 As 2 tritt bei ~742 K auf und ist ein regelmäßiger Phasenübergang erster Ordnung mit ausgeprägter Hystereseschleife.
- α”-Cd 3 As 2 ↔ β-Cd 3 As 2 tritt bei 868 K auf.
Zur Bestimmung der Gitterparameter von Cd 3 As 2 zwischen 23 und 700 °C wurde Einkristall-Röntgenbeugung verwendet . Der Übergang α → α′ erfolgt langsam und ist daher höchstwahrscheinlich eine Zwischenphase. Der Übergang α′ → α″ erfolgt viel schneller als α → α′ und hat eine sehr kleine thermische Hysterese . Dieser Übergang führt zu einer Änderung der vierfachen Achse der tetragonalen Zelle, was zu einer Kristallzwillingsbildung führt . Die Breite der Schleife ist unabhängig von der Heizrate, wird jedoch nach mehreren Temperaturzyklen schmaler.
Elektronisch
Die Verbindung Cadmiumarsenid hat einen niedrigeren Dampfdruck (0,8 atm) als Cadmium und Arsen getrennt. Cadmiumarsenid zersetzt sich nicht, wenn es verdampft und erneut kondensiert wird. Trägerkonzentration in Cd 3 As 2 beträgt normalerweise (1–4) × 10 18 Elektronen / cm 3 . Trotz hoher Ladungsträgerkonzentrationen sind auch die Elektronenbeweglichkeiten sehr hoch (bis zu 10.000 cm 2 /(V·s) bei Raumtemperatur).
Im Jahr 2014 wurde gezeigt, dass Cd 3 As 2 ein zu Graphen analoges halbmetallisches Material ist , das in einer 3D-Form vorliegt und viel einfacher zu elektronischen Geräten geformt werden sollte. Dreidimensionale (3D) topologische Dirac-Halbmetalle (TDSs) sind Bulk-Analoga von Graphen , die auch in ihrer elektronischen Struktur eine nicht-triviale Topologie aufweisen, die Ähnlichkeiten mit topologischen Isolatoren aufweist. Darüber hinaus kann ein TDS möglicherweise in andere exotische Phasen (wie Weyl-Halbmetalle, Axionenisolatoren und topologische Supraleiter ) getrieben werden. Winkelaufgelöste Photoemissionsspektroskopie zeigte ein Paar von 3D- Dirac-Fermionen in Cd 3 As 2 . Im Vergleich zu anderen 3D-TDSs, z. B. β-Cristobalit BiO
2und Na3Bi , Cd 3 As 2 ist stabil und hat viel höhere Fermigeschwindigkeiten . In-situ-Dotierung wurde verwendet, um seine Fermi-Energie abzustimmen.
Dirigieren
Cadmiumarsenid ist ein II-V- Halbleiter , der eine entartete intrinsische Leitfähigkeit des n-Typ-Halbleiters mit einer großen Mobilität, einer geringen effektiven Masse und einem stark nicht parabolischen Leitungsband aufweist, oder ein Halbleiter mit schmaler Lücke . Es zeigt eine invertierte Bandstruktur, und die optische Energielücke, z. B. , ist kleiner als 0. Bei der Abscheidung durch thermische Verdampfung (Abscheidung) zeigte Cadmiumarsenid den Schottky- ( thermionische Emission ) und den Poole-Frenkel-Effekt bei hohen elektrischen Feldern.
Magnetwiderstand
Cadmiumarsenid zeigt selbst bei der relativ hohen Temperatur von 100K sehr starke Quantenoszillationen im Widerstand. Dies macht es zum Testen kryomagnetischer Systeme nützlich, da das Vorhandensein eines so starken Signals ein klarer Indikator für die Funktion ist
Vorbereitung
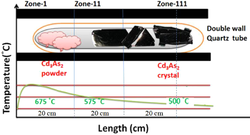
Cadmiumarsenid kann als amorphes halbleitendes Glas hergestellt werden . Laut Hiscocks und Elliot wurde Cadmiumarsenid aus Cadmiummetall hergestellt, das eine Reinheit von 6 N von Kock-Light Laboratories Limited aufwies. Hoboken lieferte β-Arsen mit einer Reinheit von 99,999 %. Stöchiometrische Anteile der Elemente Cadmium und Arsen wurden gemeinsam erhitzt. Das Abtrennen war schwierig und langwierig, da die Barren an der Kieselsäure hafteten und brachen. Es wurde ein flüssigkeitsgekapseltes Stockbarger-Wachstum geschaffen. Kristalle werden aus flüchtigen Schmelzen in flüssiger Verkapselung gezogen. Die Schmelze wird mit einer Schicht aus inerter Flüssigkeit, üblicherweise B 2 O 3 , bedeckt , und es wird ein Inertgasdruck größer als der Gleichgewichtsdampfdruck angelegt. Dadurch wird die Verdunstung aus der Schmelze eliminiert, wodurch ein Impfen und Ziehen durch die B 2 O 3 -Schicht ermöglicht wird.
Kristallstruktur
Die Elementarzelle von Cd 3 As 2 ist tetragonal. Die Arsenionen sind kubisch dicht gepackt und die Cadmiumionen sind tetraedrisch koordiniert. Die freien Tetraederplätze provozierten Forschungen von Stackelberg und Paulus (1935), die die Primärstruktur bestimmten. Jedes Arsen-Ion ist an sechs der acht Ecken eines verzerrten Würfels von Cadmium-Ionen umgeben und die beiden freien Plätze lagen an den Diagonalen.
Die Kristallstruktur von Cadmiumarsenid ist der von Zinkphosphid (Zn 3 P 2 ) , Zinkarsenid (Zn 3 As 2 ) und Cadmiumphosphid (Cd 3 P 2 ) sehr ähnlich . Diese Verbindungen des quaternären Systems Zn-Cd-P-As zeigen eine vollständig kontinuierliche feste Lösung.
Nernst-Effekt
Cadmiumarsenid wird in Infrarotdetektoren mit Nernst-Effekt und in Dünnschicht- Staudrucksensoren verwendet . Es kann auch zur Herstellung von Magnetowiderständen und in Fotodetektoren verwendet werden .
Cadmiumarsenid kann als Dotierstoff für HgCdTe verwendet werden .