Kobalt(II,III)-oxid - Cobalt(II,III) oxide

|
|
|
|
| Namen | |
|---|---|
|
IUPAC-Name
Kobalt(II)-Dikobalt(III)-Oxid
|
|
| Andere Namen
Kobaltoxid, Kobalt(II,III)-oxid, Kobaltsäureoxid, Trikobalttetroxid
|
|
| Bezeichner | |
|
3D-Modell ( JSmol )
|
|
| ChemSpider | |
| ECHA-Infokarte |
100.013.780 |
| EG-Nummer | |
|
PubChem- CID
|
|
| RTECS-Nummer | |
| UNII | |
|
CompTox-Dashboard ( EPA )
|
|
|
|
|
|
| Eigenschaften | |
| Co 3 O 4 CoO.Co 2 O 3 |
|
| Molmasse | 240,80 g/mol |
| Aussehen | schwarzer Feststoff |
| Dichte | 6,07 g / cm 3 |
| Schmelzpunkt | 895 °C (1.643 °F; 1.168 K) |
| Siedepunkt | 900 °C (1.650 °F; 1.170 K) (zersetzt) |
| Unlöslich | |
| Löslichkeit | löslich (mit Abbau) in Säuren und Laugen |
| +7380·10 -6 cm 3 /mol | |
| Struktur | |
| kubisch | |
| Fd 3 m, Nr. 227 | |
| Gefahren | |
| GHS-Piktogramme |
 
|
| GHS-Signalwort | Achtung |
| H317 , H334 , H350 , H411 | |
| P261 , P273 , P284 , P304+340 , P342+311 | |
| NFPA 704 (Feuerdiamant) | |
|
Sofern nicht anders angegeben, beziehen sich die Daten auf Materialien im Standardzustand (bei 25 °C [77 °F], 100 kPa). |
|
|
|
|
| Infobox-Referenzen | |
Kobalt(II,III)-oxid ist eine anorganische Verbindung mit der Formel Co 3 O 4 . Es ist eines von zwei gut charakterisierten Kobaltoxiden . Es ist ein schwarzer antiferromagnetischer Festkörper. Als gemischtvalente Verbindung wird seine Formel manchmal als Co II Co III 2 O 4 und manchmal als CoO•Co 2 O 3 geschrieben .
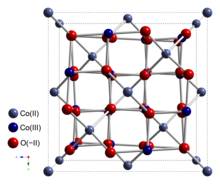
Struktur
Co 3 O 4 nimmt den normalen Spinellstruktur , mit Co 2+ -Ionen in tetraedrischen Zwischenräumen und Co 3+ -Ionen in den Oktaederlücken des kubischen dicht gepackten Gitters von Oxid - Anionen.
 |
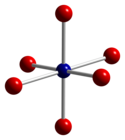 |
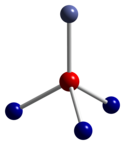
|
| tetraedrische Koordinationsgeometrie von Co(II) | verzerrte oktaedrische Koordinationsgeometrie von Co(III) | verzerrt tetraedrische Koordinationsgeometrie von O |
Synthese
Kobalt(II)-oxid , CoO, wandelt sich beim Erhitzen auf etwa 600–700 °C in Luft in Co 3 O 4 um. Oberhalb von 900 °C ist CoO stabil. Diese Reaktion wird durch das folgende Gleichgewicht beschrieben:
- 2 Co 3 O 4 ⇌ 6 CoO + O 2
Anwendungen
Kobalt(II,III)-Oxid wird alternativ zu Kobalt(II)-Oxid als blauer Farbstoff für Keramik- Email und Glas verwendet.
Kobalt(II,III)-oxid wird in einigen Lithium-Ionen-Batterien als Elektrode verwendet , möglicherweise in Form von Kobaltoxid-Nanopartikeln .
Sicherheit
Kobaltverbindungen sind in großen Mengen potenziell giftig.

