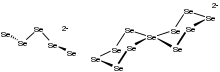
Polyselenid - Polyselenide
In der Chemie , ein Polyselenid bezieht sich gewöhnlich auf Anionen der Formel (Se n ) 2- , wobei das Atom Ich Symbol für das Element ist Selen . Viele Hauptgruppen- und Übergangsmetalle bilden mit Polyselenidanionen Komplexe.
Vorbereitung
Konzeptionell werden Polyselenide durch Deprotonierung von Polyselenanen H 2 Se n abgeleitet , aber solche neutralen Spezies werden leicht erhalten oder sind instabil. Stattdessen werden, analog zur Herstellung vieler Zintl-Ionen , Polyselenide durch Reduktion von elementarem Se mit Alkalimetallen hergestellt. Solche Reaktionen können durch Erhitzen einer Mischung der Feststoffe oder durch Auflösen von Se-Metall in Aminlösungen von Alkalimetallen durchgeführt werden. Die Synthese kann auch in hochsiedenden, polaren, aprotischen Lösungsmitteln wie DMF, HMPA und NMP durchgeführt werden. Diese Reaktionen scheinen durch die anfängliche Bildung des Alkalimetallselenids abzulaufen, gefolgt von der Reaktion des letzteren mit zusätzlichem Selen:
- 2 Na + 'Se → Na 2 Se
- Na 2 Se + n Se → Na 2 Se n +1
Einmal erzeugt, können Alkalimetallpolyselenide durch Behandlung mit Kryptandenliganden oder durch Ionenaustausch mit Quatsalzen in lipophile Salze umgewandelt werden .
- Na 2 Se n + 2 R 4 NCl → (R 4 N) 2 Se n + 2 NaCl
Strukturen
Salze von Polyseleniden wurden oft durch Röntgenkristallographie charakterisiert . Polyselenidsalze weisen im Allgemeinen offene Ketten auf, die eine Zick-Zack-Konformation annehmen. In seltenen Fällen werden cyclische Strukturen wie in Li 2 Se 5 beobachtet , das ein quadratisch-planares Se-Zentrum aufweist. Hochauflösende Festkörper- 77 Se-NMR-Spektren von [NMe 4 ] 2 Se 6 zeigen drei Selenzentren . Einkristall-Röntgenstrukturbestimmung der beiden Salze unterstützt die NMR-Daten.
Reaktivität
Polyselenide neigen zur Zersetzung an der Luft, wobei sie in diesem Fall wieder zu elementarem Selen oxidiert werden.
-
Se2−
n + 2 H + + 1 ⁄ 2 O 2 → n Se + H 2 O
Als Liganden in Koordinationskomplexen sind Polyselenide im Allgemeinen zweizähnig. Komplexe von Penta-, Tetra- und Triselenidliganden sind bekannt. Ein Beispiel ist der spirocyclische [Zn(Se 4 ) 2 ] 2- .
Siehe auch
Verweise
- ^ Greenwood, Norman N .; Earnshaw, Alan (1997). Chemie der Elemente (2. Aufl.). Butterworth-Heinemann . P. 763-765. ISBN 978-0-08-037941-8.
- ^ Thompson, D.; Boudjouk, P.A. (1988). „Bequeme Synthese von Alkalimetallseleniden und Diseleniden in Tetrahydrofuran und die Reaktivitätsunterschiede dieser Salze gegenüber organischen Bromiden“. Zeitschrift für Organische Chemie . 53 : 2109-2112. doi : 10.1021/jo00244a051 .
- ^ Kolis, J. "Coordination Chemistry of Polychalkogen Anions and Transition Metal Carbonyls" Coordination Chemistry Reviews 1990, Band 105, S. 195-219. doi : 10.1016/0010-8545(90)80023-M
- ^ Barrie, PJ; Clark, RJH; Selen-Festkörper-NMR-Spektroskopie und Strukturen von Tetramethylammoniumpentaselenid- und Hexaselenid-Komplexen. Inorg. Chem, 1995, 34, 4299–4304 DOI: 10.1021/ic00121a006
- ^ Kanatzidis, Mercouri G. (1990). „Lösliche Polychalkogenide der späten Übergangs- und Hauptgruppenelemente“. Kommentare zu Anorganische Chemie . 10 (4–5): 161–195. doi : 10.1080/02603599008048650 .