Tryptamin - Tryptamine

|
|
|
|
| Namen | |
|---|---|
|
Bevorzugter IUPAC-Name
2- (1 H -indol-3-yl) ethan-1-amin |
|
| Bezeichner | |
|
3D-Modell ( JSmol )
|
|
| ChEMBL | |
| ChemSpider | |
| ECHA-InfoCard |
100.000.464 |
|
PubChem- CID
|
|
| UNII | |
|
CompTox-Dashboard ( EPA )
|
|
|
|
|
|
| Eigenschaften | |
| C 10 H 12 N 2 | |
| Molmasse | 160,220 g·mol -1 |
| Aussehen | weißes bis orangefarbenes kristallines Pulver |
| Schmelzpunkt | 113-116˚C |
| Siedepunkt | 137 °C (279 °F; 410 K) (0,15 mmHg) |
| vernachlässigbare Löslichkeit in Wasser | |
| Gefahren | |
| Flammpunkt | 185˚C |
|
Sofern nicht anders angegeben, beziehen sich die Daten auf Materialien im Standardzustand (bei 25 °C [77 °F], 100 kPa). |
|
|
|
|
| Infobox-Referenzen | |
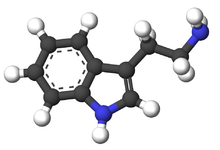
Tryptamin ist ein Indolamin- Metabolit der essentiellen Aminosäure Tryptophan . Die chemische Struktur wird durch ein Indol ─ einen kondensierten Benzol- und Pyrrolring und eine 2-Aminoethylgruppe am dritten Kohlenstoffatom definiert. Die Struktur von Tryptamin ist ein gemeinsames Merkmal bestimmter aminerger Neuromodulatoren, darunter Melatonin , Serotonin , Bufotenin und psychedelische Derivate wie Dimethyltryptamin (DMT), Psilocybin , Psilocin und andere . Tryptamin aktiviert nachweislich Spuren von Amin-assoziierten Rezeptoren, die im Gehirn von Säugetieren exprimiert werden, und reguliert die Aktivität von dopaminergen , serotonergen und glutamatergen Systemen. Im menschlichen Darm wandeln symbiotische Bakterien Nahrungstryptophan in Tryptamin um, das 5-HT 4 -Rezeptoren aktiviert und die Magen-Darm-Motilität reguliert. Mehrere Tryptamin-abgeleitete Medikamente wurden zur Behandlung von Migräne entwickelt , während Spurenamin-assoziierte Rezeptoren als potenzielles Behandlungsziel für neuropsychiatrische Erkrankungen untersucht werden.
Eine Liste der Tryptamin-Derivate finden Sie unter: Liste der substituierten Tryptamine .
Naturereignisse
Eine Liste von Pflanzen, Pilzen und Tieren, die Tryptamine enthalten, finden Sie unter Liste psychoaktiver Pflanzen und Liste natürlich vorkommender Tryptamine .
Säugetiergehirn
Der endogene Tryptaminspiegel im Gehirn von Säugetieren beträgt weniger als 100 ng pro Gramm Gewebe. Bei Patienten mit bestimmten neuropsychiatrischen Störungen wie bipolarer Depression und Schizophrenie wurden jedoch erhöhte Konzentrationen von Spurenaminen beobachtet .
Darmmikrobiom von Säugetieren
Tryptamin ist im Darm und im Kot von Menschen und Nagetieren relativ reichlich vorhanden . Kommensale Bakterien, einschließlich Ruminococcus gnavus und Clostridium sporogenes im Magen-Darm-Trakt , besitzen das Enzym Tryptophan- Decarboxylase , das bei der Umwandlung von Nahrungstryptophan in Tryptamin hilft. Tryptamin ist ein Ligand für Serotonin Typ 4 (5-HT 4 )-Rezeptoren des Darmepithels und reguliert den gastrointestinalen Elektrolythaushalt durch Kolonsekrete.
Stoffwechsel
Biosynthese
Um Tryptamin in vivo zu ergeben , entfernt Tryptophandecarboxylase die Carbonsäuregruppe am α-Kohlenstoff von Tryptophan . Synthetische Modifikationen von Tryptamin können Serotonin und Melatonin produzieren ; diese Wege treten jedoch nicht als Hauptweg für die endogene Neurotransmitter-Synthese natürlich auf.
Katabolismus
Monoaminoxidasen A und B sind die primären Enzyme, die am Tryptaminstoffwechsel zur Produktion von Indol-3-acetaldehyd beteiligt sind , jedoch ist unklar, welche Isoform für den Tryptaminabbau spezifisch ist.
Wirkmechanismen und biologische Effekte
Neuromodulation
Tryptamin kann den Spurenamin-assoziierten Rezeptor TAAR1 (hTAAR1 beim Menschen) schwach aktivieren . In begrenzten Studien wurde Tryptamin als Spuren-Neuromodulator angesehen, der in der Lage ist, die Aktivität neuronaler Zellantworten zu regulieren, ohne an die assoziierten postsynaptischen Rezeptoren zu binden.
hTAAR1
hTAAR1 ist ein stimulatorischer G-Protein-gekoppelter Rezeptor (GPCR), der im intrazellulären Kompartiment sowohl von prä- als auch von postsynaptischen Neuronen schwach exprimiert wird. Tryptamin und andere hTAAR1-Agonisten können das neuronale Feuern erhöhen, indem sie das Neurotransmitter-Recycling durch cAMP- abhängige Phosphorylierung des Monoamin-Wiederaufnahmetransporters hemmen . Dieser Mechanismus erhöht die Menge an Neurotransmitter im synaptischen Spalt, wodurch die postsynaptische Rezeptorbindung und die neuronale Aktivierung erhöht werden. Umgekehrt, wenn hTAAR1 mit G-Protein-gekoppelten nach innen rektifizierenden Kaliumkanälen (GIRKs) kolokalisiert werden, reduziert die Rezeptoraktivierung das neuronale Feuern, indem sie die Membranhyperpolarisation durch den Efflux von Kaliumionen erleichtert . Das Gleichgewicht zwischen der hemmenden und erregenden Aktivität der hTAAR1-Aktivierung unterstreicht die Rolle von Tryptamin bei der Regulierung der neuralen Aktivität.
Die Aktivierung von hTAAR1 wird als neuartige Behandlung von Depression, Sucht und Schizophrenie untersucht. hTAAR1 wird hauptsächlich in Gehirnstrukturen exprimiert, die mit Dopaminsystemen assoziiert sind, wie dem ventralen Tegmentalbereich (VTA) und Serotoninsystemen in den dorsalen Raphekernen (DRN). Zusätzlich wird das hTAAR1 Gen an 6q23.2 auf dem menschlichen Chromosom lokalisiert, die eine Suszeptibilität Locus für affektive Störungen und Schizophrenie. Die Aktivierung von TAAR1 legt eine potenzielle neue Behandlung für neuropsychiatrische Störungen nahe, da TAAR1-Agonisten eine antidepressive Aktivität, eine gesteigerte Kognition , weniger Stress und Anti-Sucht-Wirkungen bewirken.
Magen-Darm-Motilität
Tryptamin, das von mutualistischen Bakterien im menschlichen Darm produziert wird, aktiviert Serotonin-GPCRs, die ubiquitär entlang des Dickdarmepithels exprimiert werden. Bei der Tryptaminbindung durchläuft der aktivierte 5-HT 4 -Rezeptor eine Konformationsänderung, die es seiner G s alpha-Untereinheit ermöglicht, GDP gegen GTP auszutauschen , und seine Freisetzung vom 5-HT 4 -Rezeptor und der βγ-Untereinheit. GTP-gebundenes G s aktiviert die Adenylylcyclase , die die Umwandlung von ATP in zyklisches Adenosinmonophosphat (cAMP) katalysiert . cAMP öffnet Chlorid- und Kaliumionenkanäle, um die Elektrolytsekretion im Dickdarm zu fördern und die Darmmotilität zu fördern.
Pharmakodynamik
| Tryptamin | Mensch TAAR1 | Maus TAAR1 | Ratte TAAR | |||
|---|---|---|---|---|---|---|
| EG 50 | K i | EG 50 | K i | EG 50 | K i | |
| Tryptamin | 21 | N / A | 2.7 | 1,4 | 0,41 | 0,13 |
| Serotonin | >50 | N / A | >50 | N / A | 5.2 | N / A |
| Psilocin | >30 | N / A | 2.7 | 17 | 0,92 | 1,4 |
| DMT | >10 | N / A | 1,2 | 3.3 | 1,5 | 22 |
|
EC 50 und K i -Werte sind in mikromolar (μM) angegeben. EC 50 spiegelt den Betrag wieder
Tryptamin, das erforderlich ist, um 50 % der maximalen TAAR1-Antwort hervorzurufen. Je kleiner der K i -Wert ist, desto stärker bindet das Tryptamin an den Rezeptor. |
||||||
Tryptamin-basierte Therapeutika
| Arzneimittel | Mechanismus | Behandlung | Wirkung | Struktur |
|---|---|---|---|---|
| Sumatriptan | 5-HT 1B und 5-HT 1D Agonist | Migräne Kopfschmerzen | Vasokonstriktion der Blutgefäße im Gehirn | |
| Rizatriptan | 5-HT 1B und 5-HT 1D Agonist | Migräne Kopfschmerzen | Vasokonstriktion der Blutgefäße im Gehirn | |
| Zolmitriptan | 5-HT 1B und 5-HT 1D Agonist | Migräne Kopfschmerzen | Vasokonstriktion der Blutgefäße im Gehirn | |
| Almotriptan | 5-HT 1B und 5-HT 1D Agonist | Migräne Kopfschmerzen | Vasokonstriktion der Blutgefäße im Gehirn | |
| Eletriptan | 5-HT 1B und 5-HT 1D Agonist | Migräne Kopfschmerzen | Vasokonstriktion der Blutgefäße im Gehirn | |
| Frovatriptan | 5-HT 1B und 5-HT 1D Agonist | Migräne Kopfschmerzen | Vasokonstriktion der Blutgefäße im Gehirn | |
| Naratriptan | 5-HT 1B und 5-HT 1D Agonist | Migräne Kopfschmerzen | Vasokonstriktion der Blutgefäße im Gehirn |
Siehe auch
- Tryptophan
- Substituierte Tryptamine
- Spurenamine
- Serotonin-Rezeptor-Agonist
- Humaner Spurenamin-assoziierter Rezeptor 1
- Neuromodulation
Verweise
Externe Links
- Häufig gestellte Fragen zu Tryptamin
- Tryptamin Halluzinogene und Bewusstsein
- Tryptamind Psychoactives , Referenzseite zu Tryptamin und anderen Psychopharmaka .
- Tryptamin (T) Eintrag in TiHKAL • info










