Ammoniumeisen(II)sulfat - Ammonium iron(II) sulfate
|
|

|
|
| Namen | |
|---|---|
|
IUPAC-Name
Ammoniumeisen(II)sulfat
|
|
| Andere Namen
Eisen( II) -ammoniumsulfat Ammoniumeisensulfat Mohrsches Salz |
|
| Bezeichner | |
|
3D-Modell ( JSmol )
|
|
| ChEBI | |
| ChemSpider | |
| ECHA-InfoCard |
100.030.125 |
| EG-Nummer | |
|
PubChem- CID
|
|
| UNII | |
|
CompTox-Dashboard ( EPA )
|
|
|
|
|
|
| Eigenschaften | |
| Fe(SO 4 )(NH 4 ) 2 (SO 4 ) (wasserfrei) Fe(SO 4 )(NH 4 ) 2 (SO 4 )·6H 2 O (Hexahydrat) |
|
| Molmasse | 284,05 g mol −1 (wasserfrei) 392,14 g mol −1 (Hexahydrat) |
| Aussehen | Blaugrüner Feststoff |
| Dichte | 1,86 g / cm 3 |
| Schmelzpunkt | 100 bis 110 °C (212 bis 230 °F; 373 bis 383 K) |
| Siedepunkt | Unzutreffend |
| 269 g/L (Hexahydrat) | |
| Gefahren | |
| Sicherheitsdatenblatt | Fisher SDB |
| GHS-Piktogramme |

|
| GHS-Signalwort | Warnung |
| H315 , H319 , H335 | |
| P261 , P264 , P271 , P280 , P302+352 , P304+340 , P305+351+338 , P312 , P321 , P332+313 , P337+313 , P362 , P403+233 , P405 , P501 | |
| NFPA 704 (Feuerdiamant) | |
| Verwandte Verbindungen | |
|
Verwandte Verbindungen
|
Ammoniumeisen(III)sulfat |
|
Sofern nicht anders angegeben, beziehen sich die Daten auf Materialien im Standardzustand (bei 25 °C [77 °F], 100 kPa). |
|
|
|
|
| Infobox-Referenzen | |
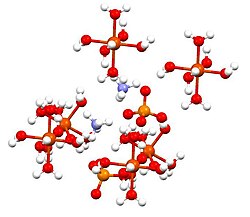
Ammoniumeisen(II)sulfat oder Mohrs Salz ist die anorganische Verbindung mit der Formel (NH 4 ) 2 Fe(SO 4 ) 2 (H 2 O) 6 . Es enthält zwei verschiedene Kationen , Fe 2+ und NH 4 + und wird als Doppelsalz von Eisensulfat und Ammoniumsulfat klassifiziert . Es ist ein übliches Laborreagenz, da es leicht kristallisiert und Kristalle der Oxidation durch Luft widerstehen. Wie die anderen Eisen(II)-Sulfatsalze löst sich Eisen(II)-Ammoniumsulfat in Wasser unter Bildung des Aquo-Komplexes [Fe(H 2 O) 6 ] 2+ , der eine oktaedrische Molekülgeometrie aufweist . Seine mineralische Form ist Mohrit .
Struktur
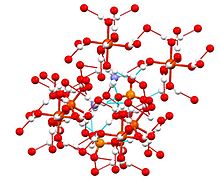
Diese Verbindung gehört zu einer Gruppe von Doppelsulfaten, die Schönite oder Tutton-Salze genannt werden . Tuttons Salze bilden monokline Kristalle und haben die Formel M 2 N(SO 4 ) 2 . 6H 2 O (M = verschiedene Monokationen). Hinsichtlich der Bindung bestehen Kristalle aus Oktaedern [Fe(H 2 O) 6 ] 2+ -Zentren, die über Wasserstoffbrücken an Sulfat und Ammonium gebunden sind.
Das Mohrsche Salz ist nach dem deutschen Chemiker Karl Friedrich Mohr benannt , der im 19. Jahrhundert viele wichtige Fortschritte in der Methodik der Titration machte.
Anwendungen
In der analytischen Chemie ist dieses Salz die bevorzugte Quelle für Eisen(II)-Ionen, da der Feststoff eine lange Haltbarkeit hat und gegen Oxidation beständig ist. Diese Stabilität erstreckt sich etwas auf Lösungen, die die Wirkung des pH-Werts auf das Eisen(III)-Redoxpaar widerspiegeln. Diese Oxidation tritt bei hohem pH leichter auf. Die Ammoniumionen machen Lösungen des Mohrschen Salzes leicht sauer, was diesen Oxidationsprozess verlangsamt. Schwefelsäure wird üblicherweise Lösungen zugesetzt, um die Oxidation zu Eisen(III) zu reduzieren.
Es wird im Dosimeter von Fricke verwendet , um hohe Dosen von Gammastrahlen zu messen.
Vorbereitung
Mohrs Salz wird hergestellt, indem man eine äquimolare Mischung von hydratisiertem Eisen(II)-sulfat und Ammoniumsulfat in Wasser, das etwas Schwefelsäure enthält , auflöst und die resultierende Lösung dann einer Kristallisation unterwirft . Eisen(II)-ammoniumsulfat bildet hellgrüne Kristalle. Dieses Salz ionisiert beim Erhitzen, um alle darin enthaltenen Kationen und Anionen zu ergeben.
Schadstoffe
Häufige Verunreinigungen sind Magnesium , Nickel , Mangan , Blei und Zink , von denen viele isomorphe Salze bilden .

