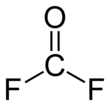
Carbonylfluorid - Carbonyl fluoride
|
|
|||
| Namen | |||
|---|---|---|---|
|
Bevorzugter IUPAC-Name
Carbonyldifluorid |
|||
| Andere Namen
Fluorphosgen; Difluoridkohlenoxid; Fluormethanoylfluorid
|
|||
| Kennungen | |||
|
3D-Modell ( JSmol )
|
|||
| ChemSpider | |||
| ECHA InfoCard |
100.005.941 |
||
| EG-Nummer | |||
|
PubChem CID
|
|||
| RTECS-Nummer | |||
| UNII | |||
| UN-Nummer | 2417 | ||
|
CompTox-Dashboard ( EPA )
|
|||
|
|||
|
|||
| Eigenschaften | |||
| COF 2 | |||
| Molmasse | 66,01 gmol -1 | ||
| Aussehen | Farbloses Gas | ||
| Dichte | 2,698 g / l (Gas), 1,139 g / cm 3 (Flüssigkeit am Schmelzpunkt) | ||
| Schmelzpunkt | –111,26 ° C (–168,27 ° F; 161,89 K) | ||
| Siedepunkt | –84,57 ° C (–120,23 ° F; 188,58 K) | ||
| reagiert heftig mit Wasser | |||
| Dampfdruck | 55,4 atm (20 ° C) | ||
| Struktur | |||
| C 2v | |||
| 0,95 D. | |||
| Gefahren | |||
| Hauptgefahren | Tödlich bei Einatmen, reagiert mit Wasser | ||
| GHS-Piktogramme |
   
|
||
| GHS Signalwort | Achtung | ||
| H280 , H290 , H314 , H330 , H331 , H370 | |||
| P234 , P260 , P261 , P264 , P270 , P271 , P280 , P284 , P301 + 330 + 331 , P303 + 361 + 353 , P304 + 340 , P305 + 351 + 338 , P307 + 311 , P310 , P311 , P320 , P321 , P363 , P390 , P403 + 233 , P404 , P405 , P410 + 403 , P501 | |||
| NFPA 704 (Feuerdiamant) | |||
| Flammpunkt | Nicht brennbar | ||
| NIOSH (US-Grenzwerte für die Gesundheitsbelastung): | |||
|
PEL (zulässig)
|
keiner | ||
|
REL (empfohlen)
|
TWA 2 ppm (5 mg / m 3 ) ST 5 ppm (15 mg / m 3 ) | ||
|
IDLH (unmittelbare Gefahr)
|
ND | ||
| Verwandte Verbindungen | |||
|
Verwandte Verbindungen
|
Phosgen Carbonylbromid Formylfluorid Thiocarbonylchlorid Aceton Harnstoff Kohlensäure |
||
|
Sofern nicht anders angegeben, werden Daten für Materialien in ihrem Standardzustand (bei 25 ° C, 100 kPa) angegeben. |
|||
|
|
|||
| Infobox-Referenzen | |||
Carbonylfluorid ist eine chemische Verbindung mit der Formel COF 2 . Dieses Gas ist wie sein analoges Phosgen farblos und hochgiftig. Das Molekül ist planar mit C 2v -Symmetrie .
Zubereitung und Eigenschaften
Carbonylfluorid wird üblicherweise als Zersetzungsprodukt von fluorierten Kohlenwasserstoffen bei deren thermischer Zersetzung hergestellt, beispielsweise aus Trifluormethanol oder Tetrafluormethan in Gegenwart von Wasser:
-
CF.
4+ H.
2O → COF
2+ 2 HF
Carbonylfluorid kann auch durch Reaktion von Phosgen mit Fluorwasserstoff und Oxidation von Kohlenmonoxid hergestellt werden , obwohl letzteres dazu neigt, zu einer Überoxidation zu Tetrafluoridkohlenstoff zu führen . Die Oxidation von Kohlenmonoxid mit Silberdifluorid ist zweckmäßig:
-
CO + 2 AgF
2→ COF
2+ 2 AgF
Carbonylfluorid ist in Gegenwart von Wasser instabil und hydrolysiert zu Kohlendioxid und Fluorwasserstoff :
-
COF
2+ H.
2O → CO
2+ 2 HF
Sicherheit
Carbonylfluorid ist toxisch mit einer empfohlenen Expositionsgrenze von 2 ppm als 8-Stunden-Zeitgewicht und 5 ppm als Kurzzeitexposition (15-Minuten-Durchschnitt).
Verweise
- ^ A b c d e NIOSH Pocket Guide zu chemischen Gefahren. "#0108" . Nationales Institut für Arbeitssicherheit und Gesundheitsschutz (NIOSH).
- ^ MW Farlow; EH Mann; CW Tullock (1960). "Carbonylfluorid". Anorganische Synthesen . Anorganische Synthesen. 6 . S. 155–158. doi : 10.1002/9780470132371.ch48 . ISBN 9780470132371.
- ^ "Carbonylfluorid" . NIOSH-Taschenleitfaden zu chemischen Gefahren . CDC-Zentren für die Kontrolle und Prävention von Krankheiten . Abgerufen am 10.09.2013 .