Exosomenkomplex - Exosome complex
Der Exosom-Komplex (oder PM/Scl-Komplex , oft nur Exosom genannt ) ist ein intrazellulärer Multi- Protein- Komplex , der verschiedene Arten von RNA -Molekülen (Ribonukleinsäure) abbauen kann. Exosomenkomplexe kommen sowohl in eukaryontischen Zellen als auch in Archaeen vor , während in Bakterien ein einfacherer Komplex, das Degradosom , ähnliche Funktionen ausübt .
Der Kern des Exosoms enthält eine sechsgliedrige Ringstruktur, an die andere Proteine gebunden sind. In eukaryotischen Zellen ist der Exosomenkomplex im Zytoplasma , im Nukleus und insbesondere im Nukleolus vorhanden , obwohl verschiedene Proteine mit dem Exosomenkomplex in diesen Kompartimenten interagieren und die RNA-Abbauaktivität des Komplexes zu für diese Zellkompartimente spezifischen Substraten regulieren . Substrate des Exosoms umfassen Boten-RNA , ribosomale RNA und viele Arten kleiner RNAs . Das Exosom hat eine exoribonukleolytische Funktion, d. h. es baut RNA ab einem Ende ( in diesem Fall das 3'-Ende ) ab und bei Eukaryoten auch eine endoribonukleolytische Funktion, d. h. es spaltet RNA an Stellen innerhalb des Moleküls.
Mehrere Proteine in der Exosom sind das Ziel von Autoantikörpern bei Patienten mit bestimmten Autoimmunerkrankungen (insbesondere die PM / Scl Overlap - Syndrom ) und einigen antimetabolischer Chemotherapien zur Krebsfunktion durch die Aktivität des exosome blockieren. Darüber hinaus verursachen Mutationen in der Exosomkomponente 3 eine pontozerebelläre Hypoplasie und eine spinale Motoneuronerkrankung .
Entdeckung
Das Exosom wurde erstmals 1997 als RNase in der Keimhefe Saccharomyces cerevisiae , einem häufig verwendeten Modellorganismus, entdeckt . Nicht lange danach, im Jahr 1999, wurde erkannt, dass das Exosom tatsächlich das Hefe-Äquivalent eines bereits beschriebenen Komplexes in menschlichen Zellen war, der als PM/Scl-Komplex bezeichnet wird und der bei Patienten mit bestimmten Autoimmunerkrankungen Jahre zuvor als Autoantigen identifiziert worden war ( siehe unten ). Die Reinigung dieses "PM/Scl-Komplexes" ermöglichte die Identifizierung weiterer menschlicher Exosomenproteine und schließlich die Charakterisierung aller Komponenten im Komplex. Die zunehmende Menge von 2001 Genomdaten , die die Vorhersage von Exosomen Proteinen in Archaea erlaubt verfügbar worden waren, obwohl es noch 2 Jahre vor dem ersten Exosom von einem Archaea Organismus gereinigt nehmen würde.
Struktur
Kernproteine

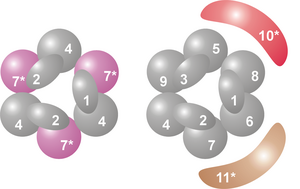
Der Kern des Komplexes hat eine Ringstruktur bestehend aus sechs Proteinen, die alle zur gleichen Klasse von RNasen gehören, den RNase PH- like Proteins. In Archaeen gibt es zwei verschiedene PH-ähnliche Proteine (genannt Rrp41 und Rrp42), die jeweils dreimal in alternierender Reihenfolge vorhanden sind. Eukaryotische Exosomenkomplexe haben sechs verschiedene Proteine, die die Ringstruktur bilden. Von diesen sechs eukaryontischen Proteinen ähneln drei dem archaealen Rrp41-Protein und die anderen drei Proteine ähneln eher dem archaealen Rrp42-Protein.

Oben auf diesem Ring befinden sich drei Proteine, die eine S1- RNA-Bindungsdomäne (RBD) besitzen. Zwei Proteine haben zusätzlich eine K-Homologie-(KH)-Domäne . Bei Eukaryoten sind drei verschiedene "S1"-Proteine an den Ring gebunden, während bei Archaeen entweder ein oder zwei verschiedene "S1"-Proteine Teil des Exosoms sein können (allerdings sind immer drei S1-Untereinheiten an den Komplex gebunden).
Diese Ringstruktur ist der der Proteine RNase PH und PNPase sehr ähnlich . In Bakterien bildet das an der tRNA- Prozessierung beteiligte Protein RNase PH einen hexameren Ring, der aus sechs identischen RNase PH-Proteinen besteht. Im Fall der PNPase, einem phosphorolytischen RNA-abbauenden Protein, das in Bakterien und den Chloroplasten und Mitochondrien einiger eukaryotischer Organismen vorkommt, sind zwei RNase-PH-Domänen und sowohl eine S1- als auch eine KH-RNA-Bindungsdomäne Teil eines einzigen Proteins, das ein trimerer Komplex, der eine Struktur annimmt, die mit der des Exosoms fast identisch ist. Aufgrund dieser hohen Ähnlichkeit sowohl in den Proteindomänen als auch in der Struktur wird angenommen, dass diese Komplexe evolutionär verwandt sind und einen gemeinsamen Vorfahren haben . Die RNase PH-ähnlichen Exosomproteine, PNPase und RNase PH gehören alle zur RNase PH-Familie von RNasen und sind phosphorolytische Exoribonukleasen , was bedeutet, dass sie anorganisches Phosphat verwenden , um Nukleotide vom 3'-Ende von RNA- Molekülen zu entfernen .
Assoziierte Proteine
Neben diesen neun Kernproteinen des Exosoms assoziieren in eukaryontischen Organismen häufig zwei weitere Proteine mit dem Komplex. Eine davon ist Rrp44, eine hydrolytische RNase, die zur RNase R- Familie hydrolytischer Exoribonukleasen (Nukleasen, die Wasser verwenden, um die Nukleotidbindungen zu spalten) gehört. Rrp44 ist nicht nur ein exoribonukleolytisches Enzym, sondern besitzt auch eine endoribonukleolytische Aktivität, die sich in einer separaten Domäne des Proteins befindet. In Hefe ist Rrp44 mit allen Exosomenkomplexen assoziiert und spielt eine entscheidende Rolle bei der Aktivität des Hefeexosomkomplexes. Während ein menschliches Homolog des Proteins existiert, wurde lange Zeit kein Beweis dafür gefunden, dass sein menschliches Homolog mit dem menschlichen Exosomenkomplex assoziiert war. Im Jahr 2010 wurde jedoch entdeckt, dass der Mensch drei Rrp44-Homologe besitzt und zwei davon mit dem Exosomenkomplex in Verbindung gebracht werden können. Diese beiden Proteine bauen höchstwahrscheinlich unterschiedliche RNA-Substrate aufgrund ihrer unterschiedlichen zellulären Lokalisation ab, wobei eines im Zytoplasma (Dis3L1) und das andere im Zellkern (Dis3) lokalisiert ist.

Das zweite häufige assoziierte Protein wird Rrp6 (bei Hefe) oder PM/Scl-100 (bei Mensch) genannt. Dieses Protein ist wie Rrp44 eine hydrolytische Exoribonuklease, aber in diesem Fall der RNase-D- Proteinfamilie. Das Protein PM/Scl-100 ist am häufigsten Teil von Exosomenkomplexen im Zellkern, kann aber auch Teil des zytoplasmatischen Exosomenkomplexes sein.
Regulatorische Proteine
Abgesehen von diesen beiden fest verbundenen Proteinuntereinheiten interagieren viele Proteine mit dem Exosomenkomplex sowohl im Zytoplasma als auch im Zellkern. Diese lose assoziierten Proteine können die Aktivität und Spezifität des Exosomenkomplexes regulieren. Im Zytoplasma interagiert das Exosom mit AU-reichen-Element (ARE)-Bindungsproteinen (zB KRSP und TTP), die den Abbau von mRNAs fördern oder verhindern können. Das nukleäre Exosom assoziiert mit RNA-bindenden Proteinen (zB MPP6/Mpp6 und C1D/Rrp47 beim Menschen/Hefe), die für die Verarbeitung bestimmter Substrate benötigt werden.
Neben einzelnen Proteinen interagieren auch andere Proteinkomplexe mit dem Exosom. Einer davon ist der zytoplasmatische Ski-Komplex , der eine RNA- Helikase (Ski2) enthält und am mRNA-Abbau beteiligt ist. Im Zellkern wird die Verarbeitung von rRNA und snoRNA durch das Exosom durch den TRAMP-Komplex vermittelt , der sowohl RNA-Helikase- (Mtr4) als auch Polyadenylierungs- (Trf4)-Aktivität enthält.
Funktion
Enzymatische Funktion
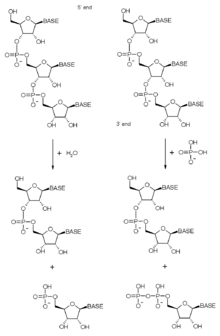
Wie oben erwähnt, enthält der Exosomenkomplex viele Proteine mit Ribonuklease-Domänen. Die genaue Natur dieser Ribonuklease-Domänen hat sich im Laufe der Evolution von bakteriellen über archaeale bis hin zu eukaryotischen Komplexen geändert, da verschiedene Aktivitäten gewonnen und verloren wurden. Das Exosom ist in erster Linie eine 3'-5'- Exoribonuklease , was bedeutet, dass es RNA-Moleküle von ihrem 3'-Ende abbaut . In Exosomenkomplexen enthaltene Exoribonukleasen sind entweder phosphorolytisch (die RNase PH-ähnlichen Proteine) oder in Eukaryoten hydrolytisch (die RNase R- und RNase D-Domänenproteine). Die phosphorolytischen Enzyme verwenden anorganisches Phosphat, um die Phosphodiesterbindungen zu spalten – wodurch Nukleotiddiphosphate freigesetzt werden . Die hydrolytischen Enzyme verwenden Wasser, um diese Bindungen zu hydrolysieren und setzen Nukleotidmonophosphate frei .
In Archaeen ist die Rrp41-Untereinheit des Komplexes eine phosphorolytische Exoribonuklease. Drei Kopien dieses Proteins liegen im Ring vor und sind für die Aktivität des Komplexes verantwortlich. In Eukaryoten hat keine der RNase-PH-Untereinheiten diese katalytische Aktivität beibehalten, was bedeutet, dass die Kernringstruktur des menschlichen Exosoms kein enzymatisch aktives Protein aufweist. Trotz dieses Verlusts an katalytischer Aktivität ist die Struktur des Kernexosoms von Archaeen bis zum Menschen hoch konserviert, was darauf hindeutet, dass der Komplex eine lebenswichtige zelluläre Funktion ausübt. Bei Eukaryoten wird das Fehlen der phosphorolytischen Aktivität durch die Anwesenheit der hydrolytischen Enzyme ausgeglichen, die in solchen Organismen für die Ribonuklease-Aktivität des Exosoms verantwortlich sind.
Wie oben erwähnt, sind die hydrolytischen Proteine Rrp6 und Rrp44 mit dem Exosom in Hefe und in Menschen assoziiert, neben Rrp6 können zwei verschiedene Proteine, Dis3 und Dis3L1, an der Position des Hefe-Rrp44-Proteins assoziiert sein. Obwohl ursprünglich angenommen wurde, dass die S1-Domänenproteine auch eine 3'-5'-hydrolytische Exoribonukleaseaktivität aufweisen, wurde die Existenz dieser Aktivität kürzlich in Frage gestellt und diese Proteine könnten nur eine Rolle bei der Bindung von Substraten vor ihrem Abbau durch den Komplex spielen.
Substrate
Das Exosom ist am Abbau und der Verarbeitung einer Vielzahl von RNA-Spezies beteiligt. Im Zytoplasma von Zellen ist es am Umsatz von Boten-RNA (mRNA)-Molekülen beteiligt. Der Komplex kann mRNA-Moleküle abbauen, die für den Abbau markiert wurden, weil sie Fehler enthalten, durch Wechselwirkungen mit Proteinen aus den Nonsense-vermittelten Zerfalls- oder Nonstop-Zerfallswegen . Alternativ werden mRNAs als Teil ihres normalen Umsatzes abgebaut . Mehrere Proteine, die mRNA-Moleküle durch Bindung an AU-reiche Elemente in der 3'-untranslatierten Region von mRNAs stabilisieren oder destabilisieren, interagieren mit dem Exosomenkomplex. Im Zellkern wird das Exosom für die korrekte Verarbeitung mehrerer kleiner nuklearer RNA-Moleküle benötigt. Schließlich ist der Nukleolus das Kompartiment, in dem sich die meisten Exosomenkomplexe befinden. Dort spielt es eine Rolle bei der Verarbeitung der 5.8S- ribosomalen RNA (der ersten identifizierten Funktion des Exosoms) und mehrerer kleiner nukleolärer RNAs .
Obwohl die meisten Zellen andere Enzyme haben, die RNA abbauen können, entweder vom 3'- oder vom 5'-Ende der RNA, ist der Exosomenkomplex für das Überleben der Zellen essentiell. Wenn die Expression von Exosomenproteinen künstlich reduziert oder gestoppt wird, zum Beispiel durch RNA-Interferenz , stoppt das Wachstum und die Zellen sterben schließlich. Sowohl die Kernproteine des Exosomenkomplexes als auch die beiden wichtigsten assoziierten Proteine sind essentielle Proteine. Bakterien haben keinen Exosomenkomplex; ähnliche Funktionen werden jedoch von einem einfacheren Komplex ausgeführt, der das Protein PNPase enthält , das als Degradosom bezeichnet wird .
Das Exosom ist ein Schlüsselkomplex in der zellulären RNA-Qualitätskontrolle. Im Gegensatz zu Prokaryoten besitzen Eukaryoten hochaktive RNA-Überwachungssysteme, die unverarbeitete und fehlprozessierte RNA-Protein-Komplexe (wie Ribosomen ) vor ihrem Austritt aus dem Zellkern erkennen. Es wird vermutet , dass dieses System verhindert , dass abweichende Komplexe wichtige zelluläre Prozesse wie die Proteinsynthese stören .
Neben der RNA-Prozessierung, dem Umsatz und den Überwachungsaktivitäten ist das Exosom für den Abbau sogenannter kryptischer instabiler Transkripte (CUTs) wichtig, die von Tausenden von Loci innerhalb des Hefegenoms produziert werden. Die Bedeutung dieser instabilen RNAs und ihr Abbau sind noch unklar, aber ähnliche RNA-Spezies wurden auch in menschlichen Zellen nachgewiesen.
Erkrankung
Autoimmunität
Der Exosom-Komplex ist das Ziel von Autoantikörpern bei Patienten, die an verschiedenen Autoimmunerkrankungen leiden . Diese Autoantikörper werden hauptsächlich bei Menschen gefunden, die am PM/Scl-Überlappungssyndrom leiden , einer Autoimmunerkrankung, bei der Patienten Symptome sowohl von Sklerodermie als auch entweder Polymyositis oder Dermatomyositis haben . Autoantikörper können im Serum von Patienten durch eine Vielzahl von Assays nachgewiesen werden. In der Vergangenheit waren die am häufigsten verwendeten Methoden Doppelimmun mit Kalb Thymus - Extrakten, Immunofluoreszenz auf HEp-2 - Zellen oder Immunpräzipitation aus menschlichen Zellextrakten. In Immunpräzipitationsassays mit Seren von Anti-Exosom-positiven Seren wird ein charakteristischer Satz von Proteinen präzipitiert. Bereits Jahre bevor der Exosomenkomplex identifiziert wurde, wurde dieses Muster als PM/Scl-Komplex bezeichnet . Immunofluoreszenz von diesen Patienten in der Regel unter Verwendung von Seren zeigt eine typische Färbung der Nukleolus von Zellen, die die Anregung ausgelöst , daß die durch Autoantikörper erkannte Antigen könnte in Ribosomen wichtig sein Synthese . In jüngerer Zeit sind rekombinante Exosomenproteine verfügbar geworden und diese wurden verwendet, um Linienimmunoassays (LIAs) und Enzyme-Linked-Immunosorbent-Assays (ELISAs) zum Nachweis dieser Antikörper zu entwickeln.
Bei diesen Krankheiten richten sich Antikörper hauptsächlich gegen zwei der Proteine des Komplexes, genannt PM/Scl-100 (das RNase D-ähnliche Protein) und PM/Scl-75 (eines der RNase PH-ähnlichen Proteine aus dem Ring) und Antikörper Die Erkennung dieser Proteine findet sich bei etwa 30% der Patienten mit dem PM/Scl-Überlappungssyndrom. Obwohl diese beiden Proteine das Hauptziel der Autoantikörper sind, können bei diesen Patienten auch andere Exosom-Untereinheiten und assoziierte Proteine (wie C1D) angegriffen werden. Gegenwärtig ist der empfindlichste Weg, diese Antikörper nachzuweisen, die Verwendung eines Peptids , das vom PM/Scl-100-Protein abgeleitet ist, als Antigen in einem ELISA anstelle von vollständigen Proteinen. Autoantikörper werden mit dieser Methode bei bis zu 55 % der Patienten mit PM/Scl-Überlappungssyndrom gefunden, können aber auch bei Patienten mit Sklerodermie, Polymyositis oder Dermatomyositis allein nachgewiesen werden.
Da die Autokörper hauptsächlich bei Patienten gefunden werden, die Merkmale mehrerer verschiedener Autoimmunerkrankungen aufweisen, können die klinischen Symptome dieser Patienten stark variieren. Die am häufigsten beobachteten Symptome sind die typischen Symptome der einzelnen Autoimmunerkrankungen und umfassen das Raynaud-Phänomen , Arthritis , Myositis und Sklerodermie . Die Behandlung dieser Patienten ist symptomatisch und ähnelt der Behandlung der einzelnen Autoimmunerkrankung, wobei häufig entweder immunsuppressive oder immunmodulierende Medikamente eingesetzt werden.
Krebsbehandlung
Es wurde gezeigt, dass das Exosom durch den Antimetaboliten Fluorouracil , ein Medikament, das in der Chemotherapie von Krebs verwendet wird , gehemmt wird . Es ist eines der erfolgreichsten Medikamente zur Behandlung von soliden Tumoren . In mit Fluorouracil behandelten Hefezellen wurden Defekte bei der Verarbeitung von ribosomaler RNA gefunden, die mit denen identisch waren, die beobachtet wurden, wenn die Aktivität des Exosoms durch molekularbiologische Strategien blockiert wurde . Das Fehlen einer korrekten ribosomalen RNA-Verarbeitung ist für Zellen tödlich, was die antimetabolische Wirkung des Arzneimittels erklärt.
Neurologische Störungen
Mutationen in Exosom-Komponente 3 verursachen infantile spinale Motoneuronerkrankung , Kleinhirnatrophie, progressive Mikrozephalie und eine tiefgreifende globale Entwicklungsverzögerung, die mit einer pontozerebellären Hypoplasie Typ 1B ( PCH1B; MIM 614678 ) übereinstimmt .
Liste der Untereinheiten
| Legende | Allgemeiner Name | Domänen | Mensch | Hefe ( S. cerevisiae ) | Archaeen | MW (kD) | Menschliches Gen | Hefe-Gen |
|---|---|---|---|---|---|---|---|---|
| 1 | Csl4 | S1 RBD | hCsl4 | Csl4p/Ski4p | Csl4 | 21–32 | EXOSC1 | YNL232W |
| 2 | Rrp4 | S1/KH RBD | hRrp4 | Rrp4p | Rrp4 | 28–39 | EXOSC2 | YHR069C |
| 3 | UVP40 | S1/KH RBD | hRrp40 | Rrp40p | (Rrp4) | 27–32 | EXOSC3 | YOL142W |
| 4 | Rrp41 | RNase PH | hRrp41 | Rrp41p/Ski6p | Rrp41 | 26–28 | EXOSC4 | YGR195W |
| 5 | Rrp46 | RNase PH | hRrp46 | Rrp46p | (Rrp41) | 25–28 | EXOSC5 | YGR095C |
| 6 | Mtr3 | RNase PH | hMtr3 | Mtr3p | (Rrp41) | 24-37 | EXOSC6 | YGR158C |
| 7 | Rrp42 | RNase PH | hRrp42 | Rrp42p | Rrp42 | 29–32 | EXOSC7 | YDL111C |
| 8 | Rrp43 | RNase PH | OIP2 | Rrp43p | (Rrp42) | 30–44 | EXOSC8 | YCR035C |
| 9 | UVP45 | RNase PH | PM/Scl-75 | Rrp45p | (Rrp42) | 34–49 | EXOSC9 | YDR280W |
| 10 | Rrp6 | RNase D | PM/Scl-100 | Rrp6p | n / A | 84–100 | EXOSC10 | YOR001W |
| 11 | Rrp44 | RNase R | Dis3
Dis3L1 |
Rrp44p/Dis3p | n / A | 105–113 | DIS3 | YOL021C |
- A In Archaeen sind mehrere Exosomenproteine in mehreren Kopien vorhanden, um den vollständigen Kern des Exosomenkomplexes zu bilden.
- B Beim Menschen können in dieser Position zwei verschiedene Proteine assoziiert sein. Im Zytoplasma von Zellen ist Dis3L1 mit dem Exosom assoziiert, während im Zellkern Dis3 an den Kernkomplex binden kann.
- C Trägt zur ribonukleolytischen Aktivität des Komplexes bei.
Siehe auch
- Das Proteasom , die wichtigste Proteinabbaumaschinerie der Zellen
- Das Spleißosom , ein am RNA-Spleißen beteiligter Komplex , der auch eine RNA-bindende Ringstruktur enthält
Verweise
Weiterlesen
- Schilders, G; Pruijn, GJ (2008). Biochemische Untersuchungen des Säugetierexosoms mit intakten Zellen . Methoden Enzymol . Methoden der Enzymologie. 448 . S. 211–226. doi : 10.1016/S0076-6879(08)02611-6 . ISBN 9780123743787. PMID 19111178 .
- Houseley, J; Tollervey, D (2008). "Die nukleare RNA-Überwachungsmaschinerie: die Verbindung zwischen ncRNAs und Genomstruktur in knospenden Hefen?". Biochim Biophys Acta . 1779 (4): 239–246. doi : 10.1016/j.bbagrm.2007.12.008 . PMID 18211833 .
- Vanacova, S; Stefl, R (2007). "Das Exosom und die RNA-Qualitätskontrolle im Zellkern" . EMBO-Berichte . 8 (7): 651–657. doi : 10.1038/sj.embor.7401005 . PMC 1905902 . PMID 17603538 .
- Büttner, K; Wenig, K; Hopfner, KP (2006). „Das Exosom: ein makromolekularer Käfig für den kontrollierten RNA-Abbau“. Molekulare Mikrobiologie . 61 (6): 1372–1379. CiteSeerX 10.1.1.232.6756 . doi : 10.1111/j.1365-2958.2006.05331.x . PMID 16968219 . S2CID 6872855 .
- Lorentzen, E; Conti, E (2006). „Das Exosom und das Proteasom: Nano-Kompartimente für den Abbau“ . Zelle . 125 (4): 651–654. doi : 10.1016/j.cell.2006.05.002 . PMID 16713559 .
- Pruijn, GJ (2005). „Donuts, die sich mit RNA befassen“. Natur Struktur- und Molekularbiologie . 12 (7): 562–564. doi : 10.1038/nsmb0705-562 . PMID 15999107 . S2CID 43218090 .
Externe Links
- Struktur des menschlichen Exosoms in der RCSB Protein Data Bank
- Struktur eines archaealen Exosoms in der RCSB Protein Data Bank
- Struktur eines an RNA gebundenen archaealen Exosoms in der RCSB Protein Data Bank
- Struktur des Hefe-Exosom-Proteins Rrp6 in der RCSB-Proteindatenbank
- 3D-makromolekulare Strukturen von Exosomen in der EM-Datenbank (EMDB)