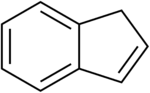
Inden - Indene
|
|

|
|
| Namen | |
|---|---|
|
Bevorzugter IUPAC-Name
1 H -Inden |
|
| Andere Namen
Benzocyclopentadien
Indonaphthen Bicyclo[4.3.0]nona-1,3,5,7-tetraen |
|
| Bezeichner | |
|
3D-Modell ( JSmol )
|
|
| 635873 | |
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| Arzneimittelbank | |
| ECHA-InfoCard |
100.002.176 |
| EG-Nummer | |
| 27265 | |
| KEGG | |
|
PubChem- CID
|
|
| UNII | |
|
CompTox-Dashboard ( EPA )
|
|
|
|
|
|
| Eigenschaften | |
| C 9 H 8 | |
| Molmasse | 116,16 |
| Aussehen | Farblose Flüssigkeit |
| Dichte | 0,997 g/ml |
| Schmelzpunkt | −1,8 °C (28,8 °F; 271,3 K) |
| Siedepunkt | 181,6 °C (358,9 °F; 454,8 K) |
| Unlöslich | |
| Säure (p K a ) | 20.1 (in DMSO) |
| −80,89 × 10 −6 cm 3 /mol | |
| Gefahren | |
| Hauptgefahren | Brennbar |
| Flammpunkt | 78,3 °C (172,9 °F; 351,4 K) |
| NIOSH (US-Grenzwerte für die Gesundheitsbelastung): | |
|
PEL (zulässig)
|
keiner |
|
REL (empfohlen)
|
TWA 10 ppm (45 mg/m 3 ) |
|
IDLH (unmittelbare Gefahr)
|
ND |
| Verwandte Verbindungen | |
|
Verwandte Verbindungen
|
Benzofuran , Benzothiophen , Indol In |
|
Sofern nicht anders angegeben, werden Daten für Materialien in ihrem Standardzustand (bei 25 ° C, 100 kPa) angegeben. |
|
|
|
|
| Infobox-Referenzen | |
Inden ist ein brennbarer polyzyklischer Kohlenwasserstoff mit der chemischen Formel C 9 H 8 . Es besteht aus einem Benzolring , der mit einem Cyclopentenring kondensiert ist. Diese aromatische Flüssigkeit ist farblos, obwohl die Proben oft blassgelb sind. Die hauptsächliche industrielle Verwendung von Inden ist die Herstellung von thermoplastischen Inden/ Cumaron- Harzen. Substituierte Indene und ihre eng verwandten Indanderivate sind wichtige Strukturmotive, die in vielen Naturstoffen und biologisch aktiven Molekülen wie Sulindac vorkommen .
Isolation
Inden kommt natürlicherweise in Kohle-Teer- Fraktionen mit einem Siedepunkt von etwa 175–185 °C vor. Es kann durch Erhitzen dieser Fraktion mit Natrium erhalten werden, um festes "Natriuminden" auszufällen. Dieser Schritt nutzt die schwache Acidität von Inden, die durch seine Deprotonierung durch Natrium nachgewiesen wird, um das Indenyl-Derivat zu ergeben. Die sodio-Inden ist umgewandelte zurück zu Inden durch Dampfdestillation .
Reaktivität
Inden polymerisiert leicht . Oxidation von Inden mit saurem Dichromat ergibt Homophthalsäure ( o -carboxylphenylacetic Säure). Es kondensiert mit Diethyloxalat in Gegenwart von Natriumethoxid zu Inden-Oxalsäureester und mit Aldehyden oder Ketonen in Gegenwart von Alkali zu Benzofulvenen , die stark gefärbt sind. Die Behandlung von Inden mit Organolithium- Reagenzien ergibt Lithium- Indenyl- Verbindungen:
- C 9 H 8 + RLi → LiC 9 H 7 + RH
Indenyl ist ein Ligand in der metallorganischen Chemie , aus dem viele Übergangsmetall-Indenylkomplexe entstehen .
Siehe auch
Verweise
- ^ Internationale Union für reine und angewandte Chemie (2014). Nomenklatur der organischen Chemie: IUPAC-Empfehlungen und bevorzugte Namen 2013 . Die Königliche Gesellschaft für Chemie . s. 207. doi : 10.1039/9781849733069 . ISBN 978-0-8504-182-4.
- ^ a b c d NIOSH Pocket Guide to Chemical Hazards. "#0340" . Nationales Institut für Arbeitssicherheit und Gesundheitsschutz (NIOSH).
- ^ Bordwell FG (1988). „Gleichgewichtssäuren in Dimethylsulfoxid-Lösung“. Konten der chemischen Forschung . 21 (12): 456–463. doi : 10.1021/ar00156a004 . Bordwell pKa-Tabelle in DMSO Archiviert 2008-10-09 bei der Wayback Machine
- ^ Wu, Jie; Qiu, Guanyinsheng (2014). „Erzeugung von Inden-Derivaten durch Tandemreaktionen“. Synlett . 25 (19): 2703–2713. doi : 10.1055/s-0034-1379318 .
- ^ Collin, Gerd; Mildenberg, Rolf; Zander, Mechthild; Höke, Hartmut; McKillip, William; Freitag, Werner; Imöhl, Wolfgang. "Harze, synthetische". Ullmanns Enzyklopädie der Technischen Chemie . Weinheim: Wiley-VCH.
- ^ O'Connor, Joseph M.; Casey, Charles P. (1987). „Ring-Slippage-Chemie von Übergangsmetall-Cyclopentadienyl- und Indenyl-Komplexen“. Chemische Bewertungen . 87 (2): 307–318. doi : 10.1021/cr00078a002 .
Externe Links
- W. v. Miller, Rohde (1890). "Zur Synthese von Indenderivaten" . Berichte der Deutschen Chemischen Gesellschaft . 23 (2): 1881-1886. doi : 10.1002/cber.18900230227 .
- W. v. Miller, Rohde (1890). "Zur Synthese von Indenderivaten" . Berichte der Deutschen Chemischen Gesellschaft . 23 (2): 1887–1902. doi : 10.1002/cber.18900230228 .
- Finar, IL (1985). Organische Chemie . Longman Wissenschaft und Technik. ISBN 0-582-44257-5.
