Simeprevir - Simeprevir
 | |
| Klinische Daten | |
|---|---|
| Aussprache |
/ S ɪ m ɛ p r ə v ɪər / Si- MEP -rə-Veer |
| Namen austauschen | Olysio, Sovriad, Galexos, andere |
| Andere Namen | TMC435; TMC435350 |
| AHFS / Drugs.com | Monographie |
| MedlinePlus | a614013 |
| Lizenzdaten | |
| Wege Verwaltung |
Durch den Mund ( Kapseln ) |
| ATC-Code | |
| Rechtsstellung | |
| Rechtsstellung | |
| Pharmakokinetische Daten | |
| Bioverfügbarkeit | 62 % (unter Fütterungsbedingungen) |
| Proteinbindung | >99,9 % |
| Stoffwechsel | Leber ( CYP3A , CYP2C8 , CYP2C19 ) |
| Beseitigung Halbwertszeit | 10–13 Stunden (HCV-nicht infizierte Personen), 41 Stunden (HCV-infizierte Personen) |
| Ausscheidung | Kot (91%), Urin (<1%) |
| Identifikatoren | |
| |
| CAS-Nummer | |
| PubChem- CID | |
| IUPHAR/BPS | |
| Arzneimittelbank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEMBL | |
| NIAID ChemDB | |
| CompTox-Dashboard ( EPA ) | |
| ECHA-Infokarte |
100.215.933 |
| Chemische und physikalische Daten | |
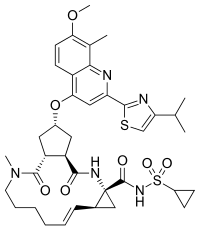
| Formel | C 38 H 47 N 5 O 7 S 2 |
| Molmasse | 749,94 g·mol -1 |
| 3D-Modell ( JSmol ) | |
| |
| |
Simeprevir , das unter dem Handelsnamen verkauft Olysio unter anderem ist ein Medikament in Kombination mit anderen Medikamenten zur Behandlung von gebrauchten Hepatitis C . Es wird speziell bei Hepatitis C Genotyp 1 und 4 angewendet. Zu den Medikamenten, mit denen es angewendet wird, gehören Sofosbuvir oder Ribavirin und Peginterferon-alfa . Heilungsraten liegen bei 80 bis 90 Prozent. Es kann bei Personen angewendet werden, die auch HIV/AIDS haben . Es wird in der Regel 12 Wochen lang einmal täglich oral eingenommen.
Häufige Nebenwirkungen sind Müdigkeit, Kopfschmerzen, Hautausschlag, Juckreiz und Empfindlichkeit gegenüber Sonnenlicht. Bei Patienten mit vorangegangener Hepatitis-B- Infektion kann die aktive Erkrankung erneut auftreten. Es wird nicht bei Patienten mit erheblichen Leberproblemen empfohlen. Während der Schwangerschaft kann es bei Anwendung mit Ribavirin dem Baby schaden, während die Sicherheit bei Anwendung mit Sofosbuvir unklar ist. Simeprevir ist ein HCV-Protease-Hemmer .
Simeprevir wurde von Medivir AB und Janssen Pharmaceutica entwickelt . Es wurde 2013 in den Vereinigten Staaten für die medizinische Verwendung zugelassen. Es wurde 2019 von der Liste der unentbehrlichen Arzneimittel der Weltgesundheitsorganisation gestrichen. Es ist seit 2015 nicht mehr als Generikum erhältlich . Im Vereinigten Königreich eine Behandlung mit Ribavirin und Peginterferon-alfa kosteten 2015 etwa 29.700 £. In den Vereinigten Staaten kostete eine Behandlung mit Sofosbuvir 2015 mehr als 171.000 $, wobei die Simeprevir-Komponente 66.360 $ kostete.
Medizinische Verwendung
Simeprevir ist indiziert zur Behandlung einer chronischen hepatischen C(CHC)-Infektion als Teil eines dreifachen antiviralen Behandlungsschemas, das aus zwei weiteren Medikamenten besteht: Peginterferon-alfa (PEG-IFN) und Ribavirin (RBV). Es ist in erster Linie wirksam bei der Behandlung von Hepatitis-C-Virus (HCV)-Genotyp 1-infizierten Patienten mit kompensierter Lebererkrankung, einschließlich Zirrhose. Derzeit liegen keine Studien vor, die die Wirksamkeit von Simeprevir als Einzeltherapie für HCV belegen. Simeprevir wird im Allgemeinen bei HCV-Genotyp-1-infizierten Patienten angewendet, aber auch für den Typ-4-Genotyp wurde eine Off-Label-medizinische Anwendung angezeigt.
Dosierung
Simeprevir wird zusammen mit Peg-IFN und RBV als Dreifachtherapie verabreicht. Die angemessene Dosierung von Simeprevir hängt von der Leberfunktion, der Nierenfunktion, der Viruslast und dem HCV-Genotyp des Patienten ab . Dieses Medikament wird nicht für Personen mit mittelschwerer oder schwerer Leberfunktionsstörung und Personen mit einer Nierenerkrankung im Endstadium empfohlen, da Simprevir bei diesen Patientengruppen nicht untersucht wurde. Simeprevir kann je nach Viruslast abgesetzt werden. Wenn beispielsweise die Viruslast des Patienten in der 4. Woche des Behandlungsschemas nachweisbar ist (> 25 Einheiten/ml), wird dies als unzureichende Behandlung angesehen und Simeprevir muss abgesetzt werden.
Kontraindikationen
Alle Kontraindikationen für Peg-IFN und RBV gelten für Simeprevir, da sie während der Behandlung von KHK in Kombination angewendet werden müssen. Zum Beispiel sind Menschen mit Sichelzellenanämie für eine RBV-Therapie kontraindiziert und daher für eine Kombinationstherapie mit Simeprevir und Peg-IFN kontraindiziert. Schwangere Frauen und Männer, deren Partnerinnen schwanger sind, sind für Simeprevir kontraindiziert, da bekannt ist, dass Peg-IFN und RBV Geburtsfehler verursachen.
Schwangerschaft
Simeprevir wird bei schwangeren Frauen oder Frauen, die eine Schwangerschaft planen, vermieden, da es zusammen mit RBV und Peg-IFN eingenommen wird, die beide in Tierstudien fetale Probleme verursacht haben. In Tierstudien wurde gezeigt, dass RBV Geburtsfehler und fötale Todesfälle verursacht. In Tierstudien wurde gezeigt, dass Peg-IFN Aborte verursacht. Die Patienten müssen vor Beginn der Therapie einen negativen Schwangerschaftstest haben, während der Behandlung mindestens zwei wirksame Verhütungsmethoden anwenden und sich monatlichen Schwangerschaftstests unterziehen. Wenn schwangere Frauen einem Ribavirin-haltigen Medikamentenschema ausgesetzt sind, werden sie ermutigt, dies über das Ribavirin-Schwangerschaftsregister zu melden.
Nebenwirkungen
Starker Juckreiz (22 %), Sonnenlichtempfindlichkeit (5 %) und Hautausschlag (25 %) sind einige der häufigsten Nebenwirkungen von Simeprevir. Andere Nebenwirkungen können Übelkeit, Muskelschmerzen , Atembeschwerden und erhöhtes Bilirubin sein . Es kann Hepatitis B bei Personen, die zuvor infiziert waren, reaktivieren. Die Europäische Arzneimittel-Agentur (EMA) hat empfohlen, alle Menschen auf Hepatitis B zu untersuchen, bevor Simeprevir auf Hepatitis C begonnen wird, um das Risiko einer Hepatitis-B-Reaktivierung zu minimieren.
Kombinationsbehandlung
Im März 2015 schickte Gilead Sciences per E-Mail Warnungen an Gesundheitsdienstleister über neun Personen, die mit der Einnahme ihrer Hepatitis-C-Medikamente Ledipasvir/Sofosbuvir oder Sofosbuvir zusammen mit Amiodaron , Daclatasvir oder Simeprevir begannen, ungewöhnlich langsame Herzschläge zu entwickeln und einer starb an einem Herzstillstand . Bei drei musste ein Herzschrittmacher eingesetzt werden. Gilead sagte, dass die Kombinationen nicht empfohlen werden und die Produktetiketten aktualisiert werden.
Wirkmechanismus
Simeprevir ist ein Hemmstoff der Hepatitis-C-Virus- Protease .
Simeprevir ist ein NS3/4A-Protease-Inhibitor und verhindert somit die Virusreifung durch Hemmung der Proteinsynthese. Simeprevir wird einmal täglich als eine Kapsel mit pegyliertem Interferon und Ribavirin zur Behandlung der chronischen Hepatitis C vom Genotyp 1 oder Genotyp 4 bei erwachsenen Patienten mit kompensierter Lebererkrankung (einschließlich Zirrhose) mit oder ohne HIV-1-Koinfektion, die in Behandlung sind, verabreicht naiv sind oder bei denen eine vorherige Interferontherapie fehlgeschlagen ist. Genotyp 1 ist die weltweit am häufigsten vorkommende Form des Hepatitis-C-Virus (HCV).
Pharmakokinetik
Simeprevir ist oral bioverfügbar. Seine Resorption nimmt bei Einnahme mit Nahrung zu und es wird daher empfohlen, sie zusammen mit Nahrung einzunehmen. Die CYP3A4-Enzyme der Leber bauen hauptsächlich Simeprevir ab, aber auch CYP2C8- und CYP2C19-Enzyme können eine Rolle spielen. Seine Halbwertszeit im Plasma beträgt bei Menschen mit HCV 41 Stunden. Die maximale Wirkung tritt 4 bis 6 Stunden nach Einnahme des Medikaments ein. Es wird hauptsächlich mit dem Stuhl ausgeschieden (91%).
Pharmakogenomik
Laut den verschreibenden Informationen von Simeprevir ist seine Wirksamkeit in Kombination mit Peginterferon alfa und Ribavirin „bei Menschen mit HCV-Genotyp 1a mit einem NS3-Q80K-Polymorphismus zu Studienbeginn im Vergleich zu Personen, die mit HCV-Genotyp 1a ohne Q80K-Polymorphismus infiziert sind, erheblich reduziert“. Menschen mit Q80K-Polymorphismus wird von der Einnahme von Simeprevir abgeraten.
Wechselwirkungen mit anderen Medikamenten
Simeprevir ist ein CYP3A4- Substrat, daher wird seine Plasmakonzentration bei Einnahme mit Medikamenten, die starke CYP3A4-Inhibitoren sind (z. B. Erythromycin , Ritonavir ) signifikant ansteigen und bei Einnahme mit starken CYP3A4-Induktoren (z. B. Efavirenz , Rifampin , Johanniskraut ) signifikant sinken . Simeprevir hemmt auch CYP3A im Darm (aber nicht in der Leber). Zum Beispiel wird Midazolam , ein Antikonvulsivum, durch intestinales CYP3As metabolisiert und die Einnahme zusammen mit Simeprevir kann zu erhöhten Midazolamspiegeln führen, die toxisch sein können. Simeprevir hemmt auch OATP1B1/3 und P-Glykoprotein (P-gp)-Transporter, bei denen es sich normalerweise um Transporter handelt, die das Medikament aus dem Plasma pumpen. Daher kann die Einnahme von Simeprevir zusammen mit Medikamenten, die Substrate für diese Transporter sind, zu erhöhten Plasmakonzentrationen dieser Medikamente führen. Beispielsweise Calciumkanalblocker (zB Diltiazem , Amlodipin ) ist P-gp - Substrate und kann zu erhöhten Konzentrationen dieser Medikamente führen , wenn sie mit simeprevir genommen. Die Einnahme von Ciclosporin , einem Substrat für OATP1B1/3, mit Simeprevir führte zu einem signifikanten Anstieg der Ciclosporin-Konzentration und wird daher nicht empfohlen, zusammen eingenommen zu werden.
Die Genehmigung
In den Vereinigten Staaten ist es von der Food and Drug Administration (FDA) zur Anwendung in Kombination mit Peginterferon-alfa und Ribavirin bei Hepatitis C zugelassen. Simeprevir ist in Japan zur Behandlung der chronischen Hepatitis-C-Infektion Genotyp 1 zugelassen.
Klinische Studie
Simeprevir wurde in Kombinationstherapien mit pegyliertem Interferon alfa-2a und Ribavirin sowie in interferonfreien Therapien mit anderen direkt wirkenden antiviralen Wirkstoffen, einschließlich Daclatasvir und Sofosbuvir, getestet .
Die Ergebnisse aus drei randomisierten, doppelblinden, placebokontrollierten klinischen Phase-3-Studien (C208, C216 und HPC3007) bei Patienten mit chronischem HCV GT1 waren günstig und führten dazu, dass die FDA die Zulassung von Simeprevir für Hepatitis C Genotyp 1 unterstützte kommentierte nach einer Präsentation von Johnson & Johnson (24. Oktober 2013), dass Studien nach der Markteinführung bei rassischen und ethnischen Minderheiten, Menschen mit HIV-Koinfektion und anderen unterrepräsentierten Bevölkerungsgruppen erforderlich sind.
SARS-CoV-2-Forschung
In mehreren Studien wurde getestet, ob der virostatische Mechanismus von von der FDA zugelassenen direkt wirkenden Wirkstoffen, einschließlich Simeprevir in Kombination mit Remdesivir (ein relevantes Medikament während der Ebola-Epidemie 2014-2016), im Kampf gegen die globale Sars-Cov-Pandemie von Nutzen sein könnte. 2. Paritaprevir , ein weiteres Molekül zur Behandlung von Hepatitis Typ C , zeigte ebenfalls vielversprechende Ergebnisse in Bezug auf die Bindungsenergie und die Stabilität des gebildeten Komplexes.
Der Vorteil bei der Arbeit mit solchen Wirkstoffen besteht darin, dass es sich bereits um von der FDA zugelassene antivirale Mittel handelt, was bedeutet, dass klinische Studienphasen schneller eingeleitet werden können. Die Geschwindigkeit der medizinischen Reaktion ist ein entscheidender Faktor, der die globalen Folgen der Pandemie beeinflusst; je schneller Gegenmittel wie Medikamente und/oder Impfstoffe großflächig verfügbar sind, desto erfolgversprechender ist die Eindämmung der Krankheit und ihrer (wirtschaftlichen) Folgen. Gerade bei der Bekämpfung von Viren, die von Natur aus eine extrem hohe Mutationsrate aufweisen, ist Geschwindigkeit ein entscheidender Faktor .
Bei SARS-CoV-2 wirkt Simeprevir, indem es die Hauptprotease (Mpro) und die RNA- abhängige RNA- Polymerase hemmt , ein nicht-strukturelles Protein , das für die virale RNA-Synthese essentiell ist.
Mpro gehört zur gleichen Enzymklasse wie NS3 / 4A, die Serin - Proteasen . Es spaltet das translatierte Polyprotein, um Proteine zu bilden, die für die virale Transkription und Replikation elementar sind . Remdesivir allein hemmt nur die Polymerase selbst; Um die Virussynthese zu stoppen, wird auch ein zugelassenes Hepatitis-C- Medikament verabreicht, um die Ausbreitung des Virus zu stoppen.
In vitro konnte die Virusinfektion von Sars-CoV-2 gestoppt werden, zudem konnte beobachtet werden, dass weitere Proteasen des Virus gehemmt und somit die Wirkung des Antivirenmittels verstärkt werden konnte. Diesbezüglich fehlen derzeit noch klinische Studien zum Nachweis der Wirksamkeit auf den Organismus, die für den großflächigen Einsatz der Wirkstoffkombination als Therapieform gegen eine Sars-CoV-2-Infektion erforderlich sind .
Die Hepatitis-Medikamente gelten als potenzielle Inhibitoren von SARS-CoV-2 Mpro im Kampf gegen die COVID-19- Infektion, und die Bindungsaffinität und ihr Mechanismus sowie die Stabilität der so gebildeten Komplexe können als Leitlinie oder sogar als Vorlage dienen wenn es darum geht, Inhibitoren zu entwickeln, die speziell auf dieses Virus abzielen. Auch die Verbindungen selbst können eine wichtige Rolle spielen und sollen in klinischen Studien weiter untersucht werden .
Verweise
Weiterlesen
- Dekan L (2016). "Simeprevir-Therapie und IFNL3-Genotyp" . In Pratt VM, McLeod HL, Rubinstein WS et al. (Hrsg.). Zusammenfassungen der medizinischen Genetik . Nationales Zentrum für Biotechnologie-Information (NCBI). PMID 28520373 . Bücherregal-ID: NBK385156.
Externe Links
- "Simeprevir" . Informationsportal für Arzneimittel . US-amerikanische Nationalbibliothek für Medizin.
