Stimulator von Interferon-Genen - Stimulator of interferon genes
Stimulator der Interferon-Gene ( STING ), auch bekannt als Transmembranprotein 173 ( TMEM173 ) und MPYS / MITA / ERIS ist ein Protein , das beim Menschen vom STING1- Gen kodiert wird .
STING spielt eine wichtige Rolle bei der angeborenen Immunität . STING induziert die Produktion von Interferon Typ I, wenn Zellen mit intrazellulären Pathogenen wie Viren , Mykobakterien und intrazellulären Parasiten infiziert werden . Interferon vom Typ I , vermittelt durch STING, schützt infizierte Zellen und benachbarte Zellen vor einer lokalen Infektion, indem es an dieselbe Zelle bindet, die es sezerniert ( autokrine Signalgebung) und benachbarte Zellen ( parakrine Signalgebung). Norovirus- Infektion.
STING funktioniert sowohl als direkter zytosolischer DNA-Sensor (CDS) als auch als Adapterprotein bei der Typ-I-Interferon- Signalübertragung durch verschiedene molekulare Mechanismen. Es hat sich gezeigt , dass es die nachgeschalteten Transkriptionsfaktoren STAT6 und IRF3 durch TBK1 aktiviert , die für die antivirale Reaktion und die angeborene Immunantwort gegen intrazelluläre Pathogene verantwortlich sind .
Struktur
Die Aminosäuren 1–379 des menschlichen STING umfassen die 4 Transmembranregionen (TMs) und eine C-terminale Domäne . Die C-terminale Domäne (CTD: Aminosäuren 138–379) enthält die Dimerisierungsdomäne (DD) und den Carboxy-terminalen Schwanz (CTT: Aminosäuren 340–379).
Der STING bildet in der Zelle ein symmetrisches Dimer. Das STING-Dimer ähnelt einem Schmetterling, mit einer tiefen Spalte zwischen den beiden Protomern. Die hydrophoben Reste von jedem STING-Protomer bilden an der Grenzfläche hydrophobe Wechselwirkungen untereinander.
Ausdruck
STING wird in hämatopoetischen Zellen in peripheren lymphatischen Geweben exprimiert , einschließlich T-Lymphozyten , NK-Zellen , myeloischen Zellen und Monozyten . Es wurde auch gezeigt, dass STING in Lunge, Eierstock , Herz, glatter Muskulatur , Netzhaut , Knochenmark und Vagina stark exprimiert wird .
Lokalisierung
Die subzelluläre Lokalisation von STING wurde als Protein des endoplasmatischen Retikulums aufgeklärt . Außerdem ist es wahrscheinlich, dass STING in unmittelbarer Nähe mit der Mitochondrien-assoziierten ER-Membran (MAM) assoziiert – der Schnittstelle zwischen dem Mitochondrium und dem ER. Während einer intrazellulären Infektion kann STING vom endoplasmatischen Retikulum in perinukleäre Vesikel relokalisieren, die möglicherweise am Exozysten- vermittelten Transport beteiligt sind. Es wurde auch gezeigt, dass STING nach doppelsträngiger DNA-Stimulation mit Autophagie-Proteinen, Mikrotubuli-assoziiertem Protein 1 Leichte Kette 3 (LC3) und Autophagie-verwandtem Protein 9A kolokalisiert , was auf seine Anwesenheit im Autophagosom schließen lässt .
Funktion
STING vermittelt die Typ-I-Interferonproduktion als Reaktion auf intrazelluläre DNA und eine Vielzahl von intrazellulären Pathogenen, einschließlich Viren , intrazellulären Bakterien und intrazellulären Parasiten . Bei einer Infektion kann STING von infizierten Zellen die Anwesenheit von Nukleinsäuren von intrazellulären Pathogenen erkennen und dann die Produktion von Interferon β und mehr als 10 Formen der Interferon α- Produktion induzieren . Interferon vom Typ I, das von infizierten Zellen produziert wird, kann Interferon-alpha/beta-Rezeptoren benachbarter Zellen finden und daran binden , um Zellen vor einer lokalen Infektion zu schützen.
Antivirale Immunität
STING ruft eine starke Typ-I-Interferon-Immunität gegen Virusinfektionen hervor. Nach viralem Eintritt sind virale Nukleinsäuren im Zytosol infizierter Zellen vorhanden. Mehrere DNA-Sensoren wie DAI , RNA-Polymerase III , IFI16 , DDX41 und cGAS können fremde Nukleinsäuren nachweisen . Nach der Erkennung viraler DNA initiieren DNA-Sensoren die nachgeschalteten Signalwege, indem sie die STING-vermittelte Interferonantwort aktivieren.
Adenovirus , Herpes-Simplex-Virus , HSV-1 und HSV-2, sowie das negativsträngige RNA-Virus , das Vesikuläre Stomatitis-Virus (VSV), können eine STING-abhängige angeborene Immunantwort aktivieren.
Ein STING-Mangel bei Mäusen führte aufgrund des Fehlens einer erfolgreichen Typ-I-Interferon-Antwort zu einer tödlichen Anfälligkeit für eine HSV-1-Infektion.
Die Punktmutation von Serin-358 dämpft die Aktivierung von STING-IFN bei Fledermäusen und soll Fledermäusen die Fähigkeit verleihen, als Reservoirwirte zu dienen.
Gegen intrazelluläre Bakterien
Es wurde gezeigt, dass intrazelluläre Bakterien, Listeria monocytogenes , die Immunantwort des Wirts durch STING stimulieren. STING kann eine wichtige Rolle bei der Produktion von MCP-1- und CCL7- Chemokinen spielen. STING-defiziente Monozyten sind während einer Infektion mit Listeria monocytogenes intrinsisch bei der Migration in die Leber defekt . Auf diese Weise schützt STING den Wirt vor einer Infektion mit Listeria monocytogenes , indem es die Monozytenmigration reguliert . Die Aktivierung von STING wird wahrscheinlich durch zyklisches Di-AMP vermittelt, das von intrazellulären Bakterien sezerniert wird.
Sonstiges
STING kann ein wichtiges Molekül für die schützende Immunität gegen infektiöse Organismen sein. Tiere, die STING nicht exprimieren können, sind beispielsweise anfälliger für eine Infektion durch VSV , HSV-1 und Listeria monocytogenes , was auf eine mögliche Korrelation mit menschlichen Infektionskrankheiten hindeutet.
Rolle bei der Wirtsimmunität
Obwohl Typ-I-IFN absolut entscheidend für die Resistenz gegen Viren ist, gibt es eine wachsende Literatur über die negative Rolle von Typ-I-Interferon bei der durch STING vermittelten Wirtsimmunität. Es wurde gezeigt, dass das AT-reiche Stamm-Loop-DNA-Motiv im Genom von Plasmodium falciparum und Plasmodium berghei und extrazelluläre DNA von Mycobacterium tuberculosis Typ-I-Interferon durch STING aktivieren . Die durch das ESX1- Sekretionssystem vermittelte Perforation der Phagosomenmembran ermöglicht der extrazellulären mykobakteriellen DNA den Zugang zu den zytosolischen DNA-Sensoren des Wirts, wodurch die Produktion von Typ-I-Interferon in Makrophagen induziert wird . Eine hohe Typ-I-Interferon- Signatur führt zur Pathogenese von M. tuberculosis und einer verlängerten Infektion. Die STING-TBK1-IRF-vermittelte Typ-I-Interferonantwort ist von zentraler Bedeutung für die Pathogenese der experimentellen zerebralen Malaria bei mit Plasmodium berghei infizierten Labortieren . Labormäuse, denen eine Typ-I-Interferon- Reaktion fehlt, sind resistent gegen experimentelle zerebrale Malaria.
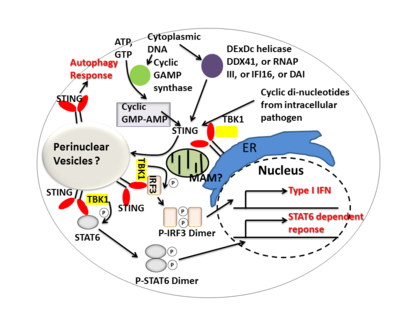
STING-Signalisierungsmechanismen
STINGc mediates Typ I Interferon - Immunantwort sowohl durch als direkten DNA - Sensor wirken kann und ein Signalisierungs Adaptorprotein . Bei Aktivierung stimuliert STING die TBK1- Aktivität, um IRF3 oder STAT6 zu phosphorylieren . Phosphorylierte IRF3s und STAT6s dimerisieren und dringen dann in den Zellkern ein, um die Expression von Genen zu stimulieren, die an der Immunantwort des Wirts beteiligt sind, wie IFNB , CCL2 , CCL20 usw.
Mehrere Berichte deuten darauf hin, dass STING mit der Aktivierung der selektiven Autophagie verbunden ist. Es wurde gezeigt, dass Mycobacterium tuberculosis zytosolische DNA-Liganden produziert, die STING aktivieren, was zur Ubiquitinierung von Bakterien und der anschließenden Rekrutierung von Autophagie- verwandten Proteinen führt, die alle für das „selektive“ autophagische Targeting und die angeborene Abwehr gegen M. tuberculosis erforderlich sind .
Zusammenfassend koordiniert STING mehrere Immunantworten auf Infektionen, einschließlich der Induktion von Interferonen und einer STAT6-abhängigen Antwort sowie einer selektiven Autophagieantwort.
Als zytosolischer DNA-Sensor
Zyklische Dinukleotide – Second-Messenger-Signalmoleküle, die von verschiedenen Bakterienarten produziert werden, wurden im Zytosol von Säugerzellen während einer intrazellulären Pathogeninfektion nachgewiesen; Dies führt zu einer Aktivierung von TBK1 - IRF3 und der nachgelagerten Produktion von Typ - I - Interferon . Es wurde gezeigt, dass STING direkt an zyklisches di-GMP bindet , und diese Erkennung führt zur Produktion von Zytokinen wie Typ-I-Interferon , die für eine erfolgreiche Elimination von Krankheitserregern unerlässlich sind.
Als Signalisierungsadapter
DDX41 , ein Mitglied der DEXDc-Helikasefamilie, erkennt in myeloischen dendritischen Zellen intrazelluläre DNA und vermittelt durch direkte Assoziation mit STING die angeborene Immunantwort. Es wurde auch gezeigt, dass andere DNA-Sensoren – DAI , RNA-Polymerase III , IFI16 , STING durch direkte oder indirekte Wechselwirkungen aktivieren.
Die cyclische GMP-AMP-Synthase (cGAS), die zur Familie der Nukleotidyltransferasen gehört, ist in der Lage, zytosolische DNA-Gehalte zu erkennen und eine STING-abhängige Interferon-Antwort zu induzieren, indem sie den sekundären Botenstoff cyclisches Guanosinmonophosphat-Adenosinmonophosphat (cyclisches GMP-AMP oder cGAMP) produziert. Nach zyklischer GMP-AMP gebunden STING aktiviert wird, erhöht sie TBK1 ‚s - Aktivität phosphoryliert IRF3 und STAT6 für Downstream - Typ - I - Interferon - Antwort.
Es wurde vorgeschlagen, dass intrazelluläres Calcium eine wichtige Rolle bei der Reaktion des STING-Signalwegs spielt.
Verweise
Weiterlesen
- Wang Y, Tong X, Omoregie ES, Liu W, Meng S, Ye X (Okt. 2012). „Tetraspanin 6 (TSPAN6) negativ reguliert Retinsäure-induzierbares Gen I-like - Rezeptor-vermittelte Immun - Signalgebung in einem Ubiquitinierung abhängig“ . Die Zeitschrift für biologische Chemie . 287 (41): 34626–34. doi : 10.1074/jbc.M112.390401 . PMC 3464568 . PMID 22908223 .
- Yin Q, Tian Y, Kabaleeswaran V, Jiang X, Tu D, Eck MJ, Chen ZJ, Wu H (Juni 2012). "Cyclic di-GMP Sensing über das angeborene Immun-Signalprotein STING" . Molekulare Zelle . 46 (6): 735–45. doi : 10.1016/j.molcel.2012.05.029 . PMC 3697849 . PMID 22705373 .
- Aguirre S, Maestre AM, Pagni S, Patel JR, Savage T, Gutman D, Maringer K, Bernal-Rubio D, Shabman RS, Simon V, Rodriguez-Madoz JR, Mulder LC, Barber GN, Fernandez-Sesma A (2012) . "DENV hemmt die Typ-I-IFN-Produktion in infizierten Zellen, indem es humanen STING spaltet" . PLOS-Erreger . 8 (10): e1002934. doi : 10.1371/journal.ppat.1002934 . PMC 3464218 . PMID 23055924 .
- Li Y, Li C, Xue P, Zhong B, Mao AP, Ran Y, Chen H, Wang YY, Yang F, Shu HB (Mai 2009). „ISG56 ist ein Negativ-Feedback-Regulator der Virus-getriggerten Signalübertragung und der zellulären antiviralen Reaktion“ . Proceedings of the National Academy of Sciences of the United States of America . 106 (19): 7945–50. doi : 10.1073/pnas.0900818106 . PMC 2683125 . PMID 19416887 .
- Conlon J, Burdette DL, Sharma S, Bhat N, Thompson M, Jiang Z, Rathinam VA, Mönche B, Jin T, Xiao TS, Vogel SN, Vance RE, Fitzgerald KA (Mai 2013). "Maus, aber kein menschlicher STING, bindet und signalisiert als Reaktion auf das gefäßzerstörende Mittel 5,6-Dimethylxanthenon-4-essigsäure" . Zeitschrift für Immunologie . 190 (10): 5216–25. doi : 10.4049/jimmunol.1300097 . PMC 3647383 . PMID 23585680 .
- Abe T, Harashima A, Xia T, Konno H, Konno K, Morales A, Ahn J, Gutman D, Barber GN (Apr 2013). "STING-Erkennung von zytoplasmatischer DNA initiiert die zelluläre Abwehr" . Molekulare Zelle . 50 (1): 5–15. doi : 10.1016/j.molcel.2013.01.039 . PMC 3881179 . PMID 23478444 .
- Nazmi A, Mukhopadhyay R, Dutta K, Basu A (2012). „STING vermittelt neuronale angeborene Immunantwort nach einer Infektion mit dem Japanischen Enzephalitis-Virus“ . Wissenschaftliche Berichte . 2 : 347. doi : 10.1038/srep00347 . PMC 3317237 . PMID 22470840 .
- Zhang J, Hu MM, Wang YY, Shu HB (August 2012). "TRIM32-Protein moduliert Typ-I-Interferon-Induktion und zelluläre antivirale Antwort, indem es auf das MITA/STING-Protein für die K63-verknüpfte Ubiquitinierung abzielt" . Die Zeitschrift für biologische Chemie . 287 (34): 28646–55. doi : 10.1074/jbc.M112.362608 . PMC 3436586 . PMID 22745133 .
- Ishikawa H, Barber GN (Okt. 2008). „STING ist ein Adapter des endoplasmatischen Retikulums, der die Signalübertragung des angeborenen Immunsystems erleichtert“ . Natur . 455 (7213): 674–8. doi : 10.1038/nature07317 . PMC 2804933 . PMID 18724357 .