Thallium (I) hydroxid - Thallium(I) hydroxide
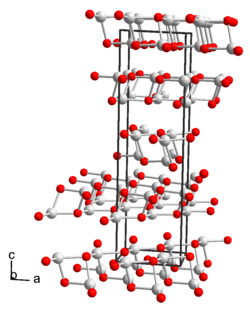
|
|
| Namen | |
|---|---|
|
IUPAC-Name
Thallium (I) -hydroxid
|
|
| Andere Namen
Thallous Hydroxid
|
|
| Kennungen | |
|
3D-Modell ( JSmol )
|
|
| ChemSpider | |
| ECHA InfoCard |
100.031.540 |
|
PubChem CID
|
|
| UNII | |
|
CompTox Dashboard ( EPA )
|
|
|
|
|
|
| Eigenschaften | |
| TlOH | |
| Molmasse | 221,390 g / mol |
| Aussehen | gelbe Nadeln |
| Dichte | 7,44 g / cm 3 |
| Schmelzpunkt | zersetzt sich bei 139 ° C. |
| 34,3 g / 100 g bei 18 ° C. | |
| Gefahren | |
| Hauptgefahren | Sehr giftig (T +)
Ätzend (C) Umweltgefährlich (N) |
|
EU-Klassifizierung (DSD) (veraltet)
|
|
| NFPA 704 (Feuerdiamant) | |
| Thermochemie | |
|
Std molare
Entropie ( S |
88,0 J · mol –1 · K –1 |
|
Std Enthalpie der
Bildung (Δ f H ⦵ 298 ) |
-238,9 kJ · mol −1 |
|
Sofern nicht anders angegeben, werden Daten für Materialien in ihrem Standardzustand (bei 25 ° C, 100 kPa) angegeben. |
|
|
|
|
| Infobox-Referenzen | |
Thallium (I) -hydroxid , die auch als Thallium Hydroxid , TlOH, ist ein Hydroxid von Thallium , mit Thallium in der Oxidationsstufe +1.
Synthese
Thallium (I) hydroxid wird durch Zersetzung von Thallium (I) ethoxid in Wasser erhalten.
- C 2 H 5 OTl + H 2 O → TlOH + C 2 H 5 OH
Dies kann auch durch direkte Reaktion von Thallium mit Ethanol und Sauerstoffgas erfolgen .
- 4 Tl + 2 C 2 H 5 OH + O 2 → 2 C 2 H 5 OTl + 2 TlOH
Ein anderes Verfahren ist die Reaktion zwischen Thallium (I) sulfat und Bariumhydroxid .
- Tl 2 SO 4 + Ba (OH) 2 → 2 TlOH + BaSO 4
Eigenschaften
Thallous Hydroxid ist eine starke Base; distanziert er an die Thalliumionen , Tl + , außer in stark basischen Bedingungen. Tl + ähnelt einem Alkalimetallion A + wie Li + oder K + .
Verweise
| Dieser mit anorganischen Verbindungen verwandte Artikel ist ein Stummel . Sie können Wikipedia helfen, indem Sie es erweitern . |

