Methylmalonyl-CoA-Mutase - Methylmalonyl-CoA mutase
| Methylmalonyl-CoA-Mutase | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Bezeichner | |||||||||
| EG-Nr. | 5.4.99.2 | ||||||||
| CAS-Nr. | 9023-90-9 | ||||||||
| Datenbanken | |||||||||
| IntEnz | IntEnz-Ansicht | ||||||||
| BRENDA | BRENDA-Eintrag | ||||||||
| ExPASy | NiceZyme-Ansicht | ||||||||
| KEGG | KEGG-Eintrag | ||||||||
| MetaCyc | Stoffwechselweg | ||||||||
| PRIAM | Profil | ||||||||
| PDB- Strukturen | RCSB PDB PDBe PDBsum | ||||||||
| Gen-Ontologie | AmiGO / QuickGO | ||||||||
| |||||||||
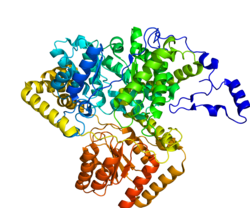
Methylmalonyl-CoA-Mutase (MCM), mitochondrial , auch als Methylmalonyl-CoA-Isomerase bekannt , ist ein Protein, das beim Menschen vom MUT- Gen kodiert wird. Dieses Vitamin B 12 -abhängige Enzym katalysiert die Isomerisierung von Methylmalonyl-CoA zu Succinyl-CoA beim Menschen. Mutationen im MUT- Gen können zu verschiedenen Arten von Methylmalonazidurie führen .
MCM wurde zuerst identifiziert Rattenleber und Schaf Niere 1955. In seiner latenten Form ist es 750 Aminosäuren in der Länge. Beim Eintritt in die Mitochondrien wird die mitochondriale Leadersequenz aus 32 Aminosäuren am N-Terminus des Proteins gespalten, wodurch das vollständig prozessierte Monomer gebildet wird. Die Monomere assoziieren dann zu Homodimeren und binden AdoCbl (eines für jedes aktive Zentrum des Monomers), um die endgültige aktive Holoenzymform zu bilden.
Struktur
Gen
Das MUT- Gen liegt auf der Chromosomenstelle von 6p12.3 und besteht aus 13 Exons , die sich über 35 kb erstrecken.
Protein
Das reife Enzym ist ein Homodimer mit der N-terminalen CoA-Bindungsdomäne und der C-terminalen Cobalamin-Bindungsdomäne.
Funktion
Methylmalonyl-CoA-Mutase wird in hohen Konzentrationen in der Niere , in mittleren Konzentrationen in Herz , Eierstöcken , Gehirn , Muskel und Leber und in niedrigen Konzentrationen in der Milz exprimiert . Das Enzym ist im gesamten zentralen Nervensystem (ZNS) zu finden. MCM befindet sich in den Mitochondrien, wo eine Reihe von Substanzen, darunter die verzweigtkettigen Aminosäuren Isoleucin und Valin sowie Methionin , Threonin , Thymin und ungeradkettige Fettsäuren , über Methylmalonat-Semialdehyd (MMlSA) oder Propionyl-CoA . metabolisiert werden (Pr-CoA) zu einer gemeinsamen Verbindung - Methylmalonyl-CoA (MMl-CoA). MCM katalysiert die reversible Isomerisierung von l‐Methylmalonyl‐CoA zu Succinyl‐CoA, wobei Cobalamin (Vitamin B12) in Form von Adenosylcobalamin (AdoCbl) als Cofaktor benötigt wird. Als wichtiger Schritt im Propionat-Katabolismus ist diese Reaktion für den Abbau von ungeradkettigen Fettsäuren , den Aminosäuren Valin , Isoleucin , Methionin und Threonin sowie Cholesterin erforderlich , die Metaboliten aus dem Abbau dieser Aminosäuren in die Tricarbonsäure leiten Zyklus .
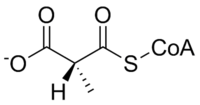
Methylmalonyl-CoA-Mutase katalysiert die folgende Reaktion:
| L-Methylmalonyl-CoA | Methylmalonyl-CoA-Mutase | Succinyl-CoA | |
|

|
||

|
|||
| Methylmalonyl-CoA-Mutase | |||
Das Substrat der Methylmalonyl-CoA-Mutase, Methylmalonyl-CoA , wird hauptsächlich von Propionyl-CoA abgeleitet , einer Substanz, die durch den Abbau und die Verdauung von Isoleucin , Valin , Threonin , Methionin , Thymin , Cholesterin oder ungeradkettigen Fettsäuren gebildet wird. Das Produkt des Enzyms, Succinyl-CoA , ist ein Schlüsselmolekül des Tricarbonsäurezyklus .
Klinische Bedeutung
Ein Mangel dieses Enzyms ist verantwortlich für eine erbliche Stoffwechselstörung, den Methylmalonyl-CoA-Mutase-Mangel , der eine der Ursachen der Methylmalonazidämie (auch Methylmalonazidurie oder MMA genannt) ist. MMA ist ein autosomal-rezessiv vererbter angeborener Stoffwechselfehler, der durch wiederkehrende Episoden von Erbrechen, Lethargie, ausgeprägter Ketoazidose , Hyperammonämie und Panzytopenie im Säuglingsalter gekennzeichnet ist und zu einem frühen Tod führen kann. Komplikationen sind Kardiomyopathie , metabolischer Schlaganfall , Pankreatitis und fortschreitendes Nierenversagen .
Entweder Mutationen des Gens MUT (kodiert für Methylmalonyl-CoA-Mutase) oder MMAA (kodiert ein Chaperon-Protein der Methylmalonyl-CoA-Mutase, MMAA- Protein) können zu einer Methylmalonyl-Azidämie führen. Mutationen zu MUT können entweder als MUT 0 (zeigt selbst in Gegenwart von überschüssigem AdoCbl keine Aktivität) oder MUT 1 (zeigt sehr geringe Aktivität in Gegenwart von überschüssigem AdoCbl) kategorisiert werden. Mehr als die Hälfte der Mutationen von MUT sind Missense-Mutationen, während Nonsense-Mutationen einen signifikanten Rest ausmachen (ca. 14%).
Übliche Behandlungsmethoden für MMA umfassen eine Lebertransplantation oder eine Leber- und Nierentransplantation zur Bekämpfung der Nierenerkrankung Methylmalonazidämie. Aber auch nach einer erfolgreichen Operation können nachteilige neurologische Effekte die Patienten weiter plagen. Es wird angenommen, dass dies auf die weit verbreitete Präsenz von Methylmalonyl-CoA-Mutase im gesamten zentralen Nervensystem zurückzuführen ist. Durch den Verlust der Funktionalität des Enzyms bauen sich Substratspiegel im ZNS auf. Das Substrat L-Methylmalonyl-CoA hydrolysiert zu Methylmalonat (Methylmalonsäure), einer neurotoxischen Dicarbonsäure, die aufgrund der schlechten Dicarbonsäuretransportkapazitäten der Blut-Hirn-Schranke effektiv im ZNS eingeschlossen wird, was zu neurologischen Schwächungen führt. Um diese Effekte zu bekämpfen, werden perioperative antikatabole Regime und kein Absetzen der Diät empfohlen.
Das Mausmodell hat sich als adäquate und genaue Methode zur Untersuchung der Auswirkungen von MMA und potenzieller Behandlungsmethoden erwiesen.
Mechanismus
Der MCM-Reaktionsmechanismus beginnt mit der homolytischen Spaltung der C- Co (III)-Bindung von AdoB12, wobei die C- und Co-Atome jeweils eines der Elektronen aufnehmen, die die gespaltene Elektronenpaarbindung gebildet haben. Das Co-Ion schwankt daher zwischen seinen Co(III)- und Co(II)-Oxidationszuständen [die beiden Zustände sind spektroskopisch unterscheidbar: Co(III) ist rot und diamagnetisch (keine ungepaarten Elektronen), während Co(II) gelb ist und paramagnetisch (ungepaarte Elektronen)]. Daher ist die Rolle von Coenzym B-12 im katalytischen Prozess die eines reversiblen Generators freier Radikale . Die C-Co(III)-Bindung ist schwach mit einer Dissoziationsenergie von 109 kJ/mol und scheint durch sterische Wechselwirkungen mit dem Enzym weiter geschwächt zu werden. Die homolytische Reaktion ist in der Biologie ungewöhnlich, ebenso das Vorhandensein einer Metall-Kohlenstoff-Bindung.
Methylmalonyl-CoA-Mutase ist ein Mitglied der Isomerase- Unterfamilie der Adenosylcobalamin-abhängigen Enzyme. Darüber hinaus wird es als Klasse I eingestuft, da es ein „DMB-off“/„His-on“-Enzym ist. Dies bezieht sich auf die Natur des AdoCbl-Cofaktors im aktiven Zentrum von Methylmalonyl-CoA. AdoCbl besteht aus einem zentralen , bestehend Kobalt -haltigen Corrinrings , einen oberen axialen Ligand (β-axialen Liganden) und einen unteren axialen Liganden (α-Axialliganden). In der Methylmalonyl-CoA-Mutase dissoziierte der β-axiale Ligand 5'-Desoxy-5'-adenosin reversibel zum Desoxyadenosyl-Radikal . Der α-axiale Ligand 5,6-Dimethylbenzimidazol (DMB) ist an der Organisation des aktiven Zentrums beteiligt, damit Histidin -610 anstelle von DMB an Co binden kann (der Grund für die 'DMB-off'/'His-on'-Notation ). Die Bindung des Histidin-610-Restes erhöht die Geschwindigkeit des homolytischen β-axialen Liganden-Co-Bindungsbruchs um den Faktor 10 12 .

Andere wichtige Reste der Methylmalonyl-CoA-Mutase sind Histidin-244, das in der Nähe des Substrats als allgemeine Säure wirkt und die Radikalspezies vor Nebenreaktionen mit Sauerstoff schützt, Glutamat -370, dessen Wasserstoffbrücke mit der 2'-OH-Gruppe der Ribose des β-axialen Liganden erzwingt die Wechselwirkung zwischen der β-axialen Liganden-Radikalspezies und dem Substrat, und Tyrosin -89, das reaktive Radikal-Zwischenstufen stabilisiert und für die Stereoselektivität des Enzyms verantwortlich ist.
Das prozessierende Protein, MMAA- Protein, erfüllt die wichtige Rolle, das Laden und den Austausch von Cofaktoren zu unterstützen. Das MMAA- Protein begünstigt die Assoziation mit dem MCM- Apoenzym und ermöglicht den Transfer des AdoCbl-Cofaktors zum aktiven Zentrum des Enzyms. Wenn das gebundene AdoCbl während der normalen Funktion einen oxidativen Schaden anrichtet, fördert das MMAA- Protein außerdem den Austausch des beschädigten Cofaktors gegen ein neues AdoCbl über einen GTP- abhängigen Weg.
Interaktionen
Verweise
Weiterlesen
- Ledley FD, Rosenblatt DS (1997). „Mutationen in Mut-Methylmalonazidämie: klinische und enzymatische Korrelationen“. Menschliche Mutation . 9 (1): 1–6. doi : 10.1002/(SICI)1098-1004(1997)9:1<1::AID-HUMU1>3.0.CO;2-E . PMID 8990001 .
- Ludwig ML, Matthews RG (1997). „Strukturbasierte Perspektiven auf B12-abhängige Enzyme“. Jahresübersicht der Biochemie . 66 : 269–313. doi : 10.1146/annurev.biochem.66.1.269 . PMID 9242908 .
- Lubrano R, Elli M, Rossi M, Travasso E, Raggi C, Barsotti P, Carducci C, Berloco P (August 2007). "Nierentransplantation bei Methylmalonazidämie: Könnte es die beste Option sein? Bericht über einen Fall nach 10 Jahren und Überprüfung der Literatur". Pädiatrische Nephrologie . 22 (8): 1209–14. doi : 10.1007/s00467-007-0460-z . PMID 17401587 . S2CID 24610554 .
- Frenkel EP, Küchen RL (Dezember 1975). „Intrazelluläre Lokalisation von hepatischer Propionyl-CoA-Carboxylase und Methylmalonyl-CoA-Mutase bei Menschen und normalen und Vitamin-B12-defizienten Ratten“. Britisches Journal für Hämatologie . 31 (4): 501–13. doi : 10.1111/j.1365-2141.1975.tb00885.x . PMID 24458 . S2CID 1232083 .
- Crane AM, Jansen R, Andrews ER, Ledley FD (Februar 1992). „Klonierung und Expression einer mutierten Methylmalonyl-Coenzym-A-Mutase mit veränderter Cobalamin-Affinität, die Mut-Methylmalonazidurie verursacht“ . Das Journal of Clinical Investigation . 89 (2): 385–91. doi : 10.1172/JCI115597 . PMC 442864 . PMID 1346616 .
- Crane AM, Martin LS, Valle D, Ledley FD (Mai 1992). „Phänotyp der Krankheit bei drei Patienten mit identischen Mutationen in Methylmalonyl-CoA-Mutase“. Humangenetik . 89 (3): 259–64. doi : 10.1007/BF00220536 . PMID 1351030 . S2CID 5624280 .
- Raff ML, Crane AM, Jansen R, Ledley FD, Rosenblatt DS (Januar 1991). "Genetische Charakterisierung einer Mutation des MUT-Locus, die Heterogenität bei mut0 und mut-Methylmalonazidurie durch interallelische Komplementation diskriminiert" . Das Journal of Clinical Investigation . 87 (1): 203–7. doi : 10.1172/JCI114972 . PMC 295.026 . PMID 1670635 .
- Jansen R., Ledley FD (November 1990). "Heterozygote Mutationen am Mut-Locus in Fibroblasten mit mut0-Methylmalonazidämie, identifiziert durch Polymerase-Kettenreaktion-cDNA-Klonierung" . Amerikanisches Journal für Humangenetik . 47 (5): 808–14. PMC 1683687 . PMID 1977311 .
- Nham SU, Wilkemeyer MF, Ledley FD (Dezember 1990). „Struktur des menschlichen Methylmalonyl-CoA-Mutase (MUT)-Locus“. Genomik . 8 (4): 710–6. doi : 10.1016/0888-7543(90)90259-W . PMID 1980486 .
- Ledley FD, Lumetta M, Nguyen PN, Kolhouse JF, Allen RH (Mai 1988). "Molekulare Klonierung von L-Methylmalonyl-CoA-Mutase: Gentransfer und Analyse von Mut-Zelllinien" . Proceedings of the National Academy of Sciences of the United States of America . 85 (10): 3518–21. Bibcode : 1988PNAS...85.3518L . doi : 10.1073/pnas.85.10.3518 . PMC 280243 . PMID 2453061 .
- Jansen R, Kalousek F, Fenton WA, Rosenberg LE, Ledley FD (Februar 1989). „Klonierung von Methylmalonyl-CoA-Mutase in voller Länge aus einer cDNA-Bibliothek unter Verwendung der Polymerase-Kettenreaktion“. Genomik . 4 (2): 198–205. doi : 10.1016/0888-7543(89)90300-5 . PMID 2567699 .
- Fenton WA, Hack AM, Kraus JP, Rosenberg LE (März 1987). "Immunchemische Studien an Fibroblasten von Patienten mit Methylmalonyl-CoA-Mutase-Apoenzym-Mangel: Nachweis einer Mutation, die den mitochondrialen Import stört" . Proceedings of the National Academy of Sciences of the United States of America . 84 (5): 1421–4. Bibcode : 1987PNAS...84.1421F . doi : 10.1073/pnas.84.5.1421 . PMC 304442 . PMID 2881300 .
- Zoghbi HY, O'Brien WE, Ledley FD (November 1988). „Verknüpfungsbeziehungen der menschlichen Methylmalonyl-CoA-Mutase zu den HLA- und D6S4-Loci auf Chromosom 6“. Genomik . 3 (4): 396–8. doi : 10.1016/0888-7543(88)90135-8 . PMID 2907507 .
- Kolhouse JF, Utley C, Allen RH (April 1980). "Isolierung und Charakterisierung von Methylmalonyl-CoA-Mutase aus menschlicher Plazenta" . Die Zeitschrift für biologische Chemie . 255 (7): 2708–12. doi : 10.1016/S0021-9258(19)85795-2 . PMID 6102092 .
- Fenton WA, Hack AM, Willard HF, Gertler A, Rosenberg LE (April 1982). „Reinigung und Eigenschaften von Methylmalonyl-Coenzym-A-Mutase aus der menschlichen Leber“. Archiv für Biochemie und Biophysik . 214 (2): 815–23. doi : 10.1016/0003-9861(82)90088-1 . PMID 6124211 .
- Qureshi AA, Crane AM, Matiaszuk NV, Rezvani I, Ledley FD, Rosenblatt DS (April 1994). "Klonierung und Expression von Mutationen, die eine intragene Komplementation bei mut0-Methylmalonazidurie zeigen" . Das Journal of Clinical Investigation . 93 (4): 1812–9. doi : 10.1172/JCI117166 . PMC 294.249 . PMID 7909321 .
- Crane AM, Ledley FD (Juli 1994). „Clustering von Mutationen in Methylmalonyl-CoA-Mutase im Zusammenhang mit Mut-Methylmalonazidämie“ . Amerikanisches Journal für Humangenetik . 55 (1): 42–50. PMC 1918235 . PMID 7912889 .
- Janata J, Kogekar N, Fenton WA (September 1997). „Expression und kinetische Charakterisierung der Methylmalonyl-CoA-Mutase von Patienten mit Mut-Phänotyp: Beweise für natürlich vorkommende interallelische Komplementation“ . Humane molekulare Genetik . 6 (9): 1457–64. doi : 10.1093/hmg/6.9.1457 . PMID 9285782 .
Externe Links
- GeneReviews/NIH/NCBI/UW-Eintrag zu Methylmalonazidämie
- Methylmalonyl-CoA+Mutase in der US National Library of Medicine Medical Subject Headings (MeSH)