Perchlorsäure - Perchloric acid
|
|
|||

|
|||
| Namen | |||
|---|---|---|---|
|
Systematischer IUPAC-Name
Chlor(VII)säure |
|||
| Andere Namen
Hyperchlorsäure
|
|||
| Bezeichner | |||
|
3D-Modell ( JSmol )
|
|||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| ECHA-Infokarte |
100.028.648 |
||
| EG-Nummer | |||
|
PubChem- CID
|
|||
| RTECS-Nummer | |||
| UNII | |||
| UN-Nummer | 1873 | ||
|
CompTox-Dashboard ( EPA )
|
|||
|
|||
|
|||
| Eigenschaften | |||
| HClO 4 | |||
| Molmasse | 100,46 g/mol | ||
| Aussehen | farblose Flüssigkeit | ||
| Geruch | geruchlos | ||
| Dichte | 1,768 g / cm 3 | ||
| Schmelzpunkt | −17 °C (1 °F; 256 K) ( Azeotrop ) −112 °C ( wasserfrei ) |
||
| Siedepunkt | 203 °C (397 °F; 476 K) ( Azeotrop ) | ||
| mischbar | |||
| Säure (p K a ) | -15,2 (±2,0); -10 | ||
| Base konjugieren | Perchlorat | ||
| Gefahren | |||
| Sicherheitsdatenblatt | ICSC 1006 | ||
| GHS-Piktogramme |
   
|
||
| GHS-Signalwort | Achtung | ||
| H271 , H290 , H302 , H314 , H373 | |||
| P210 , P280 , P303+361+353 , P304+340 , P310 , P305+351+338 , P371 , P380 , P375 | |||
| NFPA 704 (Feuerdiamant) | |||
| Flammpunkt | Nicht brennbar | ||
| Verwandte Verbindungen | |||
|
Verwandte Verbindungen
|
Salzsäure Unterchlorige Säure Chlorige Säure Chlorsäure |
||
|
Sofern nicht anders angegeben, beziehen sich die Daten auf Materialien im Standardzustand (bei 25 °C [77 °F], 100 kPa). |
|||
|
|
|||
| Infobox-Referenzen | |||
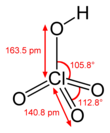
Perchlorsäure ist eine Mineralsäure mit der Formel H Cl O 4 . Diese farblose Verbindung, die normalerweise als wässrige Lösung vorliegt, ist eine stärkere Säure als Schwefelsäure , Salpetersäure und Salzsäure . Es ist ein starkes Oxidationsmittel, wenn es heiß ist, aber wässrige Lösungen bis zu etwa 70 Gew.-% bei Raumtemperatur sind im Allgemeinen sicher und zeigen nur starke Säureeigenschaften und keine oxidierenden Eigenschaften. Perchlorsäure ist nützlich zur Herstellung von Perchloratsalzen , insbesondere von Ammoniumperchlorat , einem wichtigen Raketentreibstoffbestandteil . Perchlorsäure ist gefährlich korrosiv und bildet leicht explosionsfähige Gemische.
Produktion
Perchlorsäure wird industriell auf zwei Wegen hergestellt. Die traditionelle Methode nutzt die hohe Wasserlöslichkeit von Natriumperchlorat (209 g/100 ml Wasser bei Raumtemperatur). Die Behandlung solcher Lösungen mit Salzsäure ergibt Perchlorsäure, wobei festes Natriumchlorid ausfällt:
- NaClO 4 + HCl → NaCl + HClO 4
Die konzentrierte Säure kann durch Destillation gereinigt werden . Der alternative Weg, der direkter ist und Salze vermeidet, beinhaltet die anodische Oxidation von wässrigem Chlor an einer Platinelektrode.
Laborvorbereitungen
Bei der Behandlung von Bariumperchlorat mit Schwefelsäure wird Bariumsulfat ausgefällt , wobei Perchlorsäure zurückbleibt. Es kann auch durch Mischen von Salpetersäure mit Ammoniumperchlorat und Kochen unter Zugabe von Salzsäure hergestellt werden. Die Reaktion liefert Lachgas und Perchlorsäure durch eine gleichzeitige Reaktion mit dem Ammoniumion und kann durch Abkochen der restlichen Salpeter- und Salzsäure deutlich konzentriert und gereinigt werden
Eigenschaften
Wasserfreie Perchlorsäure ist bei Raumtemperatur eine instabile ölige Flüssigkeit. Es bildet mindestens fünf Hydrate , von denen mehrere kristallographisch charakterisiert wurden . Diese Feststoffe bestehen aus dem Perchloratanion, das über Wasserstoffbrückenbindungen an H 2 O- und H 3 O + -Zentren gebunden ist. Perchlorsäure bildet mit Wasser ein Azeotrop , bestehend aus etwa 72,5% Perchlorsäure. Diese Form der Säure ist unbegrenzt stabil und im Handel erhältlich. Solche Lösungen sind hygroskopisch . So verdünnt sich konzentrierte Perchlorsäure, wenn sie der Luft offen gelassen wird, indem sie Wasser aus der Luft aufnimmt.
Dehydratisierung von Perchlorsäure ergibt das Anhydrid Dichlorheptoxid :
- 2 HClO 4 + P 4 O 10 → Cl 2 O 7 + H 2 P 4 O 11
Verwendet
Perchlorsäure wird hauptsächlich als Vorläufer von Ammoniumperchlorat hergestellt , das in Raketentreibstoff verwendet wird. Das Wachstum in der Raketentechnik hat zu einer erhöhten Produktion von Perchlorsäure geführt. Jährlich werden mehrere Millionen Kilogramm produziert. Perchlorsäure ist eines der bewährtesten Materialien zum Ätzen von Flüssigkristallanzeigen und kritischen Elektronikanwendungen sowie zur Erzgewinnung und besitzt einzigartige Eigenschaften in der analytischen Chemie. Außerdem ist es eine nützliche Komponente beim Ätzen von Chrom
Als Säure
Perchlorsäure, eine Supersäure , ist eine der stärksten Brønsted-Lowry-Säuren . Dass sein p K a kleiner als −9 ist, wird durch die Tatsache belegt, dass sein Monohydrat diskrete Hydroniumionen enthält und als stabiler, kristalliner Feststoff isoliert werden kann, formuliert als [H 3 O + ][ ClO–
4]. Die neueste Abschätzung seines wässrigen p K a ist-15,2 ± 2,0 . Es liefert eine starke Acidität mit minimaler Interferenz, da Perchlorat schwach nukleophil ist (was die hohe Acidität von HClO 4 erklärt ). Andere Säuren nichtkoordinierender Anionen , wie Fluorborsäure und Hexafluorphosphorsäure, sind anfällig für Hydrolyse, während Perchlorsäure dies nicht ist. Trotz der mit der Explosivität ihrer Salze verbundenen Gefahren wird die Säure bei bestimmten Synthesen häufig bevorzugt. Aus ähnlichen Gründen ist es ein nützliches Elutionsmittel bei der Ionenaustauschchromatographie.
Es wird auch zum Elektropolieren oder Ätzen von Aluminium, Molybdän und anderen Metallen verwendet.
Sicherheit
Aufgrund ihrer stark oxidierenden Eigenschaften unterliegt Perchlorsäure umfangreichen Vorschriften. Es ist hochreaktiv mit Metallen (zB Aluminium ) und organischen Stoffen (Holz, Kunststoffe). Arbeiten mit Perchlorsäure müssen in Abzugshauben mit Wash-Down-Funktion durchgeführt werden, um eine Ansammlung von Oxidationsmitteln in den Leitungen zu vermeiden.
Am 20. Februar 1947 wurden in Los Angeles, Kalifornien , 17 Menschen getötet und 150 verletzt, als ein Bad, bestehend aus über 1000 Litern 75 Volumenprozent Perchlorsäure und 25 Volumenprozent Essigsäureanhydrid , explodierte. Das Galvanikwerk O'Connor, 25 andere Gebäude und 40 Autos wurden ausgelöscht und 250 benachbarte Häuser beschädigt. Das Bad wurde zum Elektropolieren von Aluminiummöbeln verwendet. Außerdem wurden dem Überhitzungsbad organische Verbindungen zugesetzt, wenn ein Eisengestell durch ein mit Celluloseacetobutyrat ( Tenit-2- Kunststoff) beschichtetes Gestell ersetzt wurde . Ein paar Minuten später explodierte das Bad.
Siehe auch
Verweise
Externe Links
| HClO 4 | Er | ||||||||||||||||
| LiClO 4 | Be(ClO 4 ) 2 |
B(ClO 4)− 4 B(ClO 4 ) 3 |
ROClO 3 |
N(ClO 4 ) 3 NH 4 ClO 4 NOClO 4 |
Ö | FClO 4 | Ne | ||||||||||
| NaClO 4 | Mg(ClO 4 ) 2 | Al(ClO 4 ) 3 | Si | P | S |
ClO− 4 ClOClO 3 Cl 2 O 7 |
Ar | ||||||||||
| KClO 4 | Ca(ClO 4 ) 2 | Sc(ClO 4 ) 3 | Ti(ClO 4 ) 4 |
VO(ClO 4 ) 3 VO 2 (ClO 4 ) |
Cr(ClO 4 ) 3 | Mn(ClO 4 ) 2 | Fe(ClO 4 ) 2 |
Co(ClO 4 ) 2 , Co(ClO 4 ) 3 |
Ni(ClO 4 ) 2 | Cu(ClO 4 ) 2 | Zn(ClO 4 ) 2 | Ga(ClO 4 ) 3 | Ge | Wie | Se | Br | Kr |
| RbClO 4 | Sr(ClO 4 ) 2 | Y(ClO 4 ) 3 | Zr(ClO 4 ) 4 | Nb(ClO 4 ) 5 | Mo | Tc | Ru | Rh(ClO 4 ) 3 | Pd(ClO 4 ) 2 | AgClO 4 | Cd(ClO 4 ) 2 | In(ClO 4 ) 3 | Sn(ClO 4 ) 4 | Sb | TeO(ClO 4 ) 2 | ich | Xe |
| CsClO 4 | Ba(ClO 4 ) 2 | Hf(ClO 4 ) 4 | Ta(ClO 4 ) 5 | W | Betreff | Os | Ir | Pt | Au |
Hg 2 (ClO 4 ) 2 , Hg(ClO 4 ) 2 |
Tl(ClO 4 ) , Tl(ClO 4 ) 3 |
Pb(ClO 4 ) 2 | Bi(ClO 4 ) 3 | Po | Bei | Rn | |
| FrClO 4 | Ra | Rf | Db | Sg | Bh | Hs | Berg | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |
| ↓ | |||||||||||||||||
| La | Ce(ClO 4 ) x | Pr | Nd | Uhr | Sm(ClO 4 ) 3 | Eu(ClO 4 ) 3 | Gd(ClO 4 ) 3 | Tb(ClO 4 ) 3 | Dy(ClO 4 ) 3 | Ho(ClO 4 ) 3 | Er(ClO 4 ) 3 | Tm(ClO 4 ) 3 | Yb(ClO 4 ) 3 | Lu(ClO 4 ) 3 | |||
| Ac | Th(ClO 4 ) 4 | Pa | UO 2 (ClO 4 ) 2 | Np | Pu | Bin | Cm | Bk | Vgl | Es | Fm | Md | Nein | Lr | |||