Silberoxid - Silver oxide
|
|

|
|
| Namen | |
|---|---|
|
IUPAC-Name
Silber(I)oxid
|
|
| Andere Namen
Silberrost, Silberoxid, Silbermonoxid
|
|
| Bezeichner | |
|
3D-Modell ( JSmol )
|
|
| ChemSpider | |
| ECHA-Infokarte |
100.039.946 |
| EG-Nummer | |
| Gittergewebe | Silber+Oxid |
|
PubChem- CID
|
|
| RTECS-Nummer | |
| UNII | |
|
CompTox-Dashboard ( EPA )
|
|
|
|
|
|
| Eigenschaften | |
| Ag 2 O | |
| Molmasse | 231.735 g·mol -1 |
| Aussehen | Schwarze/braune kubische Kristalle |
| Geruch | Geruchlos |
| Dichte | 7,14 g / cm 3 |
| Schmelzpunkt | 300 °C (572 °F; 573 K) zersetzt sich ab ≥200 °C |
| 0,013 g/L (20 °C) 0,025 g/L (25 °C) 0,053 g/L (80 °C) |
|
|
Löslichkeitsprodukt ( K sp ) von AgOH
|
1,52·10 −8 (20 °C) |
| Löslichkeit | Löslich in Säure , Alkali Unlöslich in Ethanol |
| −134,0·10 −6 cm 3 /mol | |
| Struktur | |
| Kubisch | |
| PN 3 m, 224 | |
| Thermochemie | |
|
Wärmekapazität ( C )
|
65,9 J/mol·K |
|
Std molare
Entropie ( S |
122 J/mol·K |
|
Std
Bildungsenthalpie (Δ f H ⦵ 298 ) |
−31 kJ/mol |
|
Gibbs freie Energie (Δ f G ˚)
|
−11,3 kJ/mol |
| Gefahren | |
| GHS-Piktogramme |
 
|
| GHS-Signalwort | Achtung |
| H272 , H315 , H319 , H335 | |
| P220 , P261 , P305+351+338 | |
| NFPA 704 (Feuerdiamant) | |
| Letale Dosis oder Konzentration (LD, LC): | |
|
LD 50 ( mediane Dosis )
|
2,82 g/kg (Ratten, oral) |
| Verwandte Verbindungen | |
|
Verwandte Verbindungen
|
Silber(I,III)-oxid |
|
Sofern nicht anders angegeben, beziehen sich die Daten auf Materialien im Standardzustand (bei 25 °C [77 °F], 100 kPa). |
|
|
|
|
| Infobox-Referenzen | |
Silber(I)-oxid ist die chemische Verbindung mit der Formel Ag 2 O. Es ist ein feines schwarzes oder dunkelbraunes Pulver, das zur Herstellung anderer Silberverbindungen verwendet wird.
Vorbereitung

Silberoxid kann hergestellt werden, indem wässrige Lösungen von Silbernitrat und einem Alkalihydroxid kombiniert werden . Diese Reaktion liefert aufgrund der günstigen Energetik für die folgende Reaktion keine nennenswerten Mengen an Silberhydroxid:
- 2 AgOH → Ag 2 O + H 2 O ( p K = 2,875)
Unter geeignet kontrollierten Bedingungen kann diese Reaktion verwendet werden, um Ag 2 O-Pulver mit Eigenschaften herzustellen, die für verschiedene Anwendungen geeignet sind, einschließlich als feinkörniger leitfähiger Pastenfüllstoff.
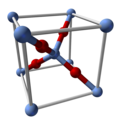
Struktur und Eigenschaften
Ag 2 O weist lineare, zweifach koordinierte Ag-Zentren auf, die durch tetraedrische Oxide verbunden sind. Es ist isostrukturell mit Cu 2 O . Es "löst" sich in Lösungsmitteln auf, die es abbauen. Es ist in Wasser aufgrund der Bildung des Ions Ag(OH) schwer löslich.−
2und möglicherweise verwandte Hydrolyseprodukte. Es ist in Ammoniaklösung löslich und produziert den Wirkstoff von Tollens' Reagenz . Eine Aufschlämmung von Ag 2 O wird leicht von Säuren angegriffen :
- Ag 2 O + 2 HX → 2 AgX + H 2 O
wobei HX = HF , HCl , HBr , HI oder CF 3 COOH ist . Es wird auch mit Lösungen von Alkalichloriden auszufällen reagiert Silberchlorid , so dass eine Lösung des entsprechenden Alkalihydroxid.
Wie viele Silberverbindungen ist Silberoxid lichtempfindlich. Es zersetzt sich auch bei Temperaturen über 280 °C.
Anwendungen
Dieses Oxid wird in Silberoxidbatterien verwendet . In der organischen Chemie wird Silberoxid als mildes Oxidationsmittel verwendet . Es oxidiert beispielsweise Aldehyde zu Carbonsäuren . Solche Reaktionen funktionieren oft am besten, wenn das Silberoxid in situ aus Silbernitrat und Alkalihydroxid hergestellt wird .
Verweise
Externe Links
- Glühen von Silberoxid – Demonstrationsexperiment: Anleitung und Video

