Nickel (II) chlorid - Nickel(II) chloride

|
|
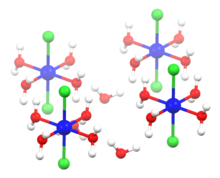 Struktur von Hexahydrat
|
|
 Wasserfrei
|
|
| Namen | |
|---|---|
|
IUPAC-Name
Nickel (II) chlorid
|
|
| Andere Namen
Nickelchlorid, Nickel (II) -salz der Salzsäure
|
|
| Kennungen | |
|
3D-Modell ( JSmol )
|
|
| ChEBI | |
| ChemSpider | |
| ECHA InfoCard |
100.028.858 |
| EG-Nummer | |
| KEGG | |
|
PubChem CID
|
|
| RTECS-Nummer | |
| UNII | |
|
CompTox Dashboard ( EPA )
|
|
|
|
|
|
| Eigenschaften | |
| NiCl 2 | |
| Molmasse | 129,5994 g / mol (wasserfrei) 237,69 g / mol (Hexahydrat) |
| Aussehen | gelbbraune Kristalle zerfließende (wasserfreie) grüne Kristalle (Hexahydrat) |
| Geruch | geruchlos |
| Dichte | 3,55 g / cm 3 (wasserfrei) 1,92 g / cm 3 (Hexahydrat) |
| Schmelzpunkt | 1.001 ° C (1.834 ° F; 1.274 K) (wasserfrei) 140 ° C (Hexahydrat) |
|
wasserfrei 67,5 g / 100 ml (25 ° C) 87,6 g / 100 ml (100 ° C) Hexahydrat 123,8 g / 100 ml (25 ° C) 160,7 g / 100 ml (100 ° C) |
|
| Löslichkeit | 0,8 g / 100 ml ( Hydrazin ), löslich in Ethylenglykol , Ethanol , Ammoniumhydroxid, unlöslich in Ammoniak , Salpetersäure |
| Säure (p K a ) | 4 (Hexahydrat) |
| + 6145,0 · 10 –6 cm 3 / mol | |
| Struktur | |
| Monoklin | |
| oktaedrisch bei Ni | |
| Thermochemie | |
|
Std molare
Entropie ( S |
107 J · mol −1 · K −1 |
|
Std Enthalpie der
Bildung (Δ f H ⦵ 298 ) |
−316 kJ · mol −1 |
| Gefahren | |
| Hauptgefahren | Sehr giftig ( T + ) reizend ( Xi ) umweltgefährlich ( N ) krebserregend |
| Sicherheitsdatenblatt | Fischer Scientific |
|
EU-Klassifikation (DSD) (veraltet)
|
Carc. Katze. 1 Muta. Katze. 3 Repr. Katze. 2 T + Xi N. |
| R-Sätze (veraltet) | R49 , R61 , R23 / 25 , R38 , R42 / 43 , R48 / 23 , R68 , R50 / 53 |
| S-Sätze (veraltet) | S53 , S45 , S60 , S61 |
| NFPA 704 (Feuerdiamant) | |
| Flammpunkt | Nicht brennbar |
| Tödliche Dosis oder Konzentration (LD, LC): | |
|
LD 50 ( mittlere Dosis )
|
105 mg / kg (Ratte, oral) |
| Verwandte Verbindungen | |
|
Andere Anionen
|
Nickel (II) fluorid Nickel (II) bromid Nickel (II) iodid |
|
Andere Kationen
|
Palladium (II) chlorid Platin (II) chlorid Platin (II, IV) chlorid Platin (IV) chlorid |
|
Verwandte Verbindungen
|
Kobalt (II) -chlorid Kupfer (II) -chlorid |
|
Sofern nicht anders angegeben, werden Daten für Materialien in ihrem Standardzustand (bei 25 ° C, 100 kPa) angegeben. |
|
|
|
|
| Infobox-Referenzen | |
Nickel (II) chlorid (oder einfach nur Nickelchlorid ) ist die chemische Verbindung NiCl 2 . Das wasserfreie Salz ist gelb, aber das bekanntere Hydrat NiCl 2 · 6H 2 O ist grün. Nickel (II) -chlorid ist in verschiedenen Formen die wichtigste Nickelquelle für die chemische Synthese. Die Nickelchloride zerfließen und absorbieren Feuchtigkeit aus der Luft, um eine Lösung zu bilden. Es wurde gezeigt, dass Nickelsalze bei längerer Inhalationsexposition krebserregend für Lunge und Nasenwege sind .
Produktion und Synthese
Die größte technische Produktion von Nickelchlorid beinhaltet die Extraktion mit Salzsäure aus Nickel matt und Rückständen aus der Röstung Raffinierung nickelhaltigen Erzen erhalten.
Nickelchlorid wird normalerweise nicht im Labor hergestellt, da es kostengünstig ist und eine lange Haltbarkeit hat. Durch Erhitzen des Hexahydrats im Bereich von 66 bis 133 ° C wird das gelbliche Dihydrat NiCl 2 · 2H 2 O erhalten. Die Hydrate wandeln sich beim Erhitzen in Thionylchlorid oder durch Erhitzen unter einem Strom von HCl-Gas in die wasserfreie Form um . Durch einfaches Erhitzen der Hydrate wird das wasserfreie Dichlorid nicht erhalten.
Die Dehydration geht mit einem Farbwechsel von grün nach gelb einher.
Wenn eine reine Verbindung ohne Kobalt benötigt wird, kann Nickelchlorid erhalten werden, indem Hexaamminenickelchlorid vorsichtig erhitzt wird :
Struktur von NiCl 2 und seinen Hydraten
NiCl 2 nimmt die CdCl 2 -Struktur an . In diesem Motiv ist jedes Ni 2+ -Zentrum an sechs Cl - -Zentren koordiniert und jedes Chlorid an drei Ni (II) -Zentren gebunden. In NiCl 2 haben die Ni-Cl-Bindungen "ionischen Charakter". Gelbes NiBr 2 und schwarzes NiI 2 nehmen ähnliche Strukturen an, jedoch mit einer unterschiedlichen Packung der Halogenide, wobei das CdI 2 -Motiv angenommen wird.
Im Gegensatz dazu besteht NiCl 2 · 6H 2 O aus getrennten trans - [NiCl 2 (H 2 O) 4 ] -Molekülen, die schwächer an benachbarte Wassermoleküle gebunden sind. Nur vier der sechs Wassermoleküle in der Formel sind an das Nickel gebunden, und die verbleibenden zwei sind Kristallwasser . Kobalt (II) chloridhexahydrat hat eine ähnliche Struktur. Das Hexahydrat kommt in der Natur als das sehr seltene Mineral Nickelbischofit vor.
Das Dihydrat NiCl 2 · 2H 2 O nimmt eine Struktur zwischen dem Hexahydrat und den wasserfreien Formen an. Es besteht aus unendlichen Ketten von NiCl 2 , wobei beide Chloridzentren Brückenliganden sind . Die trans-Stellen an den oktaedrischen Zentren sind von Aquoliganden besetzt . Ein Tetrahydrat NiCl 2 · 4H 2 O ist ebenfalls bekannt.
Reaktionen
Nickel (II) -chloridlösungen sind sauer und haben aufgrund der Hydrolyse des Ni 2+ -Ions einen pH-Wert von etwa 4 .
Koordinationskomplexe

Die meisten Reaktionen, die "Nickelchlorid" zugeschrieben werden, betreffen das Hexahydrat, obwohl spezielle Reaktionen die wasserfreie Form erfordern .
Reaktionen von NiCl beginnend 2 · 6H 2 O verwendet werden , um eine Vielzahl von Nickel zu bilden Koordinationskomplexen , weil die H 2 O - Liganden durch schnell verschoben sind Ammoniak , Amine , Thioether , Thiolate und organo Phosphine . In einigen Derivaten verbleibt das Chlorid innerhalb der Koordinationssphäre , während Chlorid durch hochbasische Liganden ersetzt wird. Illustrative Komplexe umfassen:
| Komplex | Farbe | Magnetismus | Geometrie |
|---|---|---|---|
| [Ni (NH 3 ) 6 ] Cl 2 | Blau Violett | paramagnetisch | oktaedrisch |
| [Ni ( en ) 3 ] 2+ | violett | paramagnetisch | oktaedrisch |
| NiCl 2 (dppe) | Orange | diamagnetisch | quadratisch planar |
| [Ni ( CN ) 4 ] 2− | farblos | diamagnetisch | quadratisch planar |
| [NiCl 4 ] 2− | Gelblich-grün | paramagnetisch | tetraedrisch |
Einige Nickelchloridkomplexe existieren als Gleichgewichtsmischung zweier Geometrien; Diese Beispiele sind einige der dramatischsten Darstellungen der Strukturisomerie für eine gegebene Koordinationszahl . Beispielsweise liegt NiCl 2 (PPh 3 ) 2 , das vierfach koordiniertes Ni (II) enthält, in Lösung als Gemisch sowohl der diamagnetischen quadratischen planaren als auch der paramagnetischen tetraedrischen Isomere vor. Quadratische planare Nickelkomplexe können häufig fünffach koordinierte Addukte bilden.
NiCl 2 ist der Vorläufer der Acetylacetonatkomplexe Ni (acac) 2 (H 2 O) 2 und das benzollösliche (Ni (acac) 2 ) 3 , das ein wichtiger Vorläufer von Ni (1,5-Cyclooctadien) 2 ist Reagenz in der Organonickelchemie.
In Gegenwart von Wasserfängern reagiert hydratisiertes Nickel (II) -chlorid mit Dimethoxyethan (dme) unter Bildung des Molekülkomplexes NiCl 2 (dme) 2 . Die dme-Liganden in diesem Komplex sind labil. Beispielsweise reagiert dieser Komplex mit Natriumcyclopentadienid unter Bildung der Sandwichverbindung Nickelocen .
Der Hexammin-Nickelchlorid- Komplex ist löslich, wenn der jeweilige Kobaltkomplex dies nicht ist, was eine einfache Trennung dieser eng verwandten Metalle unter Laborbedingungen ermöglicht.
Anwendungen in der organischen Synthese
NiCl 2 und sein Hydrat sind gelegentlich bei der organischen Synthese nützlich .
- Als milde Lewis-Säure, zB zur regioselektiven Isomerisierung von Dienolen:
- In Kombination mit CrCl 2 zur Kupplung eines Aldehyds und eines Vinyliodids zu Allylalkoholen .
- Zur selektiven Reduktion in Gegenwart von LiAlH 4 , zB zur Umwandlung von Alkenen in Alkane.
- Als Vorläufer für Brown ‚s P-1 und P-2 Nickelborid Katalysator durch die Reaktion mit NaBH 4 .
- Als Vorstufe für feinteiliges Ni durch Reduktion mit Zn zur Reduktion von Aldehyden, Alkenen und nitroaromatischen Verbindungen . Dieses Reagenz fördert auch Homokupplungsreaktionen, dh 2RX → RR, wobei R = Aryl, Vinyl.
- Als Katalysator für die Herstellung von Dialkyl Arylphosphonate aus Phosphite und Aryl Iodid, ArI:
- ArI + P (OEt) 3 → ArP (O) (OEt) 2 + EtI
NiCl 2 -dme (oder NiCl 2 -glyme) wird aufgrund seiner im Vergleich zum Hexahydrat erhöhten Löslichkeit verwendet.
Andere Verwendungen
Nickelchloridlösungen werden zum Galvanisieren von Nickel auf andere Metallgegenstände verwendet.
Sicherheit
Nickel (II) chlorid reizt bei Verschlucken, Einatmen, Hautkontakt und Augenkontakt. Eine längere Inhalationsexposition gegenüber Nickel und seinen Verbindungen wurde mit einem erhöhten Krebsrisiko für die Lunge und die Nasenwege in Verbindung gebracht.
Verweise
- ^ a b Lide, David S. (2003). CRC-Handbuch für Chemie und Physik, 84. Ausgabe . CRC Drücken Sie. S. 4–71. ISBN 9780849304842 .
- ^ a b Zumdahl, Steven S. (2009). Chemische Prinzipien 6. Aufl . Houghton Mifflin Company. p. A22. ISBN 978-0-618-94690-7 .
- ^ "Nickelmetall und andere Verbindungen (als Ni)" . Sofort lebens- oder gesundheitsgefährdend (IDLH) . Nationales Institut für Sicherheit und Gesundheitsschutz am Arbeitsplatz (NIOSH).
- ^ a b Grimsrud, Tom K; Andersen, Aage (2010). "Nachweis der Kanzerogenität wasserlöslicher Nickelsalze beim Menschen" . Zeitschrift für Arbeitsmedizin und Toxikologie . 5 (1): 7. doi : 10.1186 / 1745-6673-5-7 . PMC 2868037 . PMID 20377901 .
- ^ a b Ward, Laird GL (1972). "Wasserfreie Nickel (II) -halogenide und ihre Tetrakis (ethanol) - und 1,2-Dimethoxyethan-Komplexe". Anorganische Synthesen . Anorganische Synthesen. 13 . S. 154–164. doi : 10.1002 / 9780470132449.ch30 . ISBN 9780470132449 .
- ^ Pray, AP (1990). "Wasserfreie Metallchloride". Anorganische Synthesen . 28 : 321–2. doi : 10.1002 / 9780470132593.ch80 . ISBN 9780470132593 .
- ^ Karyakin, Yu.V. (1947). Reine Chemikalien. Handbuch zur Laboraufbereitung anorganischer Substanzen (in russischer Sprache) (Moskau, Leningrad "State Scientific Technical Publishing of Chemical Literature" ed.). p. 416.
- ^ a b Wells, AF Strukturelle Anorganische Chemie , Oxford Press, Oxford , Vereinigtes Königreich , 1984.
- ^ B. Morosin "Eine Röntgenbeugungsstudie an Nickel (II) -chlorid-Dihydrat" Acta Crystallogr. 1967. Band 23, S. 630-634. doi : 10.1107 / S0365110X67003305
- ^ Gill, NS & Taylor, FB (1967). "Tetrahalo-Komplexe dipositiver Metalle in der ersten Übergangsreihe". Anorganische Synthesen . 9 : 136–142. doi : 10.1002 / 9780470132401.ch37 . ISBN 9780470132401 .
- ^ GD Stucky; JB Folkers; TJ Kistenmacher (1967). "Die Kristall- und Molekülstruktur von Tetraethylammoniumtetrachlornickelat (II)". Acta Crystallographica . 23 (6): 1064–1070. doi : 10.1107 / S0365110X67004268 .
- ^ Tien-Yau Luh, Yu-Tsai Hsieh-Nickel (II) -chlorid "in der Enzyklopädie der Reagenzien für die organische Synthese (LA Paquette, Hrsg.) 2001 J. Wiley & Sons, New York. Doi : 10.1002 / 047084289X.rn012 . Artikel online Buchungsdatum: 15. April 2001.
- ^ Cornella, Josep; Edwards, Jacob T.; Qin, Tian; Kawamura, Shuhei; Wang, Jie; Pan, Chung-Mao; Gianatassio, Ryan; Schmidt, Michael; Eastgate, Martin D. (24.02.2016). "Praktische Ni-katalysierte Aryl-Alkyl-Kreuzkupplung von sekundären redoxaktiven Estern" . Zeitschrift der American Chemical Society . 138 (7): 2174–2177. doi : 10.1021 / jacs.6b00250 . PMC 4768290 . PMID 26835704 .
Externe Links
- NIOSH Pocket Guide für chemische Gefahren
- Linstrom, Peter J.; Mallard, William G. (Hrsg.); NIST Chemistry WebBook, NIST-Standardreferenzdatenbank Nr. 69 , Nationales Institut für Standards und Technologie, Gaithersburg (MD), http://webbook.nist.gov



![{\ displaystyle {\ ce {{\ overset {hexammin \ onop nickel ~ chloride} {[Ni (NH3) 6] Cl2}} -> [175-200 ^ {\ circ} {\ ce {C}}] NiCl2 { } + 6NH3}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/196a5da2ce2ec8243534e7bf366995ac5327d0a4)


