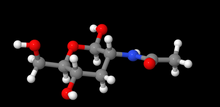
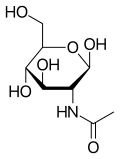
N -Acetylglucosamin - N-Acetylglucosamine

|
|
 |
|
| Namen | |
|---|---|
|
IUPAC-Name
β- D- (Acetylamino)-2-desoxy-glucopyranose
|
|
| Andere Namen
N -Acetyl- D -Glucosamin
GlcNAc NAG |
|
| Bezeichner | |
|
3D-Modell ( JSmol )
|
|
| 1247660 | |
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| ECHA-InfoCard |
100.028.517 |
| EG-Nummer | |
| 721281 | |
| KEGG | |
|
PubChem- CID
|
|
| UNII | |
|
CompTox-Dashboard ( EPA )
|
|
|
|
|
|
| Eigenschaften | |
| C 8 H 15 N O 6 | |
| Molmasse | 221.21 |
| Schmelzpunkt | 211 |
| Verwandte Verbindungen | |
|
Verwandte Monosaccharide
|
N-Acetylgalactosamin |
|
Verwandte Verbindungen
|
Glucosamin Glukose |
|
Sofern nicht anders angegeben, beziehen sich die Daten auf Materialien im Standardzustand (bei 25 °C [77 °F], 100 kPa). |
|
|
|
|
| Infobox-Referenzen | |
N - Acetylglucosamin (GlcNAc) ist ein Amid - Derivat der Monosaccharid Glucose . Es ist ein sekundäres Amid zwischen Glucosamin und Essigsäure . Es ist in mehreren biologischen Systemen von Bedeutung.
Es ist Teil eines Biopolymers in der bakteriellen Zellwand , das aus alternierenden Einheiten von GlcNAc und N- Acetylmuraminsäure (MurNAc) aufgebaut ist, die mit Oligopeptiden am Milchsäurerest von MurNAc vernetzt sind. Diese Schichtstruktur wird Peptidoglycan (früher Murein) genannt.
GlcNAc ist die monomere Einheit des Polymers Chitin , das die Außenskelette von Gliederfüßern wie Insekten und Krebstieren bildet . Es ist der Hauptbestandteil der Radulas von Weichtieren , der Schnäbel von Kopffüßern und ein Hauptbestandteil der Zellwände der meisten Pilze .
Mit Glucuronsäure polymerisiert , bildet es Hyaluronsäure .
Es wurde berichtet, dass GlcNAc ein Inhibitor der Elastase- Freisetzung aus humanen polymorphkernigen Leukozyten ist (Bereich 8–17% Hemmung), jedoch ist dies viel schwächer als die mit N- Acetylgalactosamin beobachtete Hemmung (Bereich 92–100%).
Medizinische Anwendungen
Es wurde zur Behandlung von Autoimmunerkrankungen vorgeschlagen und jüngste Tests haben einige Erfolge gezeigt.
O-GlcNAcylierung
O-GlcNAcylierung ist der Prozess der Zugabe eines einzelnen N- Acetylglucosamin-Zuckers zum Serin oder Threonin eines Proteins. Vergleichbar mit der Phosphorylierung ist die Zugabe oder Entfernung von N- Acetylglucosamin ein Mittel zur Aktivierung oder Deaktivierung von Enzymen oder Transkriptionsfaktoren . Tatsächlich konkurrieren O-GlcNAcylierung und Phosphorylierung oft um die gleichen Serin/Threonin-Stellen. Die O-GlcNAcylierung tritt am häufigsten an Chromatinproteinen auf und wird oft als Reaktion auf Stress angesehen.
Hyperglykämie erhöht die O-GlcNAcylierung, was zu Insulinresistenz führt . Erhöhte O-GlcNAcylierung aufgrund von Hyperglykämie ist offensichtlich eine dysfunktionale Form der O-GlcNAcylierung. Der Rückgang der O-GlcNAcylierung im Gehirn mit zunehmendem Alter ist mit einem kognitiven Rückgang verbunden. Wenn die O-GlcNAcylierung im Hippocampus von gealterten Mäusen erhöht wurde , verbesserten sich räumliches Lernen und Gedächtnis.
Siehe auch
- Keratansulfat
- N- Acetylgalactosamin (GalNAc)
- N- Acetyllactosamin-Synthase
- Weizenkeim-Agglutinin , ein Pflanzenlektin, das an dieses Substrat bindet
Verweise
- ^ Kamel, M.; Hanafi, M.; Bassiouni, M. (1991). „Hemmung der Elastase- Enzymfreisetzung aus humanen polymorphkernigen Leukozyten durch N- Acetyl-Galactosamin und N- Acetyl-Glucosamin“. Klinische und experimentelle Rheumatologie . 9 (1): 17–21. PMID 2054963 .
- ^ Grigorian A, Araujo L, Naidu NN, Place DJ, Choudhury B, Demetriou M (2011). „N-Acetylglucosamin hemmt die Zellantworten von T-Helfer 1 (Th1)/T-Helfer 17 (Th17) und behandelt experimentelle Autoimmun-Enzephalomyelitis“ . Zeitschrift für biologische Chemie . 286 (46): 40133–40141. doi : 10.1074/jbc.M111.277814 . PMC 3220534 . PMID 21965673 .
- ^ a b c d Hart GW, Slawson C, Ramirez-Correa G, Lagerlof O (2011). "Crosstalk zwischen O-GlcNAcylation und Phosphorylation: Rollen bei der Signalübertragung, Transkription und chronischen Erkrankungen" . Jahresübersicht der Biochemie . 80 : 825–858. doi : 10.1146/annurev-biochem-060608-102511 . PMC 3294376 . PMID 21391816 .
- ^ Ma J, Hart GW (2013). "Protein O-GlcNAcylation bei Diabetes und diabetischen Komplikationen" . Expertenreview der Proteomik . 10 (4): 365–380. doi : 10.1586/14789450.2013.820536 . PMC 3985334 . PMID 23992419 .
- ^ Wheatley EG, Albarran E, White CW 3rd, Bieri G, Sanchez-Diaz C, Pratt K, Snethlage CE, Ding JB, Villeda SA (2019). „Neuronale O-GlcNAcylation verbessert die kognitive Funktion im gealterten Mausgehirn“ . Aktuelle Biologie . 29 (20): 3359–3369. doi : 10.1016/j.cub.2019.08.003 . PMC 7199460 . PMID 31588002 .