Organocadmiumverbindung - Organocadmium compound
Eine Organocadmium Verbindung ist eine organometallische Verbindung , enthaltend ein Kohlenstoff auf Cadmium chemische Bindung . Die Organocadmiumchemie beschreibt physikalische Eigenschaften, Synthese, Reaktionen und Verwendung dieser Verbindungen. Cadmium teilt sich mit Zink und Quecksilber die Gruppe 12, und die entsprechenden Chemikalien haben viel gemeinsam.
Eines der einfachsten Beispiele ist Dimethylcadmium mit einer C-Cd- Bindungslänge von 213 pm . Alle Organocadmiumverbindungen sind empfindlich gegenüber Luft, Licht und Feuchtigkeit.
Synthese
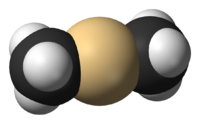
Die ersten Organocadmiumverbindungen , Dimethylcadmium , CH 3 -Cd-CH 3 , und Diethylcadmium, CH 3 CH 2 -Cd-CH 2 CH 3 , wurden 1917 von Erich Krause hergestellt. Im Allgemeinen werden sie durch Transmetallierung oder durch eine Austauschreaktion zwischen einem metallorganischen Reagens und einem Cadmiumsalz hergestellt.
Ein Verfahren zur Synthese von Diethylcadmium besteht in der Reaktion von Cadmiumbromid mit zwei Äquivalenten des Grignard-Reagenz Ethylmagnesiumbromid in Diethylether . Diethylcadmium ist ein farbloses Öl mit einem Schmelzpunkt von −21 °C .
Diphenylcadmium kann durch die Reaktion von Phenyllithium mit Cadmiumbromid hergestellt werden. Diphenylcadmium ist ein Feststoff mit einem Schmelzpunkt von 174 °C.
Fluoralkyl- und Alkenylderivate
Den etablierten Trends folgend, zeigen perfluorierte Alkyl- und Alkenylderivate von Cadmium eine verbesserte thermische Stabilität. Die Alkenylderivate werden durch die Addition von Iodtrifluorethylen an Cadmiummetall erzeugt.
Reaktionen
Der synthetische Nutzen von Organocadmium ist begrenzt. Sie sind weniger nukleophil als die Organozinks . Diese reduzierte Reaktivität zeigt sich bei der Umwandlung von Acylchloriden in Ketone mit diesen Reagenzien. Diese Reaktion wurde 1936 von Henry Gilman beschrieben und wurde verwendet, bis weniger giftige Cuprate verfügbar waren. Das verwandte Grignard-Reagens würde weiter reagieren und den tertiären Alkohol ergeben . Methyl-Cadmium wurde in einem der Schritte verwendet, die zur Cholesterin-Totalsynthese führten :
Ein weiteres Beispiel für die synthetische Verwendung eines Organocadmiums ist die Umsetzung von Diisoamylcadmium mit β-Carbomethoxypropionylchlorid zu 4-Keto-7-methyloctanosäuremethylester ohne weitere Reaktion mit der Ketongruppe oder der Estergruppe .
Diese Selektivität ist gegeben, sofern die Reaktion salzfrei durchgeführt wird. Wenn das Cadmiumreagens in situ aus einem Cadmiumsalz erzeugt wird, erzeugt das Halogenid ein nukleophileres Organocadmiumreagenz, einen at-Komplex . Der gleiche Salzeffekt kann bei Organozinkverbindungen beobachtet werden.
Dimethylcadmium wurde auch verwendet, um kolloidale Nanokristalle aus II-VI-Materialien zu synthetisieren. Seine toxische und flüchtige Natur hat Forscher dazu veranlasst, anderswo nach Cadmiumvorläufern wie Cadmiumoxid zu suchen.
Toxizität
Cadmiumverbindungen sind giftig. Dimethylcadmium ist beim Einatmen giftig für die Nieren, die Leber, das zentrale Nervensystem und die Atmungsorgane. Cadmiumverbindungen werden von der IARC im Allgemeinen als krebserregend für den Menschen angesehen .
Siehe auch
- Andere Chemien des Kohlenstoffs mit anderen Elementen der Gruppe 12 : Organozinkverbindungen und Organoquecksilberverbindungen .
Verweise
- ^ Synthetische Methoden der Organometallischen und Anorganischen Chemie Bd. 5, Kupfer, Silber, Gold, Zink, Cadmium und Quecksilber WA Herrmann Ed. ISBN 3-13-103061-5
- ^ Felix Hanke; Sarah Hindley; Anthony C. Jones; Alexander Steiner (2016). „Die Festkörperstrukturen der Hoch- und Niedertemperaturphasen von Dimethylcadmium“. Chemische Kommunikation . 52 (66): 10144–10146. doi : 10.1039/c6cc05851e . PMID 27457504 .
- ^ Erich Krause (1917). "Einfache Cadmiumdialkyle. (I. Mitteilung über organische Cadmium-Verbindungen.)" . Berichte der deutschen chemischen Gesellschaft . 50 (2): 1813–1822. doi : 10.1002/cber.19170500292 .
- ^ Burton, Donald J.; Yang, Zhen-Yu; Morken, Peter A. (1994). „Fluorierte organometallische Stoffe: Vinyl, Alkinyl, Allyl, Benzyl, Propargyl und Aryl“. Tetraeder . 50 (10): 2993–3063. doi : 10.1016/S0040-4020(01)81105-4 .
- ^ David A. Shirley (2011). „Die Synthese von Ketonen aus Säurehalogeniden und metallorganischen Verbindungen von Magnesium, Zink und Cadmium“. Org. Reaktionen . doi : 10.1002/0471264180.or008.02 .
- ^ Woodward, RB; Sondheimer, Franz; Taub, David; Heusler, Karl; McLamore, WM (1952). „Die Totalsynthese von Steroiden“. Zeitschrift der American Chemical Society . 74 (17): 4223–51. doi : 10.1021/ja01137a001 .
- ^ Cason, James; Proutjahr = 1948, Franklin S. "Methyl-4-Keto-7-Methyloctanoat". Organische Synthesen . 28 : 75. doi : 10.15227/orgsyn.028.0075 .
- ^ Jones, Paul R.; Desio, Peter J. (1978). „Die weniger bekannten Reaktionen von Organocadmium-Reagenzien“. Chemische Bewertungen . 78 (5): 491–516. doi : 10.1021/cr60315a001 .
- ^ Peng ZA, Peng X (2001). „Bildung von hochwertigen CdTe-, CdSe- und CdS-Nanokristallen mit CdO als Vorstufe“. Zeitschrift der American Chemical Society . 123 (1): 183–4. doi : 10.1021/ja003633m . PMID 11273619 .
- ^ http://www.cchem.berkeley.edu/~pagrp/index.html
- ^ Spiridonova EIa (1991). „[Experimentelle Studie der toxischen Eigenschaften von Dimethylcadmium]“. Gigiena Truda I Professional'nye Zabolevaniia (auf Russisch) (6): 14–7. PMID 1916391 .
- ^ http://monographs.iarc.fr/ENG/Monographs/vol100C/mono100C-8.pdf