Transglutaminase - Transglutaminase
| Transglutaminase | |||||||||
|---|---|---|---|---|---|---|---|---|---|
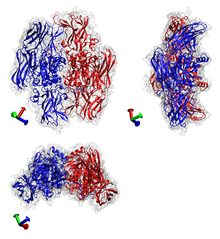 Transglutaminase-Beispiel: Gerinnungsfaktor XIII aus menschlichem Blut. PDB-Code: 1EVU.
| |||||||||
| Kennungen | |||||||||
| EG-Nr. | 2.3.2.13 | ||||||||
| CAS-Nr. | 80146-85-6 | ||||||||
| Datenbanken | |||||||||
| IntEnz | IntEnz-Ansicht | ||||||||
| BRENDA | BRENDA Eintrag | ||||||||
| EXPASy | NiceZyme Ansicht | ||||||||
| KEGG | KEGG Eintrag | ||||||||
| MetaCyc | Stoffwechselweg | ||||||||
| PRIAM | Profil | ||||||||
| PDB- Strukturen | RCSB PDB PDBe PDBsum | ||||||||
| |||||||||
Transglutaminasen sind Enzyme , die hauptsächlich in der Natur katalysiert die Bildung einer Isopeptidbindung zwischen γ- Carboxamid - Gruppen (- (C = O) NH 2 ) von Glutamin - Rest - Seitenketten und dem ε- Aminogruppen (-NH 2 ) der Lysin - Rest - Seitenketten mit anschließender Freisetzung von Ammoniak (NH 3 ). Lysin- und Glutaminreste müssen an ein Peptid oder ein Protein gebunden sein, damit diese Vernetzung (zwischen getrennten Molekülen) oder intramolekulare Reaktion (innerhalb desselben Moleküls) stattfinden kann. Durch Transglutaminase gebildete Bindungen zeigen eine hohe Beständigkeit gegen proteolytischen Abbau ( Proteolyse ). Die Reaktion ist
- Gln- (C = O) NH 2 + NH 2 -Lys → Gln- (C = O) NH-Lys + NH 3
Transglutaminasen können auch ein primäres Amin (RNH 2 ) an die Seitenkettencarboxyamidgruppe eines Protein / Peptid-gebundenen Glutaminrests binden und so eine Isopeptidbindung bilden
- Gln- (C = O) NH 2 + RNH 2 → Gln- (C = O) NHR + NH 3
Diese Enzyme können auch Glutaminreste in Gegenwart von Wasser zu Glutaminsäureresten desamidieren
- Gln- (C = O) NH 2 + H 2 O → Gln-COOH + NH 3
Transglutaminase , isoliert aus Streptomyces mobaraensis - Bakterien ist beispielsweise ein Calcium- -unabhängigen Enzym. Säugetier- Transglutaminasen benötigen neben anderen Transglutaminasen Ca 2+ -Ionen als Cofaktor .
Transglutaminasen wurden zum ersten Mal entdeckt wurde im Jahr 1959 Die genaue biochemische Aktivität von Transglutaminase beschrieben Blutgerinnungsprotein Faktor XIII im Jahr 1968.
Beispiele

Beim Menschen wurden neun Transglutaminasen charakterisiert, von denen acht Transamidierungsreaktionen katalysieren. Diese TGasen haben eine Organisation mit drei oder vier Domänen, wobei Immunglobulin- ähnliche Domänen die zentrale katalytische Domäne umgeben. Die Kerndomäne gehört zur Superfamilie der Papain (CA-Clans) und verwendet eine katalytische Cys-His-Asp- Triade . Protein 4.2 , auch als Bande 4.2 bezeichnet, ist ein katalytisch inaktives Mitglied der menschlichen Transglutaminase-Familie, das an der katalytischen Triade eine Cys-Ala-Substitution aufweist.
| Name | Gen | Aktivität | Chromosom | OMIM |
|---|---|---|---|---|
| Faktor XIII (Fibrinstabilisierungsfaktor) Kette A. | F13A1 | Koagulation | 6p25-p24 | 134570 |
| Keratinozyten-Transglutaminase | TGM1 | Haut | 14q11.2 | 190195 |
| Gewebetransglutaminase | TGM2 | allgegenwärtig | 20q11.2-q12 | 190196 |
| Epidermale Transglutaminase | TGM3 | Haut | 20q12 | 600238 |
| Prostatatransglutaminase | TGM4 | Prostata | 3p22-p21.33 | 600585 |
| TGM X. | TGM5 | Haut | 15q15.2 | 603805 |
| TGM Y. | TGM6 | Nerven, ZNS | 20q11-15 | 613900 |
| TGM Z. | TGM7 | Hoden, Lunge | 15q15.2 | 606776 |
| Protein 4.2 | EPB42 | Erythrozyten, Knochenmark, Milz | 15q15.2 | 177070 |
Bakterielle Transglutaminasen sind Einzeldomänenproteine mit einem ähnlich gefalteten Kern. Die in einigen Bakterien gefundene Transglutaminase läuft auf einer Cys-Asp-Diade.
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Biologische Rolle
Transglutaminasen bilden stark vernetzte, im Allgemeinen unlösliche Proteinpolymere. Diese biologischen Polymere sind für einen Organismus unverzichtbar, um Barrieren und stabile Strukturen zu schaffen. Beispiele sind Blutgerinnsel (Gerinnungsfaktor XIII ) sowie Haut und Haare . Die katalytische Reaktion wird im Allgemeinen als irreversibel angesehen und muss durch umfangreiche Kontrollmechanismen genau überwacht werden.
Rolle bei Krankheiten
Ein Mangel an Faktor XIII (eine seltene genetische Erkrankung) prädisponiert für Blutungen ; Konzentriertes Enzym kann verwendet werden, um die Anomalie zu korrigieren und das Blutungsrisiko zu verringern.
Anti-Transglutaminase-Antikörper werden bei Zöliakie gefunden und können eine Rolle bei der Dünndarmschädigung als Reaktion auf Gliadin aus der Nahrung spielen , das diesen Zustand charakterisiert. Bei der verwandten Erkrankung Dermatitis herpetiformis , bei der häufig Dünndarmveränderungen festgestellt werden und die auf den Ausschluss von Gliadin-haltigen Weizenprodukten aus der Nahrung reagiert, ist die epidermale Transglutaminase das vorherrschende Autoantigen.
Jüngste Forschungsergebnisse zeigen, dass Patienten mit neurologischen Erkrankungen wie Huntington und Parkinson ungewöhnlich hohe Konzentrationen einer Art von Transglutaminase, der Gewebetransglutaminase, aufweisen können . Es wird angenommen, dass Gewebetransglutaminase an der Bildung der Proteinaggregate beteiligt sein kann, die die Huntington-Krankheit verursachen, obwohl dies höchstwahrscheinlich nicht erforderlich ist.
Mutationen in der Keratinozyten-Transglutaminase sind an der lamellaren Ichthyose beteiligt .
Strukturstudien
Bis Ende 2007 wurden 19 Strukturen für diese Klasse von Enzymen mit den PDB- Zugangscodes 1EVU , 1EX0 , 1F13 , 1FIE , 1G0D , 1GGT , 1GGU , 1GGY , 1IU4 , 1KV3 , 1L9M , 1L9N , 1NUD , 1NUF , 1NUG , gelöst 1QRK , 1RLE , 1SGX und 1VJJ .
Industrielle und kulinarische Anwendungen

In der kommerziellen Lebensmittelverarbeitung wird Transglutaminase verwendet, um Proteine miteinander zu verbinden. Beispiele für Lebensmittel, die unter Verwendung von Transglutaminase hergestellt wurden, umfassen nachgeahmtes Krabbenfleisch und Fischbällchen . Es wird durch Streptoverticillium mobaraense- Fermentation in kommerziellen Mengen ( P81453 ) hergestellt oder aus tierischem Blut extrahiert und wird in einer Vielzahl von Prozessen verwendet, einschließlich der Herstellung von verarbeitetem Fleisch und Fischprodukten .
Transglutaminase kann als Bindemittel verwendet werden, um die Textur von proteinreichen Lebensmitteln wie Surimi oder Schinken zu verbessern .
Thrombin - Fibrinogen " Fleischkleber " aus Rinder- und Schweinequellen wurde 2010 in der gesamten Europäischen Union als Lebensmittelzusatzstoff verboten. Transglutaminase ist weiterhin zulässig und muss nicht deklariert werden, da es sich um ein Verarbeitungshilfsmittel handelt und nicht um einen Zusatzstoff, der vorhanden bleibt im Endprodukt.
Molekulargastronomie
Transglutaminase wird auch in der Molekularküche verwendet , um neue Texturen mit dem bestehenden Geschmack zu verschmelzen. Neben diesen Hauptanwendungen wurde Transglutaminase verwendet, um einige ungewöhnliche Lebensmittel herzustellen. Dem britischen Küchenchef Heston Blumenthal wird die Einführung von Transglutaminase in die moderne Küche zugeschrieben.
Wylie Dufresne , Chef der New Yorker Avantgarde- Restaurant wd ~ 50 , wurde Transglutaminase von Blumenthal eingeführt, und erfand eine " Pasta " aus mehr als 95% Garnelen dank Transglutaminase.
Synonyme
- Protein-Glutamin-Gamma-Glutamyltransferase (systematisch)
- Fibrinoligase
- Glutaminylpeptid-Gamma-Glutamyltransferase
- Protein-Glutamin: Amin-Gamma-Glutamyltransferase
- R-Glutaminylpeptid: Amin-Gamma-Glutamyltransferase
Siehe auch
Verweise
Weiterführende Literatur
- Fesus L., Hitomi K., Kojima S. (2015). Transglutaminasen: Mehrere funktionelle Modifikatoren und Ziele für die Entdeckung neuer Arzneimittel . Springer Japan. ISBN 978-4-431-55823-1 .
- Nuijens T, Schmidt M (2019). Enzymvermittelte Ligationsmethoden . Humana, New York, NY. ISBN 978-1-4939-9545-5 .
- Kuddus M (2018). Enzyme in der Lebensmitteltechnologie: Verbesserungen und Innovationen . Springer, Singapur. ISBN 978-981-13-1932-7 .
- Kelleher JB (11. Mai 2012). "Industrie verteidigt Zutatenkritiker verspotten als" Fleischkleber " " . Chicago Tribune . Abgerufen am 20. Juli 2012 .
- US-Patent 5,156,956 - Eine Transglutaminase, die eine Acyltransferreaktion einer Γ-Carboxyamidgruppe eines Glutaminrests in einer Peptid- oder Proteinkette in Abwesenheit von Ca 2+ katalysiert

