Organoarsen-Chemie - Organoarsenic chemistry
Organoarsenchemie ist die Chemie von Verbindungen, die eine chemische Bindung zwischen Arsen und Kohlenstoff enthalten . Einige Organoarsenverbindungen, auch "Organoarsenicals" genannt, werden industriell mit Verwendung als Insektizide , Herbizide und Fungizide hergestellt . Im Allgemeinen nehmen diese Anwendungen im Zuge der wachsenden Besorgnis über ihre Auswirkungen auf die Umwelt und die menschliche Gesundheit ab. Die Stammverbindungen sind Arsin und Arsensäure . Trotz ihrer Toxizität sind Organoarsen- Biomoleküle gut bekannt.
Geschichte
Überraschend für ein Gebiet, das heute als untergeordnet gilt, spielte die arsenorganische Chemie eine herausragende Rolle in der Geschichte der Chemie. Die älteste bekannte organoarsenische Verbindung, das übel riechende Cacodyl, wurde in "Cacodyl" (1760) beschrieben und wird manchmal als die erste synthetische metallorganische Verbindung eingestuft . Der Wirkstoff Salvarsan war eines der ersten Arzneimittel, das für Paul Ehrlich einen Nobelpreis erhielt . Verschiedene andere arsenorganische Verbindungen fanden früher Verwendung als Antibiotika (Solarson) oder andere medizinische Anwendungen.
Synthese und Klassifizierung
Arsen tritt typischerweise in den Oxidationsstufen (III) und (V) auf, veranschaulicht durch die Halogenide AsX 3 (X = F, Cl, Br, I) und AsF 5 . Dementsprechend werden arsenorganische Verbindungen häufig in diesen beiden Oxidationsstufen gefunden.
Die Hydroxyarsenverbindungen sind bekannt:
- arsenige Säuren (RAs(OH) 2 ), selten ( arsenige Säure (As(OH) 3 ) ist bekannt)
- arsinöse Säuren (R 2 AsOH), selten
- Arsinsäuren (R 2 As(O)OH), häufig, veranschaulicht durch Kakodylsäure (R = CH 3 )
- Arsonsäuren (RAs(O)(OH) 2 ), häufig, veranschaulicht durch Phenylarsonsäure (R = C 6 H 5 )
Organoarsen(V)-Chemie und Verwendungen
Arsen(V)-Verbindungen weisen typischerweise die funktionellen Gruppen RAsO(OH) 2 oder R 2 AsO(OH) auf (R = Alkyl oder Aryl). Die Biomethylierung von Arsenverbindungen beginnt mit der Bildung von Methanarsonaten . So werden dreiwertige anorganische Arsenverbindungen zu Methanarsonat methyliert. S- Adenosylmethionin ist der Methyldonor. Die Methanarsonate sind die Vorläufer von Dimethylarsonaten, wiederum durch den Reduktionszyklus (zur Methylarsonsäure) gefolgt von einer zweiten Methylierung. Diese Dimethylverbindung ist Cacodylsäure ((CH 3 ) 2 AsO 2 H), die in der Chemie der Organoarsenverbindungen eine herausragende Rolle spielt. Im Gegensatz dazu ist die Dimethylphosphonsäure in der entsprechenden Phosphorchemie weniger bedeutsam. Cacodylsäure entsteht aus der Methylierung von Arsen(III)-oxid. Phenylarsonsäuren sind durch die Reaktion von Arsensäure mit Anilinen , der sogenannten Bechamp-Reaktion, zugänglich .
Die monomethylierte Säure Methanarsonsäure (CH 3 AsO(OH) 2 ) ist eine Vorstufe von Fungiziden (Handelsname Neoasozin) im Reis- und Baumwollanbau. Derivate der Phenylarsonsäure (C 6 H 5 AsO(OH) 2 ) werden als Futterzusatzstoffe für Nutztiere verwendet, einschließlich 4-Hydroxy-3-nitrobenzolarsonsäure (3-NHPAA oder Roxarsone), Ureidophenylarsonsäure und p- Arsanilsäure . Diese Anwendungen sind umstritten, da sie lösliche Formen von Arsen in die Umwelt einbringen.
Arsen(V)-Verbindungen, die nur organische Liganden enthalten, sind selten, wobei das Pentaphenyl-Derivat As(C 6 H 5 ) 5 das herausragende Mitglied ist .
Organoarsen(III)-Chemie und Verwendungen
Die meisten dieser Verbindungen werden durch Alkylierung von AsCl 3 und seinen Derivaten unter Verwendung von Organolithium- und Grignard-Reagenzien hergestellt . Bekannt sind beispielsweise die Reihen Trimethylarsin ((CH 3 ) 3 As), Dimethylarsenchlorid ((CH 3 ) 2 AsCl) und Methylarsendichlorid (CH 3 AsCl 2 ). Die Reduktion der Chloridderivate mit Hydrid-Reduktionsreagenzien liefert die entsprechenden Hydride, wie Dimethylarsin ((CH 3 ) 2 AsH) und Methylarsin (CH 3 AsH 2 ). Ähnliche Manipulationen gelten für andere Organoarsenchloridverbindungen.
Ein wichtiger Weg zu Dimethylarsenverbindungen beginnt mit der Reduktion von Cacodylsäure (siehe oben):
- (CH 3 ) 2 AsO 2 H + 2 Zn + 4 HCl → (CH 3 ) 2 AsH + 2 ZnCl 2 + 2 H 2 O
- (CH 3 ) 2 AsO 2 H + SO 2 + HI → (CH 3 ) 2 AsI + SO 3 + H 2 O
Eine Vielzahl von Heterocyclen, die Arsen(III) enthalten, sind bekannt. Dazu gehören Arsole , das Arsen-Analogon von Pyrrol , und Arsabenzol , das Arsen-Analogon von Pyridin .
Symmetrische Organoarsen(III)-Verbindungen, zB Trimethylarsin und Triphenylarsin , werden üblicherweise als Liganden in der Koordinationschemie verwendet . Sie verhalten sich wie Phosphinliganden, sind aber weniger basisch. Die diarsine C 6 H 4 (A (CH 3 ) 2 ) 2 , wie bekannt diars ist ein chelatbildendes Ligand . Thorin ist ein Indikator für mehrere Metalle.
Organoarsen(I)-Verbindungen und Verwendungen
Am wenigsten bedeutsam in Bezug auf kommerzielle Anwendungen und Zahlen sind die Organoarsen(I)-Verbindungen. Die Antisyphytika Salvarsan und Neosalvarsan sind Vertreter dieser Klasse. Diese Verbindungen weisen typischerweise drei Bindungen zu As auf, aber nur As-As-Einfachbindungen. Arsen(I)-Verbindungen mit As=As-Doppelbindungen sind selten.
Chemiekrieg
Organoarsenische Verbindungen, insbesondere solche mit As-Cl-Bindungen, wurden vor allem während des Ersten Weltkriegs als chemische Waffen eingesetzt . Berüchtigte Beispiele sind „ Lewisit “ (Chlorvinyl-2-arsendichlorid) und „Clark I“ ( Chlordiphenylarsin ). Phenyldichlorarsin ist ein anderes.
In der Natur
Da Arsen für die meisten Lebensformen giftig ist und in einigen Gebieten in erhöhter Konzentration vorkommt, haben sich mehrere Entgiftungsstrategien entwickelt. Anorganisches Arsen und seine Verbindungen werden beim Eintritt in die Nahrungskette durch einen Methylierungsprozess nach und nach zu einer weniger toxischen Form von Arsen verstoffwechselt . Organoarsenverbindungen entstehen durch Biomethylierung von anorganischen Arsenverbindungen, über Prozesse, die durch Enzyme vermittelt werden, die mit Vitamin B 12 verwandt sind . Beispielsweise produziert der Schimmelpilz Scopulariopsis brevicaulis erhebliche Mengen an Trimethylarsin, wenn anorganisches Arsen vorhanden ist. Die organische Verbindung Arsenobetain , ein Betain , kommt in einigen marinen Lebensmitteln wie Fischen und Algen vor, aber auch in größeren Konzentrationen in Pilzen. Die durchschnittliche Aufnahme einer Person beträgt etwa 10-50 µg/Tag. Werte um 1000 µg sind nach Verzehr von Fisch oder Pilzen keine Seltenheit. Der Verzehr von Fisch ist jedoch kaum gefährlich, da diese Arsenverbindung nahezu ungiftig ist. Arsenobetain wurde erstmals im westlichen Felsenhummer nachgewiesen
An Arsen gebundene Kohlenhydrate , zusammenfassend als Arsenozucker bezeichnet, kommen vor allem in Algen vor . Arsenhaltige Lipide sind ebenfalls bekannt. Obwohl Arsen und seine Verbindungen für den Menschen giftig sind, war Salvarsan eines der ersten synthetischen Antibiotika , dessen Verwendung seit langem eingestellt wurde.
Die einzige aus einer natürlichen Quelle isolierte Polyarsenverbindung ist Arsenicin A , das im neukaledonischen Meeresschwamm Echinochalina bargibanti vorkommt .
Organoarsenverbindungen können je nach Art und Art erhebliche Gesundheitsgefahren darstellen. Arsensäure (As(OH) 3 ) hat eine LD50 von 34,5 mg/kg (Mäuse), während für Betain (CH 3 ) 3 As + CH 2 CO 2 − die LD50 10 g/kg überschreitet.
Repräsentative Verbindungen
Einige illustrative Organoarsenverbindungen sind in der folgenden Tabelle aufgeführt:
| Organoarsen | R | Molmasse | CAS-Nummer | Eigenschaften | |
| 10,10'-Oxybis-10 H -Phenoxarsine |  |
502.2318 | 58-36-6 | ||
| Triphenylarsin | Phenyl |  |
306.23 | 603-32-7 | Schmelzpunkt 58-61 °C |
| Phenyldichlorarsin | Phenyl , Chlor | 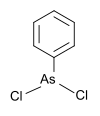 |
222.93 | 696-28-6 | |
| Roxarsone | 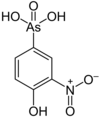 |
263.04 | 121-19-7 | ||
| Arsenobetain | 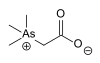 |
64436-13-1 | |||
| Arsenicin A | ![2,4,6-Trioxa-1,3,5,7-tetraarsatricyclo[3.3.1.13,7]decan](https://upload.wikimedia.org/wikipedia/commons/thumb/4/42/Arsenicin_A.png/100px-Arsenicin_A.png) |
389.76 | 925705-41-5 | Schmelzpunkt 182 bis 184 °C (360 bis 363 °F) | |
| Repräsentative Organoarsenverbindungen | |||||
Nomenklatur
Die Benennung von cyclischen Organoarsenverbindungen basiert auf einer Erweiterung des von der IUPAC genehmigten Hantzsch-Widman-Nomenklatursystems , wie im Folgenden zusammengefasst:
| Ringgröße | Ungesättigter Ring | Gesättigter Ring |
|---|---|---|
| 3 | Arsirene | Arsirane |
| 4 | Arsete | Arsetan |
| 5 | Arsole | Arsolane |
| 6 | Arsinin | Arsinan |
| 7 | Arsepine | Arsepane |
| 8 | Arsocine | Arsocane |
| 9 | Brandstiftung | Brandstiftung |
| 10 | Arsecin | Arsekan |
Aufgrund seiner Ähnlichkeit mit dem englischen Slang-Wort " Arsehole " (außerhalb Nordamerikas allgemein verwendet) wurde der Name " Arsole " als Ziel des Spaßes, als "alberner Name" und als eine von mehreren chemischen Verbindungen mit einem ungewöhnlichen Namen angesehen . Dieser Zufall des "albernen Namens" hat jedoch auch zu detaillierten wissenschaftlichen Studien angeregt.
